2.3 从海水中提取溴和碘 知识点题库
含铁元素的物质对人体健康、生产生活都有重要作用,请完成以下填空:
-
(1) 取少量某品牌油漆的原料Fe2O3(红棕色粉末)并加入适量盐酸,反应后得到棕黄色溶液,其离子反应方程式为.取少量棕黄色溶液置于试管中,滴入NaOH溶液,可观察到Fe(OH)3沉淀生成,该离子方程式为.另在小烧杯中加入30mL蒸馏水,加热至沸腾后,向沸水中滴入2mL 上述棕黄色溶液,继续加热至产生色液体,停止加热.证明所得分散系类型的最常用的物理方法为.
-
(2) 一个体重50kg的健康人含铁元素2g,Fe2+易被人体吸收,所以给贫血者补充铁时,服用维生素C可使食物中的Fe3+转化成Fe2+ , 有利于人体对铁的吸收.维生素C在这个反应中表现(“氧化性”或“还原性”).
-
(3) 高铁酸钠(Na2FeO4)能有效地杀灭水中的病菌,同时自身被还原成新生态的Fe(OH)3 , 这是一种品质优良的无机絮凝剂,能高效地除去水中的微细悬浮物.从氧化还原角度分析,杀灭病菌充分利用了Na2FeO4的强.(“氧化性”或“还原性”)
下列变化中必须加入氧化剂才能发生的是( )
A . Na2O→NaOH
B . Fe→FeCl2
C . CuO→Cu
D . H2O2→H2O
某课外学习小组为了探究NO参与的硫酸型酸雨的形成,在烧瓶中充入含有少量NO的SO2气体,先慢慢通入O2 , 一段时间后,再喷射蒸馏水即得硫酸型酸雨.则关于NO的作用说法正确的是( )
A . 还原剂
B . 氧化剂
C . 反应物
D . 催化剂
用硫酸酸化的CrO3遇酒精后,其颜色会从红色变为蓝绿色,用这个现象可以测得汽车司机是否酒后驾车.反应的化学方程式如下:2CrO3+3C2H5OH+3H2SO4═Cr2(SO4)3+3CH3CHO+6H2O此反应的氧化剂是( )
A . H2SO4
B . CrO3
C . Cr2(SO4)3
D . C2H5OH
飞船以铝粉与高氯酸铵的混合物为固体燃料,其中高氯酸铵的反应为2NH4ClO4═N2↑+Cl2↑+2O2↑+4H2O.下列有关叙述不正确的是( )
A . 该反应属于分解反应、氧化还原反应
B . 上述反应瞬间能产生大量高温气体,推动飞船飞行
C . 铝粉的作用是点燃时氧化放热引发高氯酸铵反应
D . 在反应中NH4ClO4只作氧化剂
在2KMnO4 +16HBr=5Br2 +2MnBr2 +2KBr+8H2O反应中,若消耗1 mol氧化剂,则被氧化的还原剂的物质的量是mol。
在下列变化中,必须加入合适的氧化剂才能实现的是( )
A . CuO→Cu
B . H2O2→O2
C . CaCO3→CO2
D . FeCl2→FeCl3
实验室从含碘废液(除H2O外,含有CCl4、I2、I−等)中回收碘,其实验过程如下:
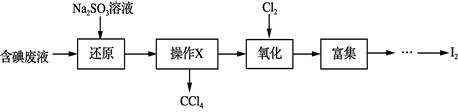
下列叙述错误的是( )
A . “操作X”的名称为萃取,可在分液漏斗中进行
B . “还原”步骤发生的反应为:SO32−+I2+H2O = 2I−+SO42−+2H+
C . “氧化”过程中,可用双氧水替代氯气
D . “富集”即I2富集于有机溶剂,同时除去某些杂质离子
甲醇既是基本有机化工原料,又可作为燃料用于替代矿物燃料。
-
(1) 工业上合成甲醇的反应为:CO(g)+2H2(g)
 CH3OH(g) ΔH。下表所列数据是该反应在不同温度下的化学平衡常数(K)。
CH3OH(g) ΔH。下表所列数据是该反应在不同温度下的化学平衡常数(K)。 温度
250℃
300℃
350℃
平衡常数K
2.041
0.270
0.012
由表中数据判断该反应为 反应(填“吸热”或“放热”)。 某温度下,将2 mol CO和6 mol H2充入2 L的密闭容器中充分反应,达到平衡后,测得c(CO)=0.2 mol/L,则CO的转化率为,此时的温度为(从表中选择)。
-
(2) 已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1 kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2 kJ/mol
③H2O(g)=H2O(l) ΔH3 kJ/mol
则反应 CH3OH(l)+O2(g)=CO(g)+2H2O(l) ΔH= kJ/mol(用ΔH1、ΔH2、ΔH3表示)。
-
(3) 现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O72‾)时,实验室利用如图装置模拟该法:
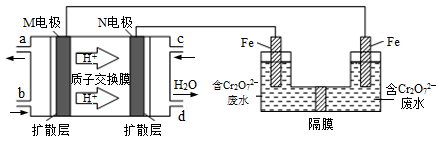
①N电极的电极反应式为 。
②请完成电解池中Cr2O72‾转化为Cr3+的离子反应方程式:
Cr2O72‾ + Fe2+ + = Cr3+ + Fe3+ +
-
(4) 处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10‾5 mol/L 时,Cr3+沉淀完全,此时溶液的pH=。(已知:Ksp=6.4×10‾31 , lg2=0.3)
设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
A . 1mol硫酸钾中阴离子所带电荷数为NA
B . 乙烯(C2H4)和环丙烷(C3H6)组成的28g混合气体中含有4NA个氢原子
C . 22.4L氯气和足量氢气反应转移的电子数为2NA
D . 将0.1mol氯化铁溶于1L水中,所得溶液含有0.2NA个Cl-
下列氧化还原反应中,水只作为还原剂的是( )
A . 3Fe+4H2O(g)  Fe3O4+4H2
B . 2H2O
Fe3O4+4H2
B . 2H2O  2H2↑+O2↑
C . 2Na2O2+2H2O═4NaOH+O2↑
D . 2F2+2H2O═4HF+O2
2H2↑+O2↑
C . 2Na2O2+2H2O═4NaOH+O2↑
D . 2F2+2H2O═4HF+O2
 Fe3O4+4H2
B . 2H2O
Fe3O4+4H2
B . 2H2O  2H2↑+O2↑
C . 2Na2O2+2H2O═4NaOH+O2↑
D . 2F2+2H2O═4HF+O2
2H2↑+O2↑
C . 2Na2O2+2H2O═4NaOH+O2↑
D . 2F2+2H2O═4HF+O2
一种锂离子电池的正极材料中含钴酸锂(LiCoO2)。某离子反应涉及到H2O、H2O2、O2、CoO2、H+、Co2+等微粒,溶液中CoO2、O2的物质的量随时间变化的曲线如下图所示。下列说法错误的是( )
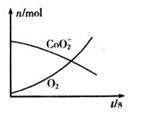
A . 反应中的还原剂是H2O2
B . 氧化性:LiCoO2>O2
C . 氧化剂与还原剂物质的量之比为2:1
D . 若反应生成2.24L(标准状况)O2 , 转移电子0.4mol
下列实验操作、现象与对应结论均正确的是( )
|
序号 |
实验操作 |
现象 |
结论 |
|
A |
向溴水中加入等体积的苯,振荡静置 |
上层接近无色,下层为红棕色 |
Br2在苯中的溶解度 大于在水中的溶解度 |
|
B |
向2mL0.1mol·L-1AgNO3溶液中滴入1mL0.1mol·L-1NaCl溶液后,再滴入1mL0.1mol·L-1Na2S溶液 |
先产生白色沉淀后又变为黑色 |
Ksp(AgCl)>Ksp(Ag2S) |
|
C |
向等体积等浓度的Na2CO3和NaHCO3溶液中各滴1-2滴酚酞溶液 |
溶液均变红且前者颜色较深 |
结合H+能力:CO |
|
D |
将蔗糖和稀H2SO4混合溶液水浴加热,冷却后加入足量NaOH溶液,再加入少量新制Cu(OH)2 , 并加热 |
产生砖红色沉淀 |
蔗糖完全水解 |
A . A
B . B
C . C
D . D
已知,向FeI2溶液中滴加少量的溴水发生反应Ⅰ:2I-+Br2=2Br-+I2;滴加足量的溴水发生反应Ⅱ:2Fe2++4I-+3Br2=2Fe3++6Br-+2I2;现向只含Fe2+、I-、Br-的溶液中通入一定量的Cl2 , 这三种离子的物质的量随n(Cl2)的变化情况如图所示,下列说法错误的是( )
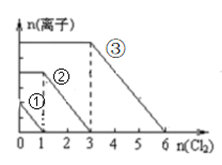
A . 线段①③分别表示的I-、Br-变化情况
B . 由图像可推断n(Fe2+)=6mol
C . 原溶液中n(Fe2+):n(I-):n(Br-)=2:1:3
D . 溶液中已发生的离子反应方程为:2Fe2++2I-+2Cl2=2Fe3++4Cl-+I2 

氧化还原反应广泛存在于生产和生活中,下列没有涉及氧化还原反应的是( )
A . 燃料的燃烧
B . 食物的腐败
C . 钢铁的锈蚀
D . 冰雪的融化
下列关于氧化还原反应的说法中正确的是( )
A . 氧化还原反应前后元素化合价有升降
B . 氧化还原反应前后一定有氧的得失
C . Fe3+→Fe2+的变化过程中,Fe元素发生氧化反应
D . 物质所含元素化合价升高的反应是还原反应
某研究小组为测定软锰矿中MnO2的质量分数,实验步骤如下:准确称取0.5000g软锰矿样品,加入1.34gNa2C2O4再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却、滤去杂质,将所得溶液全部转移到250mL容量瓶中并定容。取出25.00mL待测液置于锥形瓶中,再用0.0100mol/L KMnO4标准溶液进行滴定,当滴入20.00mLKMnO4溶液时恰好完全反应。(已知KMnO4、MnO2在酸性条件下均能将NaC2O4氧化,且还原产物均为Mn2+。)
-
(1) 配制240mL 0.0100mol/L KMnO4标准溶液,若使用分析天平需要KMnO4固体质量为g(保留4位有效数字),需要使用烧杯、量筒、玻璃棒,还缺少的玻璃仪器为(填名称)。
-
(2) 酸化KMnO4溶液可选用的酸是,KMnO4标准溶液应置于(填 “酸式”或“碱式”)滴定管中,原因是。
-
(3) KMnO4和Na2C2O4在酸性条件下反应的离子方程式为。
-
(4) 到达滴定终点的实验现象是。
-
(5) 根据实验数据计算,软锰矿中MnO2的质量分数为%。
权威专家指出:多种海产品如虾、 蟹、牡蛎等,体内含有+5价的砷(As)元素,它对人体是无毒的,但吃饭时一定不要同时大量食用海鲜和橙汁,否则容易中毒,并给出了一个公式:“大量海鲜+大量维生素C→砒霜(As2O3 , 剧毒)”。下列说法错误的是( )
A . 维生素C具有还原性
B . 橙汁中含有维生素
C . 维生素C能将+5价砷还原成+3价
D . 砒霜中毒后可服用维生素C解毒
化学与科学、技术密切相关,下列说法错误的是( )
A . 王亚平太空授课,将泡腾片(含酒石酸和碳酸氢钠)溶于水,在水球内产生气泡,发生的是氧化还原反应
B . 神州十三号返回舱侧壁壳体使用的高强度铝合金材料的主要成分是金属单质
C . 冬奥火炬“飞扬”外壳使用的碳纤维复合材料能耐高温且在空气中不燃烧
D . 冬奥场馆使用 制冷剂制冰是物理过程
制冷剂制冰是物理过程
 制冷剂制冰是物理过程
制冷剂制冰是物理过程
制备纳米颗粒M(化合物)的反应为xFe2++2S2O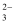 +O2+4OH-=M+S4O
+O2+4OH-=M+S4O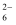 +2H2O。下列说法中,正确的是( )
+2H2O。下列说法中,正确的是( )
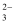 +O2+4OH-=M+S4O
+O2+4OH-=M+S4O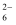 +2H2O。下列说法中,正确的是( )
+2H2O。下列说法中,正确的是( )
A . x=5
B . O2是还原剂
C . M的化学式为FeO
D . 反应中一个S2O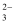 转移的电子数为1
转移的电子数为1
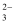 转移的电子数为1
转移的电子数为1
最近更新
- 影响一定数量气体体积大小的主要因素是 A、气体分子的摩尔质量 B、微粒本身的大小C、
- 通电直导线A与圆形通电导线环B固定放置在同一水平面上,通有如图所示的电流时,通电直导线A受到水平向__________的
- 据图中的实验常用仪器回答有关问题.(1)仪器F的名称是. (2)若用KMnO4加热制取氧气,应选用上述仪器中的(填序号)
- 下列加点的字读音不完全相同的一组是 A.要塞 边塞 出塞 阻塞 B.贫血 心
- 请你试着写出三种带有数字“2”的粒子符号并指出其含义: (1)_________________
- 我国古代一个著名的水利工程曾经使成都平原变得“水旱从人,不知饥馑”。这一水利工程是( ) A.都江堰
- 在社会生活中,青年志愿者是一道亮丽的风景线,他们无私奉献的行为 A.诠释了严谨的工作态度
- 读下图,有关我国地势优点的叙述,不正确的是A.有利于东部海上季风带米的湿润气流深入内陆,带来充沛的降水 B.使许
- 在电解液导电时,若在5s内分别有5C的正离子和5C的负离子通过电解槽中与电流方向垂直的截面,电路中电流是多少?若5s内有
- 下面短文中有10处语言错误。请在有错误的地方增加、删除或修改某个单词。 增加:在缺词处加一个漏字符号(∧),并在下面
- 学校为了调查学生在课外读物方面的支出情况,抽取了一个容量为n的样本,其频率分布直方图如图2所示,其中支出在元的同学有30
- 因式分解:= .
- 名篇名句默写 17. ,只是朱颜改。(李煜《虞美人》) 18.
- —I hear you have written a novel. —Yes, the book ________ be
- 《2010年7月中国城市房价排行榜》19日在杭州市揭晓,杭州市房价跃居榜首,新房均价达到25 840元/平方米,创历史最
- (08嘉兴市基础测试)用下列哪种情况的肺炎双球菌感染健康小鼠,会使小鼠生病和死亡 A.加热杀死的有荚膜肺炎双球菌
- 读城市发展模式图后回答下列问题:(1)能正确反映城市发展一般过程的是 A.甲 B.乙
- 两个遗传性状不同的纯种玉米杂交,得到F1在生产上种植能获得高产。若种植到F2则出现产量下降,其原因是 A.F2生命力下降
- A black hole is created when a large star burns out. Like ou
- ,坐看云起时。(王维《终南别业》)
 >HCO
>HCO 



