2.3 从海水中提取溴和碘 知识点题库
-
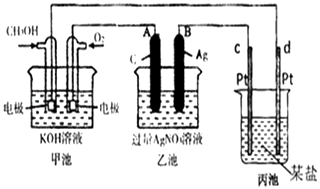
(1) 请回答图中甲池是装置,其中OH﹣移向极(填“正”或“负”)
-
(2) 写出通入CH3OH的电极反应式是
-
(3) 向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为极(填“A”或“B”),并写出此电极反应的电极反应式.
-
(4) 乙池中反应的离子方程式为.
-
(5) 当乙池中B(Ag)极的质量增加2.70g时,乙池的pH是(若此时乙池中溶液的体积为250mL);此时丙池某电极析出0.80g某金属,则丙中的某盐溶液可能是(填序号)
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3 .
 2HNO3+4N2+9H2O,在反应中被氧化与被还原的氨原子数之比为( )
2HNO3+4N2+9H2O,在反应中被氧化与被还原的氨原子数之比为( )
-
(1) 如果煤中的硫全部转化为SO2 , 每天可产生的SO2的质量为多少t;
-
(2) 这些SO2在标准状况下的体积.
-
(1) 在标准状况下制得Cl2多少升?
-
(2) 所得NaOH的物质的量浓度为多少?(电解前后溶液体积保持不变)
①SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2O;②Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O
下列有关叙述正确的是( )
-
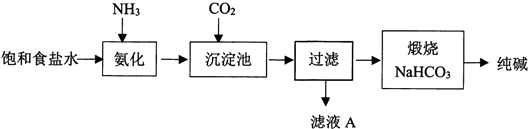
(1) 写出CO2的电子式。
-
(2) 用离子方程式表示纯碱工艺中HCO3-的生成。
-
(3) 工业生产时先氨化再通CO2 , 顺序不能颠倒,原因是。
-
(4) 滤液A中最主要的两种离子是。
-
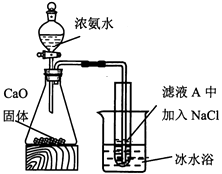
(5) 某小组设计如下实验分离滤液A中的主要物质。打开分液漏斗活塞,一段时间后,试管中有白色晶体生成,用化学原理解释白色晶体产生的原因。
-
(6) 某纯碱样品因煅烧不充分而含少量NaHCO3 , 取质量为m1的纯碱样品,充分加热后质量为m2 , 则此样品中碳酸氢钠的质量分数为。
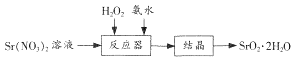
反应原理  该反应放热.
该反应放热.
-
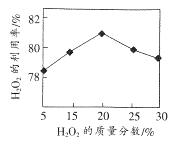
(1) 选择不同浓度的双氧水在反应器中反应,测得相同时间H2O2的利用率随浓度的变化关系如右图所示。5%的H2O2比20%的H2O2利用率低的原因是。
-
(2) SrO2.2H2O遇CO2会反应变质,反应的化学方程式为。
-
(3) 25℃时,将Sr(NO3)2溶液滴加到含有F-、CO32-的溶液中,当混合溶液中c(Sr2+)= 0.0010 mol/L时,同时存在SrF2、SrCO3两种沉淀,则此时溶液中c(F-):c(CO32-)=。
-
(4) 准确称取1.8000 g SrO2·2H2O样品置于锥形瓶中,加入适量的盐酸使之充分转化为H2O2 , 再加入足量KI摇匀后置于暗处,充分反应后,加入少量淀粉试液,用1.0000 moI/L Na2S2O3标准溶液滴定到蓝色恰好消失时,共消耗标准溶液20.00 mL,计算SrO2·2H2O样品的纯度,写出计算过程。(已知:Ksp(SrF2)=4.0×10-9 , Ksp(SrCO3)=5.0×10-9)
-
(1) 实验室用MnO2等为原料制取少量KMnO4的实验流程如下:
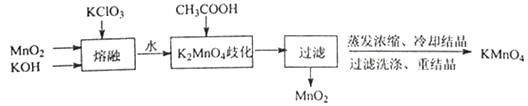
①“熔融”时,可用作坩埚材质的是 (填序号)。
a.氧化铝
b.陶瓷
c.铁
d.玻璃
②“K2MnO4歧化”的离子方程式为。
③“蒸发浓缩”时,温度需控制在80℃,适宜的加热方式是。
-
(2) 高锰酸钾法测定水体COD (化学雷氧量) 的实验步骤如下:
步骤1.准确移取100mL 水样,置于250mL 锥形瓶中。加入10mL1∶3 的硫酸,再加入15.00mL0.0200 mol·L-1KMnO4 溶液(此时溶液仍呈紫红色)。
步骤2.用小火煮沸10min (水中还原性物质被MnO4-氧化,本身还原为Mn2+),取下锥形瓶趁热加10.00mL0.0500mol·L-1Na2C2O4溶液,充分振荡(此时溶液为无色)。
步 骤3.趁热用0.0200 mol·L-1KMnO4溶液滴定至呈微红色,消耗KMnO4 溶液4.500mL。通过计算确定该水样的化学需氧量(写出计算过程)。[已知: COD是指在一定条件下,以氧化1L水样中还原性物质所消耗的氧化剂的量,通常换算为需要的O2的质量(mg),COD的单位mg·L-1。]
①根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸等
②根据反应中是否有电子的转移,将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否具有丁达尔现象,将分散系分为溶液、胶体和浊液
④根据氧化物中是否含有金属元素,将氧化物分为酸性氧化物和碱性氧化物
⑤根据物质在水溶液里或熔融状态下能否导电,将化合物分为电解质和非电解质
-
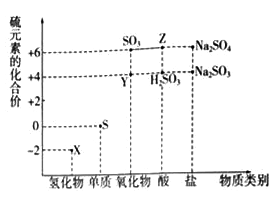
(1) 从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有(填化学式).
-
(2) 将X与Y混合,可生成淡黄色固体.该反应中氧化剂与还原剂的物质的量之比为.
-
(3) Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为.
-
(4) Na2S2O3是重要的化工原料.从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是(填代号).
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
-
(5) 已知Na2SO3能被K2Cr2O7氧化为Na2SO4则24mL 0.05mol•L﹣1的Na2SO3溶液与 20mL 0.02mol•L﹣1的K2Cr2O7溶液恰好反应时,Cr元素在还原产物中的化合价为.
Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O
-
(1) 浓盐酸在反应中显示的性质是 (填字母)。A . 只有还原性 B . 还原性和酸性 C . 只有氧化性 D . 氧化性和酸性
-
(2) 产生0.2 mol Cl2时,转移电子的物质的量为mol。
-
(3) 该反应中氧化产物与还原产物的质量比为。
-
(4) Ⅱ.质量相同的O2、NH3、H2、Cl2四种气体中,在相同温度和相同压强条件下,体积最大的是。
-
(5) 下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是(填序号)。
①NaAlO2 ②Ca(OH)2 ③Na2CO3 ④Al(OH)3
-
(6) Ⅲ.奥运金牌“金镶玉”环形碧玉由昆仑玉制成,昆仑玉的成分可简单看成是Ca2Mg5Si8O22(OH)2 , 则其用二氧化硅和金属氧化物的形式可表示为。
 ―→Mn2+
C . CO2―→
―→Mn2+
C . CO2―→ 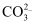 D . S2-―→
D . S2-―→ 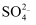
-
(1) 写出两种可以食用的含钠化合物的化学式:。将0.01 mol下列物质(①Na2O2;②Na2O;③Na2CO3;④NaCl)分别加入100 mL蒸馏水中,恢复至室温,所得溶液中阴离子浓度由大到小的顺序是(溶液体积变化忽略不计)。
-
(2) 由于钾比钠更活泼,制备K2O一般是用单质钾还原对应的过氧化物、硝酸盐或亚硝酸盐,试写出用钾与硝酸钾反应制取K2O的化学方程式(还有一种单质生成):。K2O2也有强氧化性,试写出其与SO2发生反应的化学方程式:。
-
(3) 某学生用Na2CO3和 KHCO3组成的某混合物进行实验,测得如表数据(盐酸的物质的量浓度相等且不考虑HCl的挥发)
实验序号
①
②
③
④
盐酸体积/mL
50
50
50
50
固体质量/g
3.06
6.12
9.18
12.24
生成气体体积/L(标况)
0.672
1.344
1.568
1.344
根据数据计算所用盐酸的物质的量浓度为,原混合物样品中n(Na2CO3)∶n(KHCO3)=。
 转移4mol
转移4mol 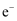 D . 三效催化剂能有效实现汽车尾气中CO、
D . 三效催化剂能有效实现汽车尾气中CO、  、
、  三种成分的净化
三种成分的净化
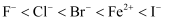 。向
。向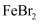 和
和 的混合溶液中通入适量氯气,原溶液中各离子的物质的量变化知下图所示(
的混合溶液中通入适量氯气,原溶液中各离子的物质的量变化知下图所示(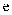 和
和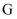 点横坐标为
点横坐标为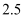 和
和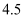 )。下列说法正确的是( )
)。下列说法正确的是( )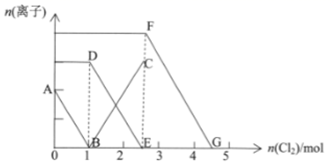
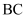 段表示
段表示 物质的量的变化情况
B . 原溶液中
物质的量的变化情况
B . 原溶液中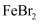 和
和 的物质的量均为
的物质的量均为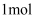 C .
C . 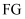 段发生的离子反应为
段发生的离子反应为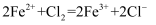 D . 反应
D . 反应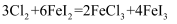 不能发生
不能发生
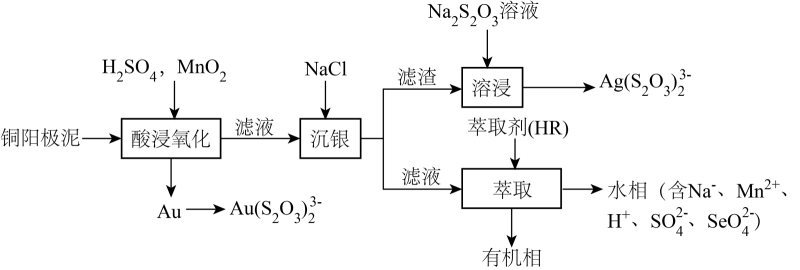
-
(1) Cu2S溶解的离子方程式为;从“有机相”可回收的金属是。
-
(2) 保持其他条件不变,测得Cu元素浸出率、Se元素浸出率和浸出渣率[
 ]随加入
]随加入 的质量变化如图所示。
的质量变化如图所示。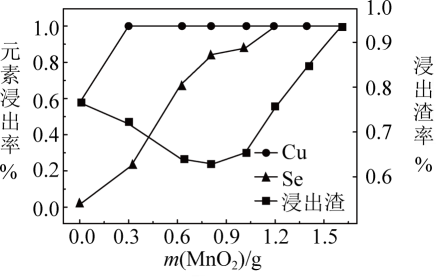
①加入
 的质量约为g时,Cu元素恰好完全浸出。
的质量约为g时,Cu元素恰好完全浸出。②当
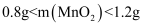 时,Se元素浸出率和浸出渣率均增加的原因是。
时,Se元素浸出率和浸出渣率均增加的原因是。 -
(3) 已知“溶浸”时发生的反应如下:
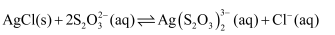
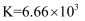 ;
;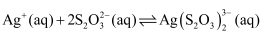
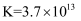
则“沉银”时,溶液中
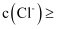
 时,可使Ag+沉淀完全[即
时,可使Ag+沉淀完全[即 ]。
]。 -
(4) 研究发现,硫代硫酸盐浸出金的过程是电化学催化腐蚀过程,催化机理如图所示。
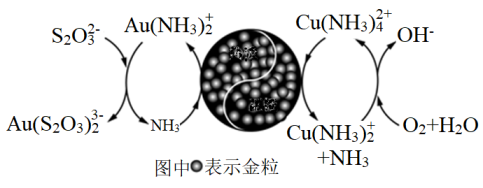
①正极的电极反应式为;浸金过程中的催化剂是(填化学式)。
②若有标准状况下11.2L
 参加反应,浸出金的质量为g。
参加反应,浸出金的质量为g。
- 甲酸的下列性质中,可以证明它是弱电解质的是( )A.1 mol·L-1的甲酸溶液的pH约为2 B.甲酸能与水以任意
- 下列气候类型,冬季多雨的是( ) A、热带雨林气候 B、温带季风气候 C、地
- 在等比数列{an}中,若a3a9=196,a5+a7=35,则q的值为____________.
- People _______drugs have manydifficulties in getting rid of
- “丹顶鹤在跳舞”属于鸟类的哪种繁殖行为 A. 求偶 B.交配 C.产卵
- 人体中占体液总量比例最多的是( ) A.细胞内液 B.细胞外液 C.血浆 D.
- (8分) 我国硫资源紧缺,山东某厂攻克了综合利用生产磷肥剩余石膏废渣制硫酸的技术难关,并且将磷铵、硫酸和水泥实施三联产,
- 名著阅读。(4分)外祖母接过我的钱,急忙塞到裙子的口袋里,垂下眼睑,夸奖我:“谢谢你,好孩子﹗咱俩养活不了自己吗?咱们俩
- 设f是集合A到B的映射,给出下列结论:①A中的每一个元素在B中都有象;②B为A中元素象的集合;③A中的不同元素在B中的象
- 以下经济建设成就在改革开放以后取得的有 ①两弹一星②青藏铁路③大庆油田④三峡水利工程 A.①② B.②③ C.②④ D.
- 简谐横波在同一均匀介质中沿x轴正方向传播,波速为v。若某时刻在波的传播方向上,位于平衡位置的两质点a、b相距为s,a、b
- 点光源S通过带有圆孔的挡板N,照射到屏M上,形成直径为d的亮圆.如果在挡板靠近光屏一侧放上一块厚玻璃砖,如图所示,这时点
- 下列与微生物相关的各项叙述中,正确的是( ) A.大肠杆菌的抗药基因一般位于拟核的DNA上 B.用纤维素酶处理根瘤
- (选做题)【化学——化学与技术】 某省2007年工业(主要是热电厂)二氧化硫排放总量为1.24×106 t,全省酸雨污染
- 韩国“首席科学家”黄禹锡曾因发表有关人类胚胎干细胞论文的造假行为,被处以最高处分——撤销教授职务。胚胎干细胞是哺乳动物或
- 下列有关物质的鉴别、除杂、分离所用的试剂或方法正确的是( ) 选项 实验目的 所用试剂或方法 A 鉴别氯化钾溶液和
- Pleasant music is often played_____classes to make students
- 如果等腰三角形的两边长分别是4和5,则它的周长是( ).A.13 B.14 C.13或14
- 下列实验结果不能作为相应定律或原理的证据之一的是(阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子)A
- 1955年,一位西方记者报道说:万隆会议“最重要的结果是中国变得强大了,她赢得了很多的朋友和善意”。得出这一结论的依据



