第3章 自然界中的元素 知识点题库
下列有关SO2的说法不正确的是( )
A . 把SO2通入紫色石蕊溶液中,石蕊溶液 会变红
B . 把SO2通入品红溶液中,品红溶液会褪色
C . 将足量SO2通入酸性高锰酸钾溶液中,溶液褪色
D . 把SO2通入氯化钡溶液中,溶液会出现白色沉淀
下列叙述不正确的是( )
A . 多余的氯气可以用氢氧化钠溶液吸收
B . 用澄清的石灰石可以鉴别CO2和SO2
C . SO2、Cl2都能使品红溶液褪色,其原理不同
D . 铁丝在氯气中燃烧生成三价铁
取三张蓝色石蕊试纸放在玻璃片上,然后按顺序分别滴加65%的HNO3、98%的H2SO4和新制的氯水,三张试纸呈现的颜色分别是( )
A . 白、红、白
B . 红、黑、白
C . 红、红、红
D . 白、黑、白
碘缺乏症遍及全球,多发生于山区.南美的安第斯山区、欧洲的阿尔卑斯山区和亚洲的喜马拉雅山区是高发病地区.我国云南、河南等10余省的山区发病率也较高.据估计我国患者大约有1000万人.为控制该病的发生,较为有效的方法是食用含碘食盐,我国政府以国家标准的方式规定在食盐中添加碘酸钾(KIO3).据此回答下列问题:
-
(1) 碘是合成下列哪种激素的主要原料之一A . 胰岛素 B . 甲状腺激素 C . 生长激素 D . 雄性激素
-
(2) 长期生活在缺碘山区,又得不到碘盐的供应,易患A . 甲状腺亢进 B . 佝偻病 C . 地方性甲状腺肿 D . 糖尿病
-
(3) 可用盐酸酸化的碘化钾和淀粉检验食盐中的碘酸钾.反应的化学方程式为.氧化产物与还原产物的物质的量之比为.能观察到的明显现象是.
-
(4) 已知KIO3可用电解方法制得.总反应化学方程式为:KI+3H2O
 KIO3+3H2↑.在某温度下.若以12A的电流强度电解KI溶液10min.理论上可得标况下氢气 L.
KIO3+3H2↑.在某温度下.若以12A的电流强度电解KI溶液10min.理论上可得标况下氢气 L.
“关爱生命,拥抱健康”.人们在日常生活中的下列行为会损害人体健康的是( )
A . 用碳酸氢钠焙制糕点
B . 在易碎的食品包装袋中充入氮气
C . 炖排骨时滴加一定量的食醋
D . 用霉变花生(含黄曲霉素)压榨花生油
下列关于硫酸的叙述中,正确的是( )
A . 浓硫酸具有脱水性,因而能使蔗糖炭化
B . 浓硫酸有强氧化性,不可贮存在铝、铁容器中
C . 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
D . 稀释浓硫酸时,应将水沿着器壁慢慢加入到浓硫酸中,并用玻璃棒不断搅拌
下列试剂中,标签上应标注  和
和  的是( )
的是( )
 和
和  的是( )
的是( )
A . C2H5OH
B . HNO3
C . NaOH
D . HCl
化学点亮生活,下列对生活中的化学理解正确的是( )
A . 节日燃放的烟花,是碱金属、锶、钡、铂、铁等金属元素焰色反应呈现的
B . 古代合成颜料中国蓝的化学式为BaCuSi4O10 , 可改写成BaO·CuO·4SiO2
C . MnO2有较强的氧化性,可作H2O2分解的氧化剂
D . 赏心悦目的雕花玻璃是使用烧碱对玻璃刻蚀而成的
海水开发利用的部分过程如图所示。下列说法错误的是( )
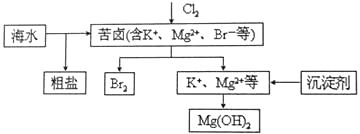

A . 向苦卤中通入Cl2是为了提取溴
B . 粗盐可采用除杂和重结晶等过程提纯
C . 工业生产中常选用NaOH作为沉淀剂
D . 富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
下列说法正确的是( )
A . H2、D2互为同位素
B . CH3CH2CH2CH2CH3和CH3CH2CH(CH3)2互为同素异形体
C . 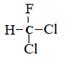 和
和 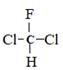 为同一物质
D . CH3CH2OH和CH2OHCHOHCH2OH具有相同的官能团,互为同系物
为同一物质
D . CH3CH2OH和CH2OHCHOHCH2OH具有相同的官能团,互为同系物
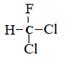 和
和 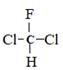 为同一物质
D . CH3CH2OH和CH2OHCHOHCH2OH具有相同的官能团,互为同系物
为同一物质
D . CH3CH2OH和CH2OHCHOHCH2OH具有相同的官能团,互为同系物
下列说法正确的是( )
A . 氯气具有强氧化性,能与铁反应生成FeCl3 , 所以液氯不可用钢瓶储存。
B . 有浓硫酸参与的反应都是氧化还原反应
C . 硅酸钠溶液俗称“水玻璃”,长期露置在空气中生成乳白色凝胶状沉淀
D . 硫在足量空气中燃烧生成大量SO3
自然界中能以游离态存在的元素是( )
A . 硫
B . 氯
C . 溴
D . 氢
利用Cu和浓硫酸制备SO2的反应涉及如图装置,下列说法错误的是( )
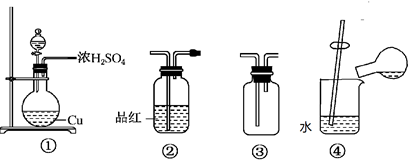
A . 用装置①制备SO2
B . 用装置②检验SO2
C . 用装置③收集SO2
D . 用装置④稀释反应后溶液
下图所示是一种综合处理SO2废气的工艺流程,假设每步都完全反应。下列说法正确的是( )
A . 溶液B中发生的反应为 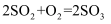 B . 此工艺的优点之一是物质能循环利用
C . 由以上流程可推知氧化性:
B . 此工艺的优点之一是物质能循环利用
C . 由以上流程可推知氧化性:  D . 可用酸性高锰酸钾溶液检验溶液C中是否含有Fe3+
D . 可用酸性高锰酸钾溶液检验溶液C中是否含有Fe3+
 B . 此工艺的优点之一是物质能循环利用
C . 由以上流程可推知氧化性:
B . 此工艺的优点之一是物质能循环利用
C . 由以上流程可推知氧化性:  D . 可用酸性高锰酸钾溶液检验溶液C中是否含有Fe3+
D . 可用酸性高锰酸钾溶液检验溶液C中是否含有Fe3+
利用如图装置能达到相应实验目的的是( )
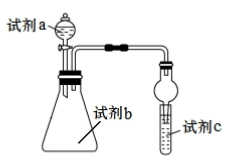
| 选项 | 试剂a | 试剂b | 试剂c | 实验目的 |
| A | 稀盐酸 | NaHCO3 | 澄清石灰水 | 验证得电子能力Cl>C |
| B | 浓氨水 | 生石灰 | 酚酞 | 证明NH3·H2O是弱碱 |
| C | 氯水 | 淀粉KI溶液 | NaOH溶液 | 证明氧化性Cl>I |
| D | 浓硝酸 | 石灰石 | Na2SiO3溶液 | 验证得电子能力N>C>Si |
A . A
B . B
C . C
D . D
下列关于自然界中氮循环(如图)的说法错误的是( )
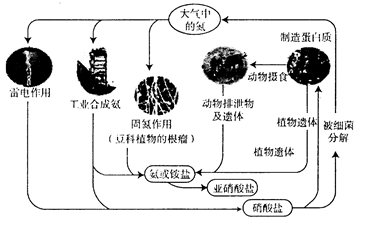
A . 自然界中,含氮有机物和含氮无机物之间可以相互转化
B . 氨与铵盐参与循环成为大气中的游离氮只发生氧化反应
C . 工业合成氨是氮肥工业的基础,氨也是重要的工业原料
D . 在自然界氮循环中,碳、氢、氧三种元素也参加了循环
下列叙述中,不符合化学事实的是( )
A . 1965年我国科学家首次成功合成了结晶牛胰岛素
B . 《梦溪笔谈》中记载“熬胆矾铁釜,久之亦化为铜”,是发生了置换反应
C . 侯氏制碱法所制得“碱”的主要成分是氢氧化钠
D . 五彩缤纷的烟花利用了焰色试验的原理
向BaCl2溶液通入适量的SO2气体,无明显现象,再通入某气体,仍然无明显现象,该气体可能是( )
A . CO2
B . NH3
C . Cl2
D . NO2
-
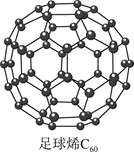
(1) I.碳元素作为一种形成化合物种类最多的元素,其单质及化合物具有广泛的用途。
储能材料是当今科学研究的热点,C60(结构如图)可用作储氢材料。继C60后,科学家又合成了Si60、N60 , 下列有关说法正确的是。
a.C60、Si60、N60都属于新型化合物
b.C60、Si60、N60互为同分异构体
c.已知N60结构与C60相似,由于N-N键能小于N≡N,故N60的稳定性弱于N2
d.已知金刚石中C-C键长154pm,C60中C-C键长145-140pm,故C60熔点高于金刚石
-
(2) II.玻璃生产离不开碳酸盐,原料在熔炉里发生的主要反应如下:2Na2CO3+CaCO3+3SiO2
 2Na2SiO3+CaSiO3+3CO2↑
2Na2SiO3+CaSiO3+3CO2↑ 上述反应中,反应物之一在熔融状态下不导电,该物质属于晶体。写出气体产物的电子式,其属于分子(填“极性”或“非极性”)。
-
(3) 上述反应中,在周期表中相邻的两种元素的原子半径>(填元素符号);处于第三周期的元素名称是;金属性最强的短周期元素原子核外有种不同能级的电子,其单质在O2中燃烧,生成的产物可能有(写化学式)。
-
(4) III.碳元素能形成多种酸,如常见的碳酸、草酸(H2C2O4)等。已知下列3个变化:
 →CO2、
→CO2、  →CO2、Fe3+→Fe2+。
→CO2、Fe3+→Fe2+。 找出其中一个变化与“
 →Mn2+”组成一个反应,写出该反应的离子方程式并配平。
→Mn2+”组成一个反应,写出该反应的离子方程式并配平。 -
(5) 上述反应中的高锰酸钾在不同条件下可发生如下反应:
 +5e+8H+→Mn2++4H2O;
+5e+8H+→Mn2++4H2O;  +3e+2H2O→MnO2+4OH-;
+3e+2H2O→MnO2+4OH-;  +e→
+e→ 
①由此可知,高锰酸根离子(
 )反应后的产物与有关。
)反应后的产物与有关。②高锰酸钾溶液与硫化亚铁发生如下反应:10FeS+6KMnO4+24H2SO4→3K2SO4+6MnSO4+5Fe2(SO4)3+10S↓+24H2O,已知该反应进行一段时间后,固体的质量减少了2.8g,则硫元素与KMnO4之间发生电子转移的数目为个。
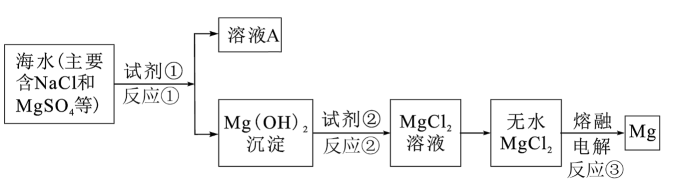
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
-
(1) 镁在元素周期表中的位置是。反应①②③中属于氧化还原反应的有。
-
(2) 为了使
 转化为
转化为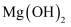 ;试剂①可以选用,确定海水中的
;试剂①可以选用,确定海水中的 已全部转化为
已全部转化为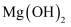 的方法是。
的方法是。
-
(3) 若要检验溶液A中含有的
 , 使用的试剂是。
, 使用的试剂是。
-
(4) 无水
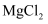 在熔融状态下,通电后会产生Mg和
在熔融状态下,通电后会产生Mg和 , 该反应的化学方程式为。
, 该反应的化学方程式为。
-
(5) 海水中本来就有氯化镁,从海水中制取
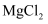 时,却要经历“
时,却要经历“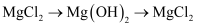 ”的转化。该转化过程的目的是。
”的转化。该转化过程的目的是。
最近更新
- 已知复数z1=(2-i)i,复数z2=a+3i(a∈R),若复数z2=kz1(k∈R),则a=() A.
- 四川雅安发生地震后,某校九(1)班学生开展献爱心活动,积极向灾区捐款。如图是该班同学捐款的条形统计图,写出一条你从图中所
- 补出下列名篇名句中的空缺部分。(6分)(四题任选三题)⑴且夫天地之间,物各有主;_______,_______。(苏轼《
- My sister, who is a red sweater now, a foreign
- 将二倍体芝麻的种子萌发成的幼苗用秋水仙素处理后得到四倍体芝麻,与四倍体芝麻相关的叙述中正确的是() A.与原来的二倍体芝
- 多项式x2+mx+5因式分解得(x+5)(x+n),则m= 6 ,n= 1 .
- One of China’s most famous art forms is the 200-year-
- 阅读下面两首唐诗,然后回答问题。(8 分)洛中访袁拾遗不遇孟浩然阳访才子,江岭作流人。闻说梅花早,何如北地春。(1)两首
- He changed so much that I didn’t r him at firs
- 下列叙述正确的是()A.在碱金属元素中,所有碱金属的氧化物均属于碱性氧化物B.由于碱金属形成的碱均为强碱,所以碱金
- 到1990年,人类已知结构的化学物质是1000万种,2009年9月8日为5000万种。2011年5月23日中国医学科学院
- 五个大小相同的正方体搭成的几何体如图所示,其主视图是()A. B. C. D.
- 补写出下列名篇名句中的空缺部分。(6分) (1)《师说》中韩愈认为弟子不必不如师,师不必贤于弟子的原因是“ ,
- (2011•雅安)已知一次函数y=kx+b,k从2,﹣3中随机取一个值,b从1,﹣1,﹣2中随机取一个值,则该一次函数的
- 我国政府推行的政务公开,就是要把自己掌握的信息以及履行职责的情况向社会公开,增强政府工作的透明度。为此,广东省率先把政务
- Mum is coming. What present _______ for your birthday? A. yo
- I met Anna accident in the street yesterday. A.in
- 下表反映出近代中国对外经济发展呈现的特征是( ) 1895年1913年增长货物性质中国进口1.7亿5.7亿3.3倍生活
- 用“/”给下文断句 诸将已得宋忠颇有喜色上曰宋忠本庸材以利口取给谄谀奸恶货赂得官才掌兵柄便尔骄纵此辈荧惑小人视之如狐鼠耳
- 下面是4位同学对分子、原子、离子的认识,其中正确的是



