第3章 自然界中的元素 知识点题库
亚硝酸钠是一种防腐剂和增色剂,但在食品中过量时会对人体产生危害.其在酸性条件下会产生NO和NO2 . 下列有关说法错误的是( )
A . NaNO2既具有氧化性又具有还原性
B . 食用“醋溜豆芽”可能会减少亚硝酸钠对人体的危害
C . NaNO2和胃酸作用的离子方程式为:2NO2﹣+2H+═NO↑+NO2↑+H2O
D . 1 mol NaNO2在酸性条件下完全反应生成NO和NO2 , 转移电子的物质的量为1 mol
下列有关NaHCO3与Na2CO3的说法中,正确的是( )
A . 分别加热两种样品,没有残留物质是NaHCO3
B . 分别配成溶液,再加入澄清石灰水,无白色沉淀生成的是NaHCO3
C . 分别与相同物质的量浓度的盐酸反应,产生CO2的速率Na2CO3>NaHCO3
D . 常温时在水中的溶解度:Na2CO3>NaHCO3
下列说法正确的是( )
A . 因为氢氟酸显弱酸性,可用于雕刻玻璃
B . 因为液态氨气化时吸热,可用液态氨作制冷剂
C . 明矾溶于水生成氢氧化铝胶体,起消毒杀菌的作用
D . 用铝制容器盛放浓硝酸,是因为铝和浓硝酸不反应
利用下图可以从不同角度研究含氮物质的性质及其转化关系。图中甲~辛均含氮元素。回答下列问题:

-
(1) 下列给出的图中物质之间的转化可以一步实现的是__________。A . 甲→丁 B . 乙→丁 C . 丁→戊 D . 戊→丙
-
(2) 下列说法正确的是____________。A . 丙和丁在一定条件下都能生成戊,属于酸性氧化物 B . “甲→乙→丙→丁→戊”就是工业制戊的转化过程 C . 己和辛在一定条件下都可与固体NaOH作用生成乙,其生成乙的原理相同 D . 如果庚和辛为同种物质,则可由乙和戊反应制得
-
(3) 氯碱工业生产中常用乙检查氯气管道是否泄漏,其现象为。已知反应过程中还有甲生成,该反应的化学方程式为。
-
(4) 已知铁与过量戊的溶液反应,其反应的化学方程式为:Fe+戊→丙+丁+庚+H2O(方程式未配平)。若产物中丙和丁的物质的量之比为1:3,则铁与戊的物质的量之比为。若检验庚中铁元素的价态,可选用的试剂为,反应的离子方程式为。
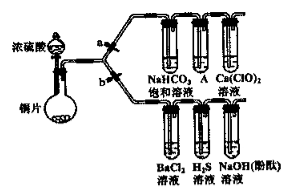
根据要求完成下列实验。(a、b为弹餐夹,其他装置略去)
-
(1) I验证SO2具有氧化性、还原性和酸性氧化物的通性。
连接仪器、检查装置气密性、加药品后,打开b (关闭a),然后滴入浓硫酸,加热。装有浓硫酸的仪器名称是,铜与浓硫酸反应的化学方程式是 。
-
(2) 能验证SO2具有氧化性的实验现象是。
-
(3) 装有BaCl2溶液的试管中无任何现象,将其分成两份,分别滴加氨水和氯水,均产生白色沉淀,沉淀的化学式分别是,。写出其中SO2显示还原性并生成白色沉淀的总的离子方程式。
-
(4) 能验证SO2具有酸性氧化物的通性的实验现象是,若通入过量的SO2 , 其化学方程式是。
-
(5) II验证酸性的相对强弱:碳酸>次氯酸。(已知酸性:亚硫酸>碳酸)
打开a关闭b。装置A中的足量的试剂是。利用该装置能否判断碳酸的酸性比次氯酸强,理由是。
下列物质中,能使淀粉碘化钾溶液变蓝的是( )
A . 氨水
B . 溴水
C . 苏打水
D . 食盐水
一定量的铁、镁和铜的混合物与一定量的浓HNO3恰好反应,得到硝酸盐溶液和NO2、N2O4、NO的混合气体,这些气体与2.24L O2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成硝酸.若向所得硝酸盐溶液中加入2mol/L的NaOH溶液至Fe3+、Mg2+、Cu2+恰好沉淀,则消耗NaOH 溶液的体积是( )
A . 400 mL
B . 200 mL
C . 150 mL
D . 80 mL
下列操作能达到实验目的或不影响实验的是( )
A . 容量瓶用水洗净后,可不经干燥直接用于配制溶液
B . 向煮沸的1 mol/L NaOH溶液中滴加FeCl3饱和溶液制备Fe(OH)3胶体
C . 向溶液中滴加盐酸酸化的氯化钡,若有白色沉淀,说明溶液中含硫酸根
D . 蒸馏时应先加热然后再通冷凝水
某固体试样A是由一定量的Al、Mg均匀组成的混合物,为验证混合物的组成,进行如下实验:
①取m g试样A,全部溶于0.5L 2mol·L-1稀硫酸溶液中,放出11.2 L气体(已换算成标准状况),同时生成溶液B;
②另取m g试样A,加入2mol·L-1的NaOH溶液,当加到100mL时,气体不再生成;
③往溶液B中加入2mol/L NaOH,至沉淀不再发生变化。
根据以上过程回答下列问题:
-
(1) 溶液B中是否含有H+(填“是”或“否”);
-
(2) 写出②中发生反应的离子方程式;
-
(3) 下列能表示过程③产生的沉淀质量W与加入NaOH溶液体积V的关系是;
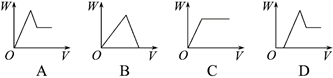
-
(4) m g试样A中含Mg的质量为g;
-
(5) 林同学通过查阅资料,发现浓硫酸与铝发生钝化,但与Mg能剧烈反应生成SO2 , 如果忽略钝化的反应过程,可以通过测定浓硫酸与固体试样反应产生的气体体积,来确定混合物A中镁的质量分数。
郭同学认为林同学的方案可行,但考虑到如果反应结束后硫酸未保持“浓”的状态,测定结果会(填“偏大”、“偏小”或“不变”),其依据是。
某溶液含有Ba2+、Fe2+、Cl-、NO3-等离子,向其中加入足量的稀硫酸后,溶液中离子的物质的量几乎不变的是( )
A . Ba2+
B . Fe2+
C . Cl-
D . NO3-
以下说法正确的是( )
A . 1molCl2和足量Fe反应生成FeCl3转移电子数为3NA
B . Fe与稀HNO3反应,无论生成Fe(NO3)3、Fe(NO3)2 , 还是二者的混合物,被还原的HNO3总是占参与反应的HNO3的 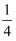 C . 将水蒸气通过灼热的铁粉,铁与水在高温下反应粉末变红
D . 将一定量的铁、铜的混合物加入100mL0.1mol·L-1的FeCl3溶液中,充分反应后溶液中有固体剩余,则剩余的固体中可能含有铜,也可能含有铁
C . 将水蒸气通过灼热的铁粉,铁与水在高温下反应粉末变红
D . 将一定量的铁、铜的混合物加入100mL0.1mol·L-1的FeCl3溶液中,充分反应后溶液中有固体剩余,则剩余的固体中可能含有铜,也可能含有铁
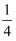 C . 将水蒸气通过灼热的铁粉,铁与水在高温下反应粉末变红
D . 将一定量的铁、铜的混合物加入100mL0.1mol·L-1的FeCl3溶液中,充分反应后溶液中有固体剩余,则剩余的固体中可能含有铜,也可能含有铁
C . 将水蒸气通过灼热的铁粉,铁与水在高温下反应粉末变红
D . 将一定量的铁、铜的混合物加入100mL0.1mol·L-1的FeCl3溶液中,充分反应后溶液中有固体剩余,则剩余的固体中可能含有铜,也可能含有铁
下列物质在给定条件下的转化均能一步实现的是( )
A . Fe3O4  Fe
Fe  FeCl3
B . H2O2
FeCl3
B . H2O2  H2
H2  H2O
C . CaCl2溶液
H2O
C . CaCl2溶液  CaCO3
CaCO3  CO2
D . CuSO4溶液
CO2
D . CuSO4溶液 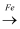 Cu
Cu  CuO
CuO
 Fe
Fe  FeCl3
B . H2O2
FeCl3
B . H2O2  H2
H2  H2O
C . CaCl2溶液
H2O
C . CaCl2溶液  CaCO3
CaCO3  CO2
D . CuSO4溶液
CO2
D . CuSO4溶液 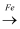 Cu
Cu  CuO
CuO
实验室制取、收集NH3 , 并组装NH3的喷泉实验装置。下列图示装置和原理能达到实验目的的是( )
A . 制NH3  B . 干燥NH3
B . 干燥NH3 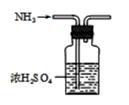 C . 收集NH3
C . 收集NH3 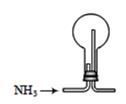 D . 喷泉实验装置
D . 喷泉实验装置 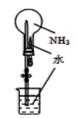
 B . 干燥NH3
B . 干燥NH3  C . 收集NH3
C . 收集NH3  D . 喷泉实验装置
D . 喷泉实验装置 
甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成有关问题的解答。
-
(1) 甲组同学采用如图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有3.2g铜。
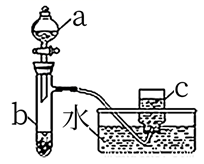
①请写出铜与稀硝酸反应的离子反应方程式:。
②在铜与硝酸的反应中,硝酸所表现出的化学性质主要有。
③若a中液体为浓硝酸,则仪器c中收集的气体主要是(填化学式)。
④待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,生成沉淀的质量是g。
-
(2) 乙组同学对铁与稀硝酸的反应进行探究。他们用amolFe和含有bmolHNO3的稀硝酸进行实验,若两种物质恰好反应都无剩余,且HNO3只被还原成NO,反应结束后溶液中含有Fe3+和Fe2+。
①反应结束后溶液中NO
 的物质的量的取值范围是(用含a的代数式表示)。
的物质的量的取值范围是(用含a的代数式表示)。②若反应结束后的溶液中Fe3+、Fe2+的物质的量之比[n(Fe3+):n(Fe2+)]为3:1,则b:a的值为。
下列实验过程中,始终无明显现象的是( )
A .  通入
通入 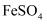 溶液中
B .
溶液中
B .  通入的
通入的 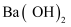 溶液中
C .
溶液中
C .  通入
通入 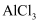 溶液中
D .
溶液中
D .  通入
通入 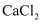 溶液中
溶液中
 通入
通入 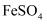 溶液中
B .
溶液中
B .  通入的
通入的 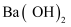 溶液中
C .
溶液中
C .  通入
通入 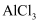 溶液中
D .
溶液中
D .  通入
通入 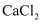 溶液中
溶液中
据文献报道,金红石 Ti3+L3表面催化氮气固定机理如下图所示,下列叙述错误的是( )
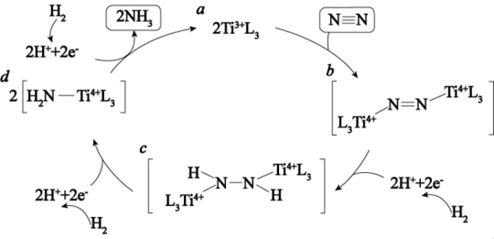
A . 催化剂可以提高固氮速率的原因是改变该反应的 ΔH
B . 该催化固氮总反应为 3H2+N2=2NH3
C . 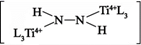 是反应中间体
D . 整个催化过程中存在 N—Ti键的断裂和生成
是反应中间体
D . 整个催化过程中存在 N—Ti键的断裂和生成
100%硫酸吸收SO3可生成焦硫酸(分子式为H2S2O7或H2SO4·SO3)。下列说法错误的是( )
A . Na2S2O7水溶液呈中性
B . 焦硫酸具有强氧化性
C . Na2S2O7可与NaOH溶液反应生成Na2SO4
D . 100%硫酸吸收SO3生成焦硫酸的变化是化学变化
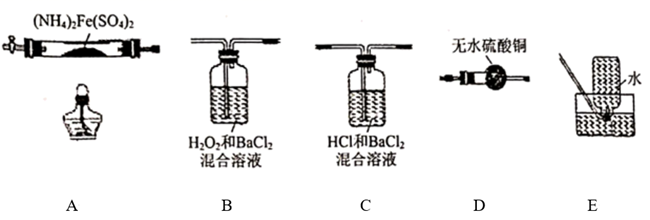
硫酸亚铁铵[(NH4)2Fe(SO4)2]是分析化学中的重要试剂,在不同温度下加热分解所得产物不同。设计如图实验装置(夹持装置略去),在500℃时隔绝空气加热A中的硫酸亚铁铵至分解完全,确定分解产物(铁的氧化物、硫的氧化物、含氮物质、水)的具体成分(已知每个装置中的药品足量)。
-
(1) 利用上述装置完成该实验,则该装置的正确连接顺序为(用装置下面的字母填连接顺序,每个装置都要使用)。加热A前需要通入一段时间N2目的是。
-
(2) 若观察到B中有白色沉淀生成,C中无明显现象,则装置C的作用为,D中白色变为蓝色,写出B中发生反应的离子方程式装置B与装置C能否互换(填 “能”或“否”),原因是(填“能”则不填此空)。
-
(3) A中固体完全分解后变为红棕色粉末,某同学设计实验验证固体残留物仅为Fe2O3 , 而不含FeO,请帮他完成表中内容(试剂,仪器和用品自选)。
实验步骤
预期现象
结论
固本残留物仅为Fe2O3
-
(4) 硫酸亚铁铵在500℃时隔绝空气加热完全分解,若E中收集到的气体只有N2 , A中固体残留物Fe2O3的质量为80g,B中沉淀物质的量为2rnol,则生成N2的质量为g。
-
(5) 某含铬(Cr2O72-)废水用硫酸亚铁铵溶液滴定处理,反应后铁元素和铬元素完全转化为沉淀(沉淀中铬元素化合价为+3),该沉淀经干燥后得到amolFeO•FemCrnO3 , 不考虑处理过程中的实际损耗,则消耗硫酸亚铁铵的物质的量为mol(用a的代数式表示)。
含有同一种元素的物质A、B、C、D、E存在如图转化关系(某些产物及反应条件已省略)。下列有关说法正确的是( )
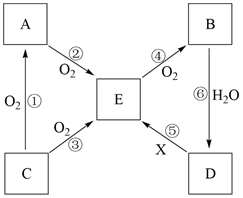
A . 图中除⑥外的其他转化过程一定属于氧化还原反应
B . 工业上实现④转化的条件为高温、高压和催化剂
C . 若A在常温下呈固态,物质C、E均能使溴水褪色
D . 若A在常温下呈气态,C能与D的浓溶液反应而转变为A
SO2有毒,但葡萄酒中都含有少量的SO2 , 以起到保鲜、杀菌和抗氧化的作用。下列说法不正确的是( )
A . 葡萄酒中的SO2对人体无害,因为它的含量很少
B . 葡萄酒中的SO2具有抗氧化的作用,因为SO2具有较强的还原性
C . 从红葡萄酒的颜色可判断出,其中的SO2没有漂白性
D . 葡萄酒倒入酒杯摇一摇,可以减少其中SO2的含量
最近更新
- 第四部分 任务型阅读 (共10小题;每小题1分, 满分10分) 请认真阅读下列短文, 并根据所读内容在文章后表格
- 每年的“十一”黄金周都是旅游的盛宴。据此回答下列小题 12.2015年中秋和“十一”黄金周离得很近,不少游客打算拼假出行
- 点A在x轴上,位于原点的右侧,距离坐标原点5个单位长度,则此点的坐标为 ;点B在y轴上,位于原点的下方,
- 、右图是中国古代利用水力提高生产效率的一项装置示意图, 这项装置主要应用于 A、纺织
- 如图所示操作中错误的是
- 埃及的阿斯旺大坝曾经是埃及民众和政府的骄傲,可是这个大坝建成20多年后,人们发现:沿河流域可耕地的土壤肥力持续下降;下游
- 图13为“长江、黄河干流位置示意图”,读图回答问题。(1)长江、黄河,都发源于 高原,上游 (水或水能)
- 在“探究影响导体电阻大小的因素”的活动中,小明发现实验器材中金属丝只有一根,其它器材足够,如果要他完成下面的一些实验探究
- 流动性偏好是指人们宁愿持有流动性高但不能生利的货币,也不愿持有其他虽能生利但较难变现的资产的心理动机。(例如,人们愿意以
- 已知全集U={1,2,3,4,5,6},A={1,2,3,4},B={3,4,5,6},那么CU(A∩B)=(
- 下列词语中加点字的读音全都相同的一组是( ) A.情致 耄耋 脍炙人口 栉风沐雨 B.煽惑 腥膻
- 下列词语中加点的字,每对读音都不相同的一组是() A.调度/宏观调控 降解/降龙伏虎 搪塞/敷衍塞责 B.省视/省吃俭用
- ......
- ______ you eat the correct foods ______ be able to keep fit
- 阅读下文,完成第1—6题。 天目山 ①去天目山,是心里积存已久的一个念想,不是为观光,是为了那些大树。几十
- 下列各图所表示的生物学意义,叙述正确是 A.正常情况下甲图生物自交后代中会出现基因型为AaBBDd的个体 B.乙图中黑
- 下列生活现象属于物理变化的是()A. 食物腐烂 B. 酒精燃烧 C. 铁生锈 D. 衣服晾干
- 在市场经济条件下,政府必须界定清楚自己的职能。凡是市场机制能够解决的问题政府就不要“越位”;对满足社会需求而必须提供的公
- 如果恒成立,则的取值范围是 .
- 电视剧《贞观长歌》中有很多剧情发生在都城长安的“市”上,下列“市”的场景布置不符合史实的是( ) A.“市”



