第三章 水溶液中的离子平衡 知识点题库
下列条件变化会使H2O的电离平衡向电离方向移动,且pH<7的是( )
A . 常温下,向水中加少量稀盐酸
B . 将纯水加热到100℃
C . 常温下,向水中加少量Na
D . 常温下,向水中加少量Na2CO3固体
下列属于弱电解质的是( )
A . CO2
B . BaSO4
C . HClO
D . Cl2
25℃时,0.1mol/L的HA溶液中 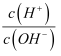 =1010 , 0.01mol/L的BOH溶液pH=12.请回答下列问题:
=1010 , 0.01mol/L的BOH溶液pH=12.请回答下列问题:
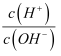 =1010 , 0.01mol/L的BOH溶液pH=12.请回答下列问题:
=1010 , 0.01mol/L的BOH溶液pH=12.请回答下列问题:
-
(1) HA是(填“强电解质”或“弱电解质”,下同),BOH是.
-
(2) HA的电离方程式是.其中由水电离出的c(H+)=mol/L
-
(3) 在加水稀释HA的过程中,随着水量的增加而减小的是 (填字母).A .
 B .
B . 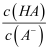 C . c(H+)与c(OH﹣)的乘积
D . c(OH﹣)
C . c(H+)与c(OH﹣)的乘积
D . c(OH﹣)
-
(4) 将等体积等物质的量浓度的HA溶液和BOH溶液混合后的溶液呈性,请用离子方程式解释其原因,混合溶液中各离子浓度由大到小的顺序是.
-
(5) 常温下pH=12的BOH溶液100mL,加0.01mol/L NaHSO4使溶液的pH为11.(混合溶液体积变化忽略不计),应加 NaHSO4mL(保留到小数点后一位)
古代造纸工艺中使用的某种物质存在副作用,它易导致纸张发生酸性腐蚀,使纸张变脆易破损,该物质是( )
A . 明矾
B . 芒硝
C . 草木灰
D . 漂白粉
下列说法中正确的是( )
A . 将H2S通入AgNO3和AgCl的浊液中,观察到黑色沉淀,说明Ksp(AgCl)> Ksp(Ag2S)
B . Ksp越小,难溶电解质在水中的溶解能力一定越弱
C . 相同温度下,在水中和NaCl溶液中分别加入过量AgCl固体,所得溶液中c(Ag+)相同
D . Ksp的大小与离子浓度无关,只与难溶电解质的性质和温度有关
下列物质因发生水解而显碱性的是()
A . HCl
B . CH3COONa
C . NH4Cl
D . KOH
了解化学反应原理,学会健康生活。下列对有关现象及事实的解释错误的是( )
| 选项 | 现象或事实 | 主要原因 |
| A | 热纯碱溶液比冷纯碱溶液除油污效果好 | 热溶液中碳酸钠水解程度大,碱性强 |
| B | 夏天雷雨过后感觉到空气特别的清新 | 空气中O3含量增加、尘埃减少 |
| C | 使用含氟牙膏能防止龋齿 | 牙齿中的羟基磷灰石与牙膏里的氟离子转化成更难溶的氟磷灰石 |
| D | 铜合金水龙头使用长了会生成铜绿 | 发生了析氢腐蚀 |
A . A
B . B
C . C
D . D
下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 硝酸将Fe2+氧化为Fe3+ |
| B | 将铜粉加入1.0mol/LFe2(SO4)3溶液中 | 溶液变蓝,有黑色固体出现 | 金属铁比铜活泼 |
| C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| D | 将0.1mol/LMgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol/LCuSO4溶液 | 先有白色沉淀生成,后变为浅蓝色沉淀 | Cu(OH)2的溶度积比Mg(OH)2的小 |
A . A
B . B
C . C
D . D
-
(1) 泡沫灭火器内装有NaHCO3饱和溶液,该溶液呈(填酸性、碱性、中性),原因(用离子方程式解释);灭火器中另一容器装有Al2(SO4)3溶液,该溶液呈(填酸性、碱性、中性),原因(用离子方程式释)当意外失火时,使泡沫灭火器倒过来即可使药液混合,喷出CO2和Al(OH) 3,阻止火势蔓延。原因(用离子方程式解释)
-
(2) 已知25℃,AgI的饱和溶液中,c(Ag+)=1.22×10-8mol/L,AgCl的饱和溶液中,c(Ag+)=1.25×10-5mol/L。若在5ml含有KCl和KI各为0.01mol/L的溶液中,加入8ml 0.01mol/L AgNO3溶液,这时溶液中所含溶质的离子浓度由大到小的次序是
-
(3) 在某温度下,将H2和I2各0.10mol的气态混合物充入10L的密闭容器中充分反应,达到平衡后,测得c(H2)=0.0080mol/L。该反应的平衡常数 K=;在上述温度下,该容器中若通入H2和I2蒸气各0.20mol,求达到化学平衡状态时c(H2)= ,c(I2)= ,c(HI)=
已知水中存在如下平衡:H2O+H2O⇌H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是( )
A . 加热水至100℃[其中c(H+)=1×10-6mol/L]
B . 向水中加入NaHSO4
C . 向水中加入Cu(NO3)2
D . 在水中加入Na2SO3
下列说法正确的是( )。
A . 实验室从海带中提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取
B . 用玻璃棒蘸取某溶液灼烧,火焰呈黄色并不能说明该溶液中含有钠元素
C . 可用玻璃棒蘸取氯水点在pH试纸上测其pH
D . 配制浓硫酸、浓硝酸的混酸时,应将浓硝酸沿玻璃棒缓慢注入浓硫酸中
25℃时,某混合溶液中c(CH3COOH)+c(CH3COO-)=0.1mol/L,lgc(CH3COOH)、lgc(CH3COO-)、lgc(H+)和lgc(OH-)随pH变化的关系如图所示。已知Ka为CH3COOH的电离常数,下列说法正确的是( )
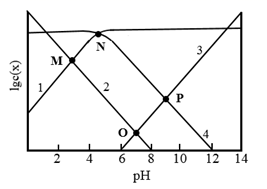
A . 曲线1为lgc(OH)随pH变化的曲线
B . N点时,pOH=14-lgKa
C . 该体系中,c(CH3COO-)= 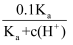 mol/L
D . O点时,c(CH3COOH)=c(CH3COO-)
mol/L
D . O点时,c(CH3COOH)=c(CH3COO-)
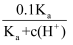 mol/L
D . O点时,c(CH3COOH)=c(CH3COO-)
mol/L
D . O点时,c(CH3COOH)=c(CH3COO-)
下列金属单质和金属化合物的应用错误的是( )
A . 用热纯碱溶液清洗废铁屑表面的油污
B . 明矾既可用于净水,也可用于治疗胃酸过多
C . 常温下可用钢瓶贮存液氯
D . 生石灰可用作食品干燥剂
下列物质的水溶液因水解而呈碱性的是( )
A . NH3
B . Na2S
C . KOH
D . NH4Cl
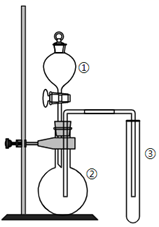
利用如图所示装置进行实验,能达到相应实验目的的是( )
| 选项 | ① | ② | ③ | 实验目的 | |
| A | 浓 | 蔗糖 | 品红溶液 | 检验是否有 | |
| B | 稀 | 某盐溶液 | 澄清石灰水 | 检验盐溶液中是否含有 | |
| C | 浓盐酸 | | | 比较非金属性:Cl与S | |
| D | 浓 | 浓盐酸 | | 比较 |
A . A
B . B
C . C
D . D
二氯异氰尿酸钠[(CNO)3Cl2Na]是常用的杀菌消毒剂,常温下为白色固体,难溶于冷水。某同学利用高浓度的NaClO溶液和(CNO)3H3固体,在10℃时反应制备二氯异氰尿酸钠,实验装置如下图所示(部分夹持装置略)。
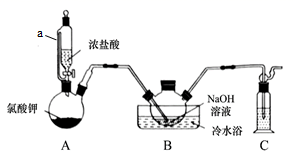
已知:2NaClO + (CNO)3H3 = (CNO)3Cl2Na + NaOH + H2O
回答下列问题:
-
(1) 仪器a的名称为恒压滴液漏斗,与分液漏斗相比其优点是。
-
(2) 待装置B中出现现象时,可由三颈烧瓶上口加入(CNO)3H3固体;反应过程中仍需不断通入 Cl2的理由是。
-
(3) 反应结束后,装置B中的浊液经过滤、、干燥得粗产品。上述装置存在一处缺陷会导致装置B中NaOH利用率降低,改进的方法是。
-
(4) 通过下列实验测定二氯异氰尿酸钠样品中有效氯的含量。
反应原理: [(CNO)3Cl2]-+ H+ +2H2O = (CNO)3H3 + 2HClO, HClO + 2I- + H+ = I2 + Cl-+ H2O, I2 + 2S2O
 = S4O
= S4O 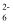 + 2I-
+ 2I-实验步骤:准确称取m g样品,用容量瓶配成250 mL溶液;取25.00 mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,充分反应后,用 c mol/L Na2S2O3标准溶液滴定至溶液呈微黄色。加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液平均为 V mL。
①滴定终点现象为。
②该样品的有效氯含量表达式为 。(该样品的有效氯=
 ×100%)
×100%)
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 3g由 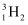 与
与  组成的混合物中含中子总数为NA
B . 1L0.1mol/LNaAlO2溶液中含
组成的混合物中含中子总数为NA
B . 1L0.1mol/LNaAlO2溶液中含  数目为0.1NA
C . 4.4g由乙醛与乙酸乙酯组成的混合物中含氧原子总数为0.1NA
D . 1molH2与2molI2在密闭容器中充分反应后,生成HI分子数为2NA
数目为0.1NA
C . 4.4g由乙醛与乙酸乙酯组成的混合物中含氧原子总数为0.1NA
D . 1molH2与2molI2在密闭容器中充分反应后,生成HI分子数为2NA
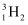 与
与  组成的混合物中含中子总数为NA
B . 1L0.1mol/LNaAlO2溶液中含
组成的混合物中含中子总数为NA
B . 1L0.1mol/LNaAlO2溶液中含  数目为0.1NA
C . 4.4g由乙醛与乙酸乙酯组成的混合物中含氧原子总数为0.1NA
D . 1molH2与2molI2在密闭容器中充分反应后,生成HI分子数为2NA
数目为0.1NA
C . 4.4g由乙醛与乙酸乙酯组成的混合物中含氧原子总数为0.1NA
D . 1molH2与2molI2在密闭容器中充分反应后,生成HI分子数为2NA
“84”消毒液(NaClO溶液)可用于消毒,下列说法正确的是( )
A . 可用pH试纸测定该消毒液的pH
B . NaClO暴露在空气中变质形成HClO
C . NaClO溶液漂白原理与活性炭相同
D . “84”消毒液与“洁厕灵"(HCl)混用,效果更佳.
25℃时,向1L某缓冲溶液(含0.1mol·L-1CH3COOH、0.08mol·L-1CH3COONa)和1L0.1mol·L-1CH3COOH溶液中加入NaOH(s)或通入HCl(g),两种溶液的pH变化如图所示(不考虑溶液体积变化)。已知缓冲溶液pH=pKa-lg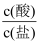 , 下列说法正确的是( )
, 下列说法正确的是( )
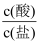 , 下列说法正确的是( )
, 下列说法正确的是( )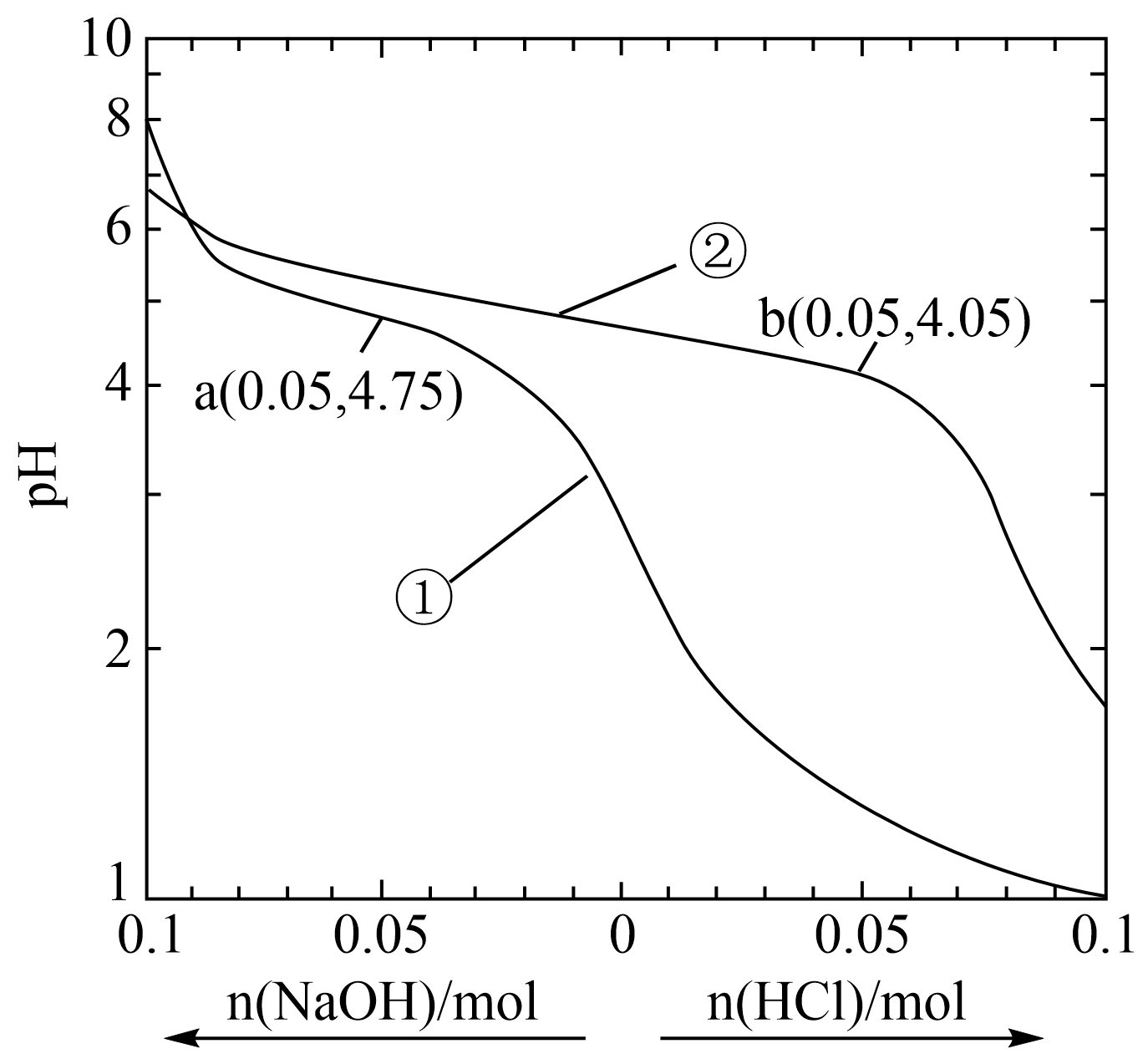
A . 曲线①对应的溶液是缓冲溶液
B . 25℃时醋酸的电离常数的数量级为10-5
C . a点溶液中离子浓度的大小关系为c(CH3COO-)=c(CH3COOH)>c(H+)>c(OH-)
D . b点溶液存在:4c(CH3COOH)+9c(H+)=9c(Cl-)+9c(OH-)+5c(CH3COO-)
酸碱中和滴定实验中,下列说法正确的是( )
A . 中和滴定操作中所需标准溶液越浓越好,指示剂一般加入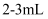 B . 滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁
C . 酸碱指示剂的变色点就是反应终点
D . 滴定前滴定管中的液体液面处于
B . 滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁
C . 酸碱指示剂的变色点就是反应终点
D . 滴定前滴定管中的液体液面处于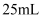 处,滴定过程中用去
处,滴定过程中用去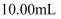 的液体,此时滴定管中剩余液体的体积为
的液体,此时滴定管中剩余液体的体积为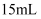
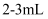 B . 滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁
C . 酸碱指示剂的变色点就是反应终点
D . 滴定前滴定管中的液体液面处于
B . 滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁
C . 酸碱指示剂的变色点就是反应终点
D . 滴定前滴定管中的液体液面处于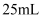 处,滴定过程中用去
处,滴定过程中用去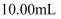 的液体,此时滴定管中剩余液体的体积为
的液体,此时滴定管中剩余液体的体积为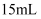
最近更新
- “一送红军,下了山,秋风细雨,缠绵绵。……问一声亲人,红军啊,几时人马,再回山。”这是某部历史电视剧的主题歌,红军被迫
- 词语积累——下列词语的意义,不完全相反的一项是(3分) A.冗长——简短 安谧——喧嚣 孤陋寡闻——
- “天冷穿棉袄,天热扇扇子”主要反映的是( )与地理的关系。 A、生产建设 B、日常生活
- 唐雎不辱使命 《战国策》 秦王使人谓 安陵 君曰:“寡人欲以五百里之地易安陵, 安陵 君其许寡人!” 安陵 君曰:“大
- 2005年11月29日至12月1日,中央经济工作会议在京召开。会议强调,2006年要进一步推进改革开放,加快调整经济结构
- 由乙炔、苯和乙醛组成的混合物,经测定其中碳的质量分数为72%,则氧的质量分数为( ) A.22%
- 已知矩形ABCD,AB=1,BC=.将△ABD沿矩形的对角线BD所在的直线进行翻折,在翻折过程中,() A.存在某个位置
- 蛋白质是由多种氨基酸构成的极为复杂的化合物,丙氨酸是其中的一种.如图是丙氨酸的分子模型,请回答: (1)丙氨酸的分子式为
- 右图是为纪念一部重要文献颁布300周年而发行 的纪念币.这部文献是 A.古罗马的《十二铜表法) B.英国
- 巴黎公社的伟大创举主要表现在( ) A、废除旧的国家机器,建立新的国家机构 B、监督铁路运输和军需生产 C、国家工
- 如图1是一辆汽车做直线运动的s-t图象,对相应的线段所表示的运动,下列哪些说法不正确的是( ) 图1A.AB段
- 关于西亚地理特征的叙述,正确的是A.濒临黑海、地中海、红海、阿拉伯海、里海 B.两河流域是指阿姆河和锡尔河流域C.地形
- It takes me about ________ minutes to go to work by bus ever
- 下列说法不正确的是A.在有机物中碳原子与其他原子最多形成4个共价键B.用溴水既可以鉴别甲烷和乙烯,也可以除去甲烷中的乙烯
- 《全球通史》记述意大利准备侵略埃塞俄比亚时写道:“墨索里尼在拿定主意后决定立即行动,因为他认为当时外交形势对他很有利。”
- 如图是生活中一些常见物质的pH,其中能使无色酚酞溶液变红的是() A. 厕所清洁剂 B. 橘子汁 C. 食盐水 D. 炉
- 15. 1919年北京政府教育部主事的条陈中写到“此次罢学风潮,近因由政治问题发生”。条陈中的“政治问题”指( )
- ----- I’m taking part in the English Speaking Contest next
- 如图所示,粗细均匀的U形细玻璃管右端封闭,开口向下竖直放置,长L的横管中充满汞液,封住长L的右管中的气柱.不计温度变化,
- 下图是 60°纬线的地形剖面示意图。判读后完成14--16题。 14.下列盐度与①海域盐度最接近的是 A.40‰

 生成
生成 或
或 

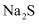 溶液
溶液 悬浊液
悬浊液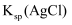 与
与 



