课题2 海水的综合利用 知识点题库
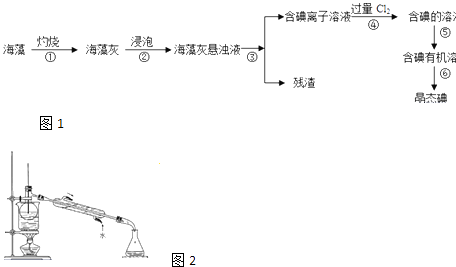
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在,实验室里从海藻中提取碘的流程如下:
![]()
某兴趣小组对上述流程②③的设计如图所示:
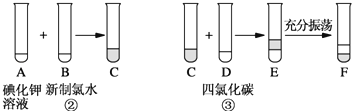
已知②中发生反应的化学方程式为:Cl2+2KI=2KCl+I2 , 回答下列问题:
-
(1) 反应Cl2+2KI=2KCl+I2 的氧化剂是,还原产物是,当生成的I2为2mol时,该反应转移的电子数目为.该反应的离子方程式是:.
-
(2) 写出提取过程中,实验①③的名称.①;③.
-
(3) F中下层液体的颜色为色,上层液体中溶质的主要成分为.
-
(4) 从F中得到的固态碘还需进行的操作是、蒸馏.
-
(5) 流程①中使用到的实验仪器有,流程③中使用到的实验仪器有.
A.试管 B.普通漏斗 C.分液漏斗 D.烧杯 E.玻璃棒.
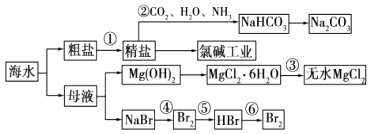
以CaCO3、海水等为原料,可以制备一系列物质,如图所示.下列说法正确的是( )
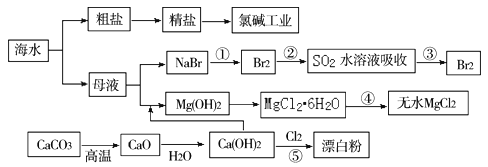
-
(1)
目前,国际上使用的“海水淡化”技术主要有蒸馏法、膜分离方法、电渗析法等.
(1)蒸馏法所需玻璃仪器有酒精灯、锥形瓶、尾接管和 、 .
(2)电渗析法原理如图1所示:
①淡水从 口(填“a”或“b”)流出;为了防止海水中的SO42﹣、Ca2+、Mg2+堵塞交换膜,需加入药品对之净化除去,则药品加入顺序次依是NaOH、 、
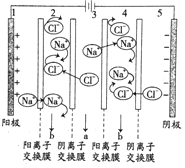
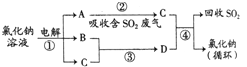
②电渗析法制取淡水的过程中产生的电解产物,用来处理二氧化硫的废气并回收二氧化硫及氯化钠,其循环的流程如图2.请写出反应、有关的化学反应方程式:
-
(2) 海水中蕴含着丰富的化学资源如镁、钾、铀.
(3)从海水中提取镁的部分步骤如下:
m.将蒸发结晶得到的MgCl2•6H2O在一定条件下加热,得到无水MgCl2;
n.电解熔融的氯化镁制金属镁.
步骤m中的“一定条件”指的是 ,目的是 ;步骤n不用熔融氧化镁制金属镁的原因是
(4)铀是核反应最重要的燃料之一,已经研制成功一种螯合型离子交换树脂,它专门吸附海水中的U4+ , 而不吸附其他元素.其反应原理为 (树脂用HR代替),发生离子交换后的离子交换膜用酸处理还可再生并得到含铀的溶液,其反应原理为
-
(1) 海水中蕴含的元素有80多种,它是一个巨大的宝藏.
①海水中镁的总储量约为1.8×1015 t,海水里镁的存在形式主要是 .(填“游离态”或“化合态”)
②下列物质不经过化学变化就能从海水中获得的是 .(填字母)
A.单质钠 B.单质钾 C.氯化钠
③目前化学工业的主要支柱之一是氯碱工业,它是以 为基础制取氯气等产品的工业.
-
(2) 材料是人类生存和发展的物质基础,合理使用材料可以改善人类生活.
①工业上制造光导纤维的基本原料是 .
②下列物质中,不能用来制造耐火材料的是 .(填字母)
A.氧化镁 B.过氧化钠 C.三氧化二铝
③在生铁和钢这2种金属材料中,含碳量较高的是
-
(3) 保持洁净安全的生存环境已成为全人类的共识.
①pH< 的雨水称为酸雨.燃煤产生的 是引起我国酸雨的主要原因.
②下列物质中,会破坏臭氧层的是 .(填字母)
A.氮气 B.一氧化碳 C.氟氯烃
③在生产中,人们曾用浓氨水来检验氯气管道是否漏气,已知能发生的反应为(在有水蒸气存在时):2NH3+3Cl2=6HCl+N2 , 则如果氯气管道某处漏气,用该方法检查时的现象是
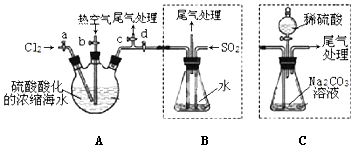
①连接A与B,关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
②关闭a、c,打开b、d,向A中鼓入足量热空气;
③进行步骤②的同时,向B中通入足量SO2;
④关闭b,打开a,再通过A向B中缓慢通入足量Cl2;
⑤将B中所得液体进行蒸馏,收集液溴.
请回答:
-
(1) 判断步骤①中反应已经结束的最简单方法为.
-
(2) 步骤②中鼓入热空气的作用为;
步骤③B中发生的主要反应的离子方程式为.
-
(3) 综合分析步骤①、②、③和④,这四步操作的最终目的为.
-
(4) 此实验中尾气可用(填选项字母)吸收处理.
a.水 b.浓硫酸 c.NaOH溶液 d.饱和NaCl溶液
-
(5) 步骤⑤中,蒸馏用到的玻璃仪器除酒精灯、温度计、尾接管、锥形瓶外,还有和;要达到提纯溴的目的,操作中应控制的关键条件为.
-
(6) 若直接连接A与C,进行步骤①和②,充分反应后,向锥形瓶中滴加稀硫酸,再经步骤⑤,也能制得液溴.滴加稀硫酸之前,C中反应生成了NaBr、NaBrO3等,该反应的化学方程式为.
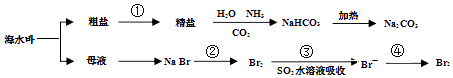
-
(1) 指出上述提取碘的过程中有关实验操作的名称:步骤③,步骤⑤.
-
(2) 写出步骤④对应反应的离子方程式:
-
(3) 提取碘的过程中,可供选择的有机试剂是 (填编号)A . 醋酸 B . 苯 C . 四氯化碳 D . 酒精
-
(4) 为了使海藻灰中的碘离子转化为碘的有机溶液,即完成步骤③至⑤,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网、以及必要的夹持仪器和物品,尚缺少的玻璃仪器是.
-
(5) 从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏.指出如图实验装置中存在的错误之处:.
-
(1) 海水中盐的开发利用:
①海水制盐目前以盐田法为t,建盐田必须选在远离江河入海口,多风少雨,潮汐落差大且又平坦空旷的海滩.所建盐田分为贮水池、蒸发池和池.
②目前工业上采用比较先进的离子交换膜电解槽法进行氯碱工业生产,在电解槽中阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,请说明氯碱生产中阳离子交换膜的作用:(写一点即可).
-
(2) 电渗析法是近年发展起的一种较好的海水淡化技术,其原理如图所示.其中具有选择性的阴离子交换膜和阳离子交换膜相间排列.请回答下面的问题:
①海水不能直接通入到阴极室中,理由是.
②A口排出的是(填“淡水”或“浓水”)
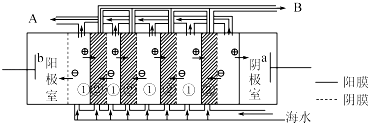
-
(3) 用苦卤(含Na+、K+、Mg2+、Cl﹣、Br﹣等离子)可提取溴,其生产流程如下
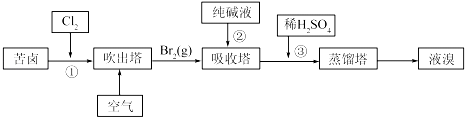
①若吸收塔中的溶液含BrO3﹣ , 则吸收塔中反应的离子方程式为:
②通过①氯化已获得含Br2的溶液.为何还需经过吹出、吸收、酸化重新获得含Br2的溶液?.
③向蒸馏塔中通入水蒸气加热.控制温度在90℃左右进行蒸馏的原因是.
产品标准 | GB5461 |
产品等级 | 一级 |
配料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50mg/kg |
分装时期 | |
分装企业 |
-
(1) 写出碘酸钾与碘化钾在硫酸酸化条件下的化学方程式:.
-
(2) 上述反应生成的I2可用四氯化碳检验.向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳.
①Na2SO3稀溶液与I2反应的离子方程式是.
②某学生设计回收四氯化碳的操作为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体
d.将分液漏斗充分振荡后静置
其中,上述操作正确的顺序是:(填序号)
-
(3) 已知:I2+2S2O32﹣═2I﹣+S4O62﹣ . 某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10﹣3mol•L﹣1的Na2S2O3溶液10.0mL,恰好反应完全.
①判断c中反应恰好完全依据的现象是.
②b中反应所产生的I2的物质的量是mol.
③根据以上实验和包装袋说明,所测精制盐的碘含量是mg/kg.(以含w的代数式表示)
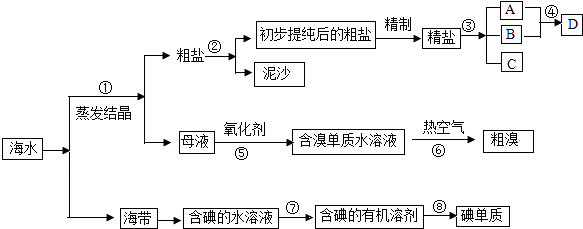
请根据以上信息回答下列问题:
-
(1) 写出步骤②、⑧分离提纯的方法:
②⑧.
-
(2) 步骤⑦分离提纯过程中需要选用的玻璃仪器除烧杯外,还需要的仪器是.
-
(3) D具有杀菌消毒的作用,请写出反应④的化学方程式.
-
(4) 初步提纯后的粗盐中含有Ca2+、Mg2+、SO42﹣等杂质,精制时所用的试剂为:
①盐酸 ②氯化钡溶液 ③氢氧化钠溶液 ④碳酸钠溶液,
下列试剂添加顺序合理的是 .
A . ②③④① B . ③④②① C . ④③②① D . ③②④① -
(5) 若用来提取Br2 , 反应⑤所用的氧化剂的来源较合理的是 .A . 从外地购买 B . 在当地新建生产厂 C . 从本厂生产烧碱处循环
-
(6) 流程⑥将溴单质从水溶液中分离出来是基于溴单质具有性,该方法对比有机溶剂萃取法的优点是.
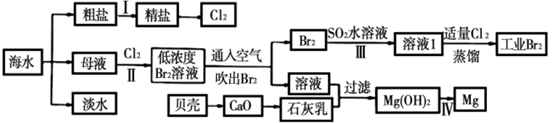
 等杂质离子,精制时加入试剂的顺序可以是氯化钡溶液、氢氧化钠溶液 、碳酸钠溶液 、稀盐酸
C . 提取溴时,已经获得Br2又将Br2还原为Br- , 其目的是富集溴元素
D . 提取镁时,从Mg (OH)2只需一步反应即可得到Mg单质
等杂质离子,精制时加入试剂的顺序可以是氯化钡溶液、氢氧化钠溶液 、碳酸钠溶液 、稀盐酸
C . 提取溴时,已经获得Br2又将Br2还原为Br- , 其目的是富集溴元素
D . 提取镁时,从Mg (OH)2只需一步反应即可得到Mg单质
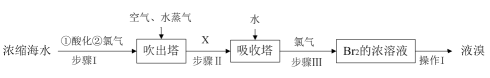
下列说法错误的是( )
 +2Br-
B . 步骤I与步骤III中发生的主要反应相同
C . 操作I中将液溴分离出来的方法可用裂化汽油进行萃取、分液然后再蒸馏
D . 工业上每获得1molBr2 , 需要消耗标准状况下Cl2的体积大于44.8L
+2Br-
B . 步骤I与步骤III中发生的主要反应相同
C . 操作I中将液溴分离出来的方法可用裂化汽油进行萃取、分液然后再蒸馏
D . 工业上每获得1molBr2 , 需要消耗标准状况下Cl2的体积大于44.8L
-
(1) Ⅰ.保证食品安全、保持营养均衡,是保障人体健康的基础。
由于化学物质使用不当,给人印象不佳的化学名词越来越多:苏丹红、三聚氰胺……。下列做法不会危及人体健康的是____(填字母)。
A . 为改善食品品质而加入规定范围内的食品添加剂 B . 用霉变花生压榨食用油 C . 用小苏打做糕点的疏松剂 D . 用工业盐亚硝酸钠腌制鱼肉 -
(2) Ⅱ.20世纪90年代初,国际上提出了“预防污染”这一新概念。绿色化学是“预防污染”的根本手段,它的目标是研究和寻找能充分利用的无毒害原材料,最大限度地节约能源,在化工生产各个环节中都实现净化和无污染。
下列各项属于“绿色化学”要求的是____(填字母)。
A . 处理污染物 B . 治理污染点 C . 杜绝污染源 -
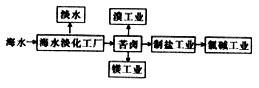
(3) Ⅲ.资源的利用有着重要的意义。我国具有广阔的海岸线,海洋中蕴含着丰富的资源。下面是海水综合利用联合工业体系的简图:
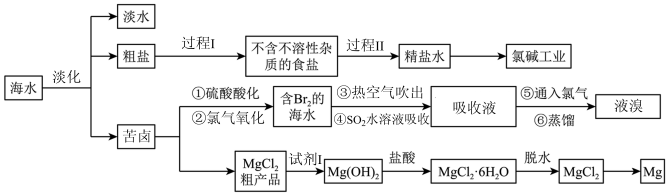
回答下列问题:
过程I采用的操作是。
-
(4) 工业上从海水中提取液溴的流程图中,步骤④除了用
 吸收
吸收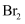 外,理论上下列也能吸收
外,理论上下列也能吸收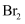 的是____(填字母)。
A .
的是____(填字母)。
A . B .
B .  C .
C .  D . NaCl
D . NaCl
-
(5) 经过步骤①②已获得
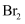 , 不直接用含
, 不直接用含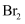 的海水进行蒸馏得到液溴,而要经过“热空气吹出、
的海水进行蒸馏得到液溴,而要经过“热空气吹出、 吸收、通入氯气”后再蒸馏,其目的是。
吸收、通入氯气”后再蒸馏,其目的是。
-
(6) 根据上述反应可判断
 、
、 、
、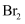 三种物质氧化性由强到弱的顺序是。
三种物质氧化性由强到弱的顺序是。
-
(7) 为了使镁离子沉淀下来,并充分利用当地的贝壳(主要成分为碳酸钙)资源,加入的试剂I是(填化学式)。
-
(8) 步骤⑥的蒸馏过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:。
- 已知关于x的分式方程+=1的解是非负数,则m的取值范围是() A. m>2 B.m≥2
- .说:“改革开放迈不开步子,不敢闯,说来说去就是怕资本主义的东西多了,走了资本主义道路。”“计划经济不等于社会主义,资本
- 已知二次函数(1)求证:无论a为任何实数,二次函数的图象与x轴总有两个交点.(2)当x≥2时,函数值随的增大而减小,求的
- 某溶液中大量存在以下五种离子:NO3-、SO42-、Fe3+、H+、M,其物质的量浓度之比为c(NO3-):c(SO42
- 下列电子排布式属于基态原子的电子排布式的是A.1s22s12p1 B. 1s22s22p3
- 下面A图表示动物精巢内所看到的体细胞分裂及其精子形成过程中染色体、染色单体、DNA数量的变化图,B图表示在上述两种细胞分
- 关于物质结构的下列叙述中,正确的是( ) A.含有共价键的物质一定是共价化合物B.离子化合物中一定存在金属元素
- --Peter, let’s check what westill have left. --Well, it is n
- 2011年8月以来,全国新闻战线开展了“走基层、转作风、改文风”活动。这是基于 ①社会实践是文化创新的源泉和动力
- 如图,一颗豆子随机扔到桌面上,假设豆子不落在线上,则它落在阴影区域的概率为________(A) (
- 依据国家相关法律规定,机动车驾驶员醉驾将受到刑事处罚。检测驾驶员是否酒后驾车,可用一 种装有重铬酸钾(K2Cr2O7)的
- 该漫画反映了当前世界上存在着严重的 ( ) A、人口问题 B、环境问题
- 如果你父母向你询问,家里如何存款更合理,你的回答是 A.尽可能都存定期,这样利息多 B.多存活期,这样用款方便 C.把钱
- 我国东海钓鱼岛经常刮大风,岛上生存着许多无翅或残翅的昆虫,对这一现象的正确解释是() A.有翅昆虫全部被风刮走了
- 在数学学习中,及时对知识进行归纳和整理是完善知识结构的重要方法.善于学习的小明在学习了一次方程(组)、一元一次不等式和一
- 下列物质属于非电解质,但水溶液能导电的是( ) A.Cl2 B.CO2
- 如题17图所示的电容式话筒就是一种电容式传感器,其原理是:导电性振动膜片与固定电极构成了一个电容器,当振动膜片在声压的作
- 下列有关番茄代谢或调节的变化趋势图,正确的是 A.番茄植株在不同种植密度下光合作用强度的变化B.两组番茄植株分别在正常和
- 3.下列各句中,加点的词语运用正确的一项是 A.从2006年开始,我们就起动了城墙保护工程,拆除违章建筑,对部分墙体进行
- 已知数列满足,求数列的通项公式。



