课题2 海水的综合利用 知识点题库
(1)电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有Ca2+、Mg2+、SO42﹣等杂质,所以在进入电解槽前需要进行精制,通常可以选用Na2CO3、NaOH、BaCl2作为除杂质的试剂,则加入三种试剂的先后顺序为 ;加入Na2CO3后所发生反应的离子方程式为 ;若食盐水不经过精制就直接进入离子膜电解槽,可能出现的后果是 .
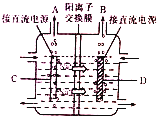
(2)如图是工业上电解饱和食盐水的离子交换膜电解槽示意图(阳极用金属钛网制成,阴极用碳钢网制成),则B处产生气体的化学式为 ,C电极的名称是 ,电解总反应的化学方程式为 ;
(3)从阳极槽出来的淡盐水往往含有少量的溶解氯,需要加入8%﹣9%的亚硫酸氢钠溶液将其彻底除去,该反应的离子方程式为 ;
(4)已知在电解槽中,每小时通过1A的直流电理论上可以产生1.492g的烧碱,某工厂用300个电解槽串联生产8小时,制得32%的烧碱溶液(密度为1.342t/m3)113m3 , 电解槽的电流强度为1.45×104A,则该电解槽的电解效率η(NaOH)= .[提示:η=(产品的实际产量/产品的理论产量)×100%].
-
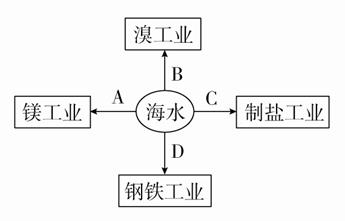
(1) 将海水浓缩后,向其中通入氯气,将溴化物氧化,以溴化钠为例,用化学方程式表示该反应,该反应属于四种基本反应类型中的反应,也属于反应(选填“氧化还原反应”或“非氧化还原反应”).
-
(2) 向上述混合液中吹入热空气,将 生成的溴吹出,是根据溴的沸点比水的沸点(选填“低”或“高”)的性质,吹出的溴用碳酸钠溶液吸收,这一过程的化学方程式为3Br2+3Na2CO3═5NaBr+NaBrO3+3CO2↑,生成物中溴元素的化合价分别为价. 这一类型的化学反应称为歧化反应.
-
(1) 指出提取碘的过程中有关的实验操作的名称:①,③.
-
(2) 提取碘的过程中,可选择的有机溶剂是 .A . 酒精 B . 醋酸 C . 四氯化碳
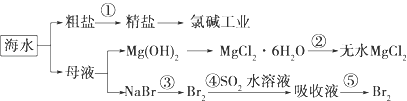
下列有关说法正确的是( )
①FeS2  SO3
SO3  H2SO4
H2SO4
②Al2O3  NaAlO2(aq)
NaAlO2(aq) 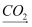 Al(OH)3
Al(OH)3
③NaCl(aq)  Na
Na  Na2O2
Na2O2
④Fe  FeSO4(aq)
FeSO4(aq) 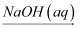 Fe(OH)2
Fe(OH)2 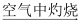 Fe2O3
Fe2O3
⑤海水 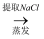 母液
母液  粗溴
粗溴 

 Br2 .
Br2 .
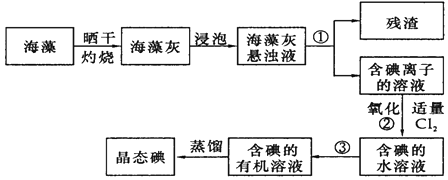
指出提取碘的过程中有关实验操作名称:①,③;写出过程②中有关反应的离子方程式.

干海带  海带灰
海带灰  浸泡液
浸泡液  I2(CCl4)→I2
I2(CCl4)→I2
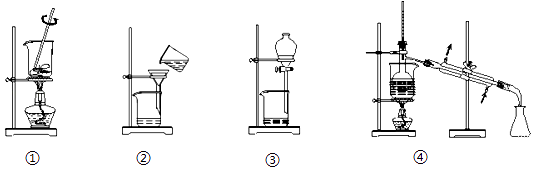
从A~C中选择适当的装置填空(填字母): 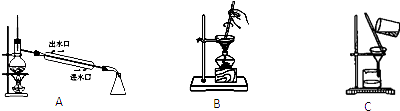
-
(1) 过滤操作时用到的装置是.
-
(2) 从I2的CCl4溶液中提取单质I2并回收CCl4的可用装置.
-
(3) 萃取分液时用到的主要玻璃仪器是,分液后得到的下层液体颜色为.
-
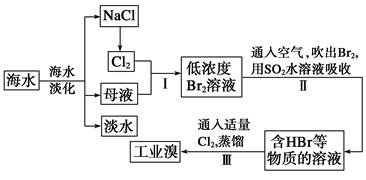
(1) 请列举海水淡化的两种方法:、。
-
(2) 步骤Ⅰ中已获得Br2 , 步骤Ⅱ中又将Br2还原为Br- , 其目的是。
-
(3) 步骤Ⅱ用SO2水溶液吸收Br2 , 吸收率可达95%,有关反应的化学方程式为, 由此反应可知,除环境保护外,在工业生产中应解决的主要问题是。
-
(1) 下图是从海水中提取镁的简单流程。
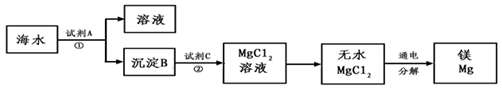
①工业上常用于沉淀Mg2+的试剂A是。
②由无水MgCl2制取Mg的化学方程式是。
-
(2) 海带灰中富含以I-形式存在的碘元素.实验室提取I2的途径如下所示:
干海带
 海带灰
海带灰  滤液
滤液 
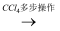 I2
I2①灼烧海带至灰烬时所用的主要仪器名称是 。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式。
③反应结束后,加入CCl4作萃取剂,采用萃取—分液的方法从碘水中提取碘,主要操作步骤如图:
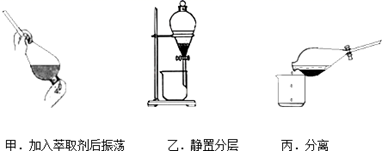
甲、乙、丙3步实验操作中,错误的是 (填“甲”、“乙”或“丙”)。
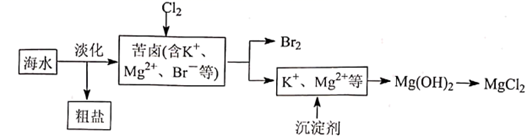
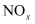 是形成酸雨的主要物质
是形成酸雨的主要物质
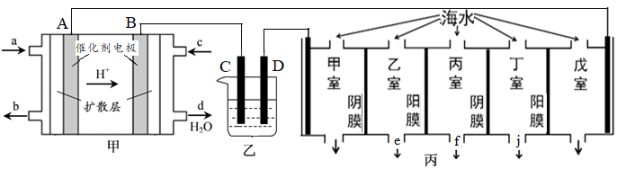
-
(1) 甲装置中c口通入的气体是,A电极的电极反应式为。
-
(2) 乙装置用来模拟精炼和电镀。
①若用于粗铜的精炼,装置中电极C是(填“粗铜”或“纯铜”),工作一段时间后,电解质CuSO4溶液的浓度将(填“增大”“减小”或“不变”)。
②若用于电镀金属银,则电镀液宜使用溶液,镀件是(填“C”或“D”)。
-
(3) 电渗析法是海水淡化的常用方法,某地海水中主要离子的含量如下表,现利用“电渗析法”进行淡化,技术原理如图丙所示(两端为惰性电极,阳膜只允许阳离子通过,阴膜只允许阴离子通过)。
离子
Na+
K+
Ca2+
Mg2+
Cl-

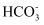
含量/mg·L-1
9360
83
200
1100
16000
1200
118
①淡化过程中在室中易形成水垢[主要成分CaCO3和Mg(OH)2],该室中除发生电极反应外,还发生反应的离子方程式为。
②产生淡水的出水口为 (选填“e”、“f”、“j”)。
![]()
下列说法错误的是( )
- 如果指数函数y=在x∈R上是减函数,则a的取值范围是 ( ) A.a>2 B.a<3
- 《德意志帝国宪法》规定:“联邦议会与帝国议会的召集、开会、延会、闭会之权属于皇帝。“‘联邦议会的主席职位及其事务的领导权
- 阅读下文,完成下列各题。 晋侯、秦伯围郑,以其无礼于晋,且贰于楚也。晋军函陵,秦军氾南。佚之狐言于郑伯曰:“国危矣,若使
- 如图所示:甲图中①②表示目镜,③④表示物镜,⑤⑥表示物镜与载玻片之间的距离,乙和丙分别表示不同物镜下观察到的图象.下面描
- 如右图所示,在等臂杠杆两端各系一个等质量的铁球,调平后将球分别浸没在等质量、等质量分数的稀H2SO4和CuSO4溶液中,
- 某同学将番茄幼苗移栽后,开始几天出现萎蔫现象,其主要原因是( ) A.该番茄幼苗对新的环境出现的不适应现象 B.
- 阅读下文,回答问题。黎 明 的 眼 睛端木蕻良⑴三月清晨,把窗子推开,第一片阳光便飞到人们的全身。对着阳光带进来的新鲜空
- 漫画寓意:由于企业排污造成水质受到严重污染,加之有关部门监督管理不力,导致鱼虾死尽,“三个和尚”无水可吃。从经济学角度来
- Theyhave already had some everyday words_________ to the new
- 下列哪个大洲既位于北半球又位于西半球:( ) A.亚洲 B.非洲 C.北美洲
- 2009年3月18日下午,温家宝总理在回答记者问中说到过这样的一句话,“我们懂得一个道理,那就是取火莫若取燧,汲水莫若凿
- 下列选项体现了“国家的统一,社会的安定,有利于社会发展”的有 ( ) ①日本明治维新的成功②德意志帝国的诞生③美
- 函数的图象的大致形状是 ( ) A B C
- 金属R投入稀硫酸中,有气泡产生;镁条插入R的硫酸盐溶液中,有R析出,则R、Mg、Cu的金属活动性顺序是 A.
- 在古代社会,中华文化曾长期走在世界前列。但是随着中国封建统治的日渐没落和西方近代工业文明的巨大冲击,中华文化也经历了衰微
- 如图,PA切⊙O于点A,割线PBC经过圆心O,OB=PB=1,OA绕点O逆时针旋转60°到OD,则PD的长为
- 如图甲所示,水平放置足够长的平行金属导轨,左右两端分别接有一个阻值为R的电阻,匀强磁场与导轨平面垂直,质量m = 0.1
- (本小题满分12分) 在平面直角坐标系中,已知动点到点的距离为,到轴的距离为,且. (I)求点的轨迹的方程; (Ⅱ)若、
- 初速度为零的匀加速直线运动,在第3s、第4s内的总位移是1.2m,则第5s内的位移是A.0.7m
- 设是等比数列的前项和,,则公比 ( ) A、 B、 C、或 D、或



