课题2 海水的综合利用 知识点题库
①通足量氯气 ②将海带烧成灰,向灰中加水搅拌
③加CCl4振荡 ④过滤 ⑤用分液漏斗分液。
合理的操作顺序为
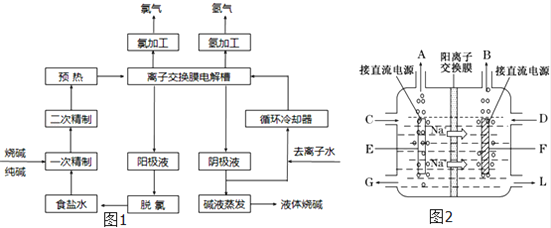
(1)该流程中可以循环的物质是 .
(2)电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有Ca2+、Mg2+、SO42﹣等无机杂质,所以在进入电解槽前需要进行两次精制,写出一次精制中发生的离子方程式,若食盐水不经过二次精制就直接进入离子膜电解槽会产生什么后果 .
(3)图2是工业上电解饱和食盐水的离子交换膜电解槽示意图(阳极用金属钛网制成,阴极由碳钢网制成).则B处产生的气体是 ,E电极的名称是 .电解总反应的离子方程式为 .
(4)从阳极槽出来的淡盐水中,往往含有少量的溶解氯,需要加入8%~9%的亚硫酸钠溶液将其彻底除去,该反应的化学方程式为 .
(5)已知在电解槽中,每小时通过1安培的直流电可以产生1.492g的烧碱,某工厂用300个电解槽串联生产8小时,制得32%的烧碱溶液(密度为1.342吨/m3)113m3 , 电解槽的电流强度1.45×104A,该电解槽的电解效率为 .
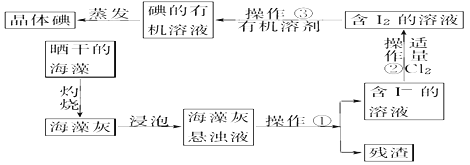
海洋中含碘丰富,其中碘以I﹣形式存在.某实验提取碘的流程如图所示.
-
(1) 下列海产品中可以考虑用于工业上大量地提取碘的是 .
①贝壳 ②紫菜 ③鱼 ④海带
-
(2) 图中海藻灼烧成灰的目的是 指出实验操作①的名称
-
(3) 下列有机溶剂不能用来提取碘的是A . 汽油 B . 四氯化碳 C . 酒精
-
(1) ①称取一定质量的样品;②将样品加水溶解,制成粗盐溶液;③向粗盐溶液中加入过量的某种试剂,过滤;④将沉淀洗涤后小心烘干,得到纯净的固体A;⑤滤液在进行某一操作后,移入蒸发皿进行蒸发,得到纯净的固体;⑥称量实验中得到的某种固体.
步骤②③⑤中都使用到的仪器是;它在步骤②和⑤的操作方法相同,但目的不同,在步骤②的目的是,在步骤⑤的目的是.
-
(2) 步骤③中加入的试剂是;步骤⑤中进行的“某一操作”是,目的是.
-
(3) 步骤⑥中你认为需要称量的固体是固体A还是固体B?,你不选择另一种固体的理由是.
-
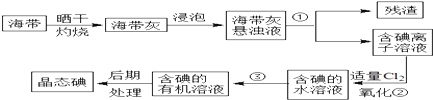
(1) 步骤①的实验操作名称是;
-
(2) 现有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品.完成该实验尚缺少的玻璃仪器是和;
-
(3) 步骤③中能选用CCl4从碘水中萃取碘的原因是(双选) ;A . CCl4与水不互溶 B . CCl4可与I2发生取代反应 C . CCl4的密度比水大 D . CCl4不易燃烧,可作灭火剂 E . 碘在CCl4中的溶解度比在水中大很多
-
(4) 步骤②中反应的离子方程式为;
-
(5) 请设计一种简单的实验方法,检验提取碘后的水溶液中是否还含有单质碘:.
Ⅰ.空气吹出纯碱吸收法.方法是将氯气通入到富含溴离子的海水中,使溴置换出来,再用空气将溴吹出,用纯碱溶液吸收,最后用硫酸酸化,即可得到单质溴.该方法涉及的反应有:
①Cl2+2Br﹣═Br2+2Cl﹣
②3Br2+3CO  ═BrO
═BrO  +5Br﹣+3CO2↑;
+5Br﹣+3CO2↑;
③BrO  +5Br﹣+6H+═3Br2+3H2O
+5Br﹣+6H+═3Br2+3H2O
其中②中的氧化剂是,③中的还原剂是.
Ⅱ.空气吹出SO2吸收法.该方法基本同(Ⅰ),只是将吹出的溴用SO2溶液来吸收,使溴转化为氢溴酸,然后再用氯气氧化氢溴酸即得单质溴.
写出溴与二氧化硫反应的化学方程式.
Ⅲ.溶剂萃取法.该法是利用单质溴在水中和萃取剂中溶解度的不同的原理来进行的.
实验室中萃取用到的主要实验仪器名称是.
下列可以用于海水中溴的萃取的试剂是(填序号).
①乙醇②四氯化碳③硝酸.
 Mg(OH)2
Mg(OH)2  Mg
B . 海水
Mg
B . 海水  Mg(OH)2溶液
Mg(OH)2溶液  MgCl2
MgCl2  Mg
C . 海水
Mg
C . 海水  Mg(OH)2
Mg(OH)2  MgO
MgO  Mg
D . 海水
Mg
D . 海水  Mg(OH)2溶液
Mg(OH)2溶液  MgCl2溶液
MgCl2溶液  MgCl2
MgCl2  Mg
Mg
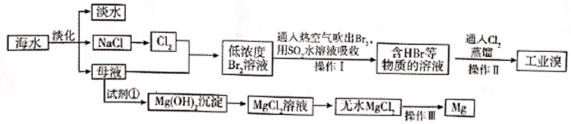
请回答下列问题:
-
(1) 请写出海水淡化的两种方法:、 。
-
(2) 通入热空气吹出Br2 , 利用了Br2的 (填序号)。
a.氧化性
b.还原性
c.挥发性
-
(3) 操作Ⅰ用SO2水溶液吸收Br2 , 有关反应的离子方程式为。
-
(4) 写出操作Ⅱ通氯气后发生的离子方程式。
-
(5) 为使母液中的MgCl2转化为Mg(OH)2 , 从原料来源及经济效益角度考虑, 试剂①最好选用 。
a.氨水
b.氢氧化钙
c.氢氧化钠
-
(6) 操作Ⅲ的化学方程式为 。
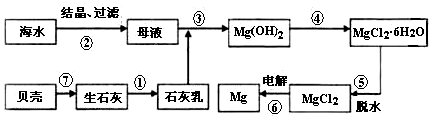
下列说法错误的是( )
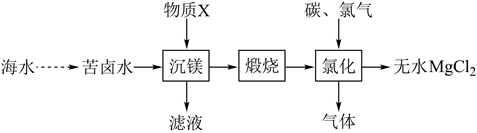
下列说法错误的是( )
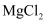 制备金属镁
C . “氯化”过程中发生的反应为
制备金属镁
C . “氯化”过程中发生的反应为  D . “煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水
D . “煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水 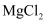
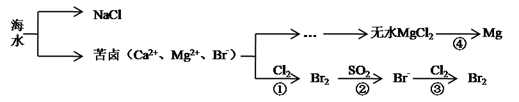
-
(1) 淡化海水的方法有(写一种合理方法即可)。由海水提取的粗盐中含有Ca2+、Mg2+、SO42-等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、(填化学式),之后(填操作名称),再加入适量(填试剂名称)。将所得溶液加热浓缩、冷却结晶,得到精盐。
-
(2) 反应④由无水MgCl2制取金属镁的常用工业方法是。
-
(3) 向苦卤中通入Cl2置换出Br2 , 再用空气吹出溴并用SO2吸收,转化为Br- , 反复多次,
以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是。
-
(4) 工业上也可以用Na2CO3溶液吸收吹出的Br2 , 生成溴化钠和溴酸钠,同时放出CO2。写出反应的离子方程式,最后再用H2SO4处理所得溶液重新得到Br2。
 溶液刻蚀铜制印刷电路板
D . 从海水中提取粗盐
溶液刻蚀铜制印刷电路板
D . 从海水中提取粗盐
-
(1) 一种节能技术是将电解池与燃料电池相组合,相关物料传输与转化关系如下图所示,其中的电极未标出,所用的离子交换膜都只允许阳离子通过。
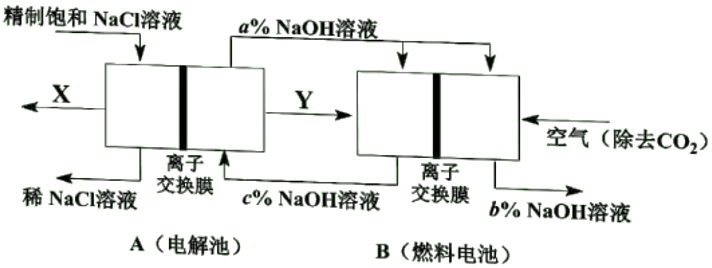
①当产生0.5molX时,A中通过离子交换膜的Na+有mol。
②写出燃料电池B中负极上的电极反应式。
③比较图中NaOH质量分数a%、b%、c%由大到小的顺序。
-
(2) 降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入O2 , 避免水电离的H+直接得电子生成H2 , 降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应式为。
- 一个几何体的三视图如图,则组成该几何体的简单几何体为()A.圆柱和圆锥 B.正方体和
- 跳远训练时,甲、乙两同学在相同条件下各跳10次,统计得,他们的平均成绩都是5.68,甲的方差为0.3,乙的方差为0.4
- Form July to October everyyear, about a quarter of the world
- 读某省区轮廓图,完成下题。图中河流P与长江相比较 A.P河流的水量大
- 我国主要牧区分布在( ) A.南方地区和北方地区 B.西北地区和青藏地区 C.北方地区和西北地区
- How can they learn so much they spend such a lot of
- 如图,小手盖住的点的坐标可能为A.B.C.D.
- 族周期 IA 0 1①ⅡAⅢAⅣAⅤAⅥAⅦA 2 ②③④ 3⑤ ⑥⑦ ⑧ 下表为元素周期表的一部分,请参照元素
- 下列有关人类特有的条件反射的叙述,不正确的是( ) A.由语言、文字等抽象信号刺激引起的条件反射 B.反射弧必须有大脑
- 如果点A(-1, a),B(2, b)在直线y= -2017x+ 2017上,那么a-b的值的符号为_____(填“+”
- A、B、C三种固体物质的溶解度曲线如图所示.有关叙述正确的是()A.t1℃时,A、B、C的溶解度大小关系是A>B=C B
- ......
- 世界上出现的第一个由发达国家和发展中国家组成的区域集团化组织是 A.欧盟 B. 北美自由贸易区
- 对于一定质量的气体,忽略分子间的相互作用力。当温度升高时 A.气体的内能不变 B.气体分子的平
- I didn’t know what “loquacious” meant and had to ________ in
- 下图所示实验操作中,正确的是A.取用液体B.点燃酒精灯C.称量氯化钠固体D.加热固体
- 亚氨基羟锂(Li2NH)是一种储氢容量器,安全性好的固体储氢材料,其储氢原理可表示为Li2NH+H2=LiNH2+LiH
- 已知关于x的方程(1-a)x2+(a+2)x-4=0,a∈R,求:(1)方程有两个正根的充要条件;(2)方程至少有一个
- 选择下列实验方法分离物质,将分离方法的序号填在横线上。 A.萃取分液法 B.加热分解法 C.结晶法 D.分液法 E.蒸馏
- 举世瞩目的上海世博会于2010年4月30日晚在黄浦江两岸盛大开幕。这是一场期待已久的文明盛宴,多元文化共襄盛典,绵延50



