第四节 氨 硝酸 硫酸 知识点题库
-
(1) 硝酸在该反应中体现的性质有.
-
(2) 如果参加反应的Cu和HNO3的物质的量之比是3:10,写出并配平该反应的离子方程式.
-
(3) 0.004molCu被硝酸完全溶解后,Cu失去的电子数是,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是,在标准状况下若将收集NO和NO2的集气瓶倒立于水中,通入一定量的氧气充分反应后发现无气体剩余,则通入O2的体积为 mL;所得溶液(假设溶质不扩散)的物质的量浓度是.
 标志的物质是( )
标志的物质是( )
实验Ⅰ:制取NaClO2晶体按右图装置进行制取。
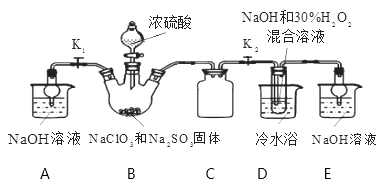
已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,38-60℃时析出NaClO2 , 高于60℃时NaClO2分解成NaClO3和NaCl。
-
(1) 用50%双氧水配制30%的H2O2溶液,需要的玻璃仪器除玻璃棒、胶头滴管、烧杯外,还需要(填仪器名称);装置C的作用是。
-
(2) B中产生ClO2的化学方程式。
-
(3) 装置D中反应生成NaClO2的化学方程式为 。反应后的溶液中阴离子除了ClO2-、ClO3-、Cl-、ClO-、OH—外还可能含有的一种阴离子是,检验该离子的方法是。
-
(4) 请补充从装置D反应后的溶液中获得NaClO2晶体的操作步骤。
①减压,55℃蒸发结晶;②;③;④;得到成品。
-
(5) 如果撤去D中的冷水浴,可能导致产品中混有的杂质是;
-
(6) 实验Ⅱ:样品杂质分析与纯度测定
测定样品中NaClO2的纯度。测定时进行如下实验:
准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2-+ 4I-+4H+ =2H2O+2I2+Cl- , 将所得混合液稀释成100mL待测溶液。
取25.00mL待测溶液,加入淀粉溶液做指示剂,用c mol·L-1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL(已知:I2 +2S2O32-=2I-+S4O62-)。
①确认滴定终点的现象是。
②所称取的样品中NaClO2的物质的量为mol(用含c、V的代数式表示)。
① 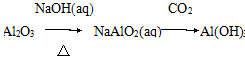
② ![]()
③ ![]()
④ 
⑤ 
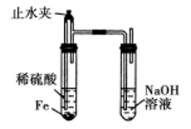 B . 比较碳酸钠与碳酸氢钠的热稳定性
B . 比较碳酸钠与碳酸氢钠的热稳定性 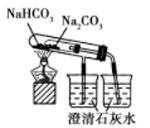 C . 实验室制取少氨气
C . 实验室制取少氨气 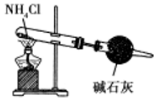 D . 检查装置气密性
D . 检查装置气密性 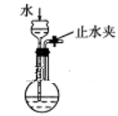
| 选项 | 操作 | 现象 | 解释或结论 |
| A | 向某无色溶液中加入足量稀盐酸酸化的Ba(NO3)2溶液 | 出现白色沉淀 | 溶液中一定存在 |
| B | 用光照射装有甲烷和氯气的混合气体气体的试管 | 颜色逐渐变浅,试管内壁出现油状液滴 | 甲烷与氯气发生了反应 |
| C | 向蔗糖溶液中加3~5滴稀硫酸,将混合液煮沸几分钟,冷却;向冷却后的溶液中加入银氨溶液,水浴加热 | 没有银镜产生 | 蔗糖未发生水解 |
| D | 向盛有某溶液的试管中滴加稀NaOH溶液,将湿润红色石荔试纸置于试管口 | 试纸不变蓝 | 原溶液中无 |
①硫是一种黄色的能溶于水的晶体 ②火山喷出物中含有大量含硫化合物 ③硫在空气中燃烧的产物是二氧化硫 ④硫在纯氧中燃烧的产物是三氧化硫
| 实验操作 | 实验现象 | ||
| 金属为铜 | 金属为锌 | 金属为铝 | |
| 点燃 | 不燃烧 | 燃烧 | 燃烧 |
| 通入 | 褪色 | 褪色 | 褪色 |
| 通入 | 无明显变化 | 无明显变化 | 出现黑色沉淀 |
| 通入品红溶液 | 褪色 | 褪色 | 不褪色 |
已知: 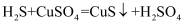 (CuS为黑色固体);
(CuS为黑色固体);  可燃
可燃
下列说法错误的是( )
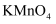 酸性溶液褪色的气体是
酸性溶液褪色的气体是  B . 加入铝片的实验中,燃烧现象能证明生成气体中一定含
B . 加入铝片的实验中,燃烧现象能证明生成气体中一定含  C . 加入锌片的实验中,生成的气体一定是混合气体
D . 金属与浓硫酸反应的还原产物与金属活动性强弱有关
C . 加入锌片的实验中,生成的气体一定是混合气体
D . 金属与浓硫酸反应的还原产物与金属活动性强弱有关
Ⅰ.用已准确称量的KBrO3固体配制一定体积的0.0002 mol·L-1KBrO3标准溶液;
Ⅱ.取5.00 mL上述溶液,加入过量KBr,加H2SO4酸化,溶液颜色呈棕黄色;
Ⅲ.向Ⅱ所得溶液中加入50.00 mL废水,加水稀释至100 mL;量取25.00 mL于锥形瓶中;
Ⅳ.向锥形瓶中加入过量KI;
Ⅴ.用0.0001 mol·L-1Na2S2O3标准溶液滴定Ⅳ中溶液至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液12.00 mL。
已知:I2+2Na2S2O3=2NaI+Na2S4O6;Na2S2O3和Na2S4O6溶液颜色均为无色。
-
(1) Ⅲ中发生反应的化学方程式是。
-
(2) Ⅴ中滴定至终点的现象是。
-
(3) Ⅱ~Ⅳ中反应须在密闭容器中进行,否则会造成测定结果(填“偏高”“偏低”或“无影响”)。
-
(4) 计算该废水中苯酚的含量(写出计算过程)
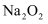 与
与 使品红溶液褪色的原理相同
C . 浓硫酸可以用铁罐车运输,因为
使品红溶液褪色的原理相同
C . 浓硫酸可以用铁罐车运输,因为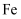 与浓硫酸不反应
D .
与浓硫酸不反应
D .  溶于水反应生成
溶于水反应生成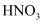 , 所以
, 所以 属于酸性氧化物
属于酸性氧化物
任务I:从以下试剂中选择合适的试剂实现 →
→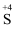 的转化。
的转化。
试剂清单:①浓H2SO4②稀H2SO4③酸性KMnO4溶液④品红⑤Cu
-
(1) 写出实现转化的化学方程式。
-
(2) 设计实验证明实现了该转化(写出操作和现象)。
任务II:实现硫元素在不同价态之间的转化。
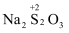 溶液
溶液 SO2
SO2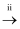 Na2SO3溶液
Na2SO3溶液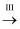 Na2SO4溶液
Na2SO4溶液 -
(3) 欲制备Na2S2O3 , 从氧化还原角度分析,合理的是____(填字母)。A . Na2S+S B . Na2SO3+S C . Na2SO3+Na2SO4 D . SO2+Na2SO4
-
(4) 转化Ⅱ中加入的物质可以是。(填物质类别)
-
(5) 转化Ⅲ可以通入氧气来实现,写出相应离子方程式。
-
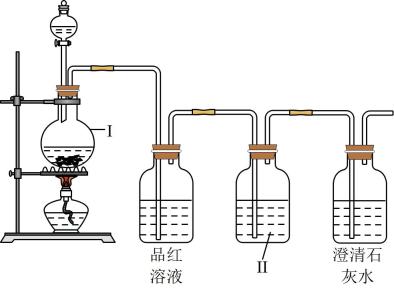
(1) 设备I的仪器名称是。
-
(2) 设备II中盛放的试剂是,该试剂的作用是。
-
(3) 浓硫酸与木炭反应的化学方程式是。
-
(4) 证明产物中含有CO2的实验现象是。
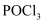 是重要的基础化工原料,某兴趣小组准备用三氯化磷、氯气、二氧化硫制备
是重要的基础化工原料,某兴趣小组准备用三氯化磷、氯气、二氧化硫制备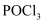 , 产物中还有一种遇水强烈水解的物质
, 产物中还有一种遇水强烈水解的物质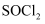 (查资料可知
(查资料可知 遇水强烈水解,易与氧气反应;
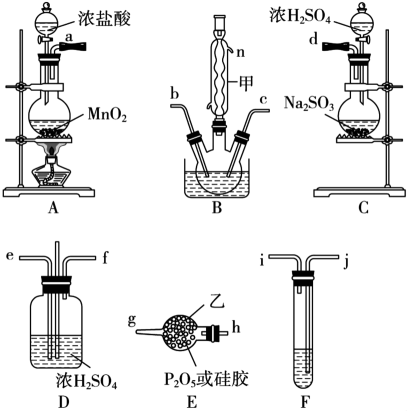
遇水强烈水解,易与氧气反应;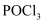 遇水强烈水解,能溶于
遇水强烈水解,能溶于 )。
)。
-
(1) 已知装置A制备
 , 装置C制备
, 装置C制备 , 装置B制备
, 装置B制备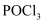 , 以上仪器接口连接的顺序为ah-d,装置B中发生反应的化学方程式为。
, 以上仪器接口连接的顺序为ah-d,装置B中发生反应的化学方程式为。
-
(2) 装置F中试剂的名称为,仪器甲的名称为。
-
(3) 此实验设计中有一不足之处是。
-
(4) 测定
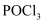 含量。准确称取12.0g
含量。准确称取12.0g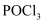 产品,置于盛有100
产品,置于盛有100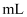 蒸馏水的水解瓶中摇动至完全水解,取10.0
蒸馏水的水解瓶中摇动至完全水解,取10.0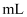 水解液于烧杯中,加入足量的硝酸酸化的
水解液于烧杯中,加入足量的硝酸酸化的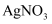 溶液,充分反应得到白色沉淀过滤、洗涤、烘干,称重为2.87g.产品中
溶液,充分反应得到白色沉淀过滤、洗涤、烘干,称重为2.87g.产品中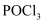 的百分含量为。(已知
的百分含量为。(已知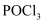 的相对分子质量为153.5)
的相对分子质量为153.5)
- What’s troubling them is ______ enoughexperienced workers.
- 阅读下面的文字,完成小题。(20分) 扣 子 [前苏联]卡沙耶夫 瓦西利•维克托罗维奇•切尔内舍夫正在办公,同时用小
- 氧气是化学性质比较活泼的气体,可以与许多物质发生反应。氧气的这一特性,使氧气在生产和生活中有着广泛的应用;也正是由于氧气
- 我国境内已知的最早人类是 A.元谋人 B.蓝田人 C.北京人 D.山顶洞人
- 为确定某溶液的离子组成,进行实验: ①测定溶液的pH值,溶液显碱性; ②取少量溶液加稀盐酸至溶液呈酸性,产生能使澄清石灰
- 1.依次填入下列各句横线处的成语,最恰当的一组是 ①作为城里人如果错误地认为农村远离城市,对农村污染视而不见,甚至把城市
- 小明在做“探究通过导体的电流与电阻的关系”的实验中,采用了图甲所示的电路图。(1)请按照电路图,用笔画线代替导线,将图乙
- 某租赁公司拥有汽车100辆,当每辆车的月租金为3 000元时,可全部租出,每辆车的月租金每增加50元,未租出的车会增加一
- 1﹣=
- 民族风俗习惯的基本特点是①相对稳定性 ②广泛群众性 ③民族性 ④很强敏感性A.①③④ B.①②
- 下列变化不属于化学变化的是( ) A.SO2使品红溶液褪色 B.氯水使有
- 明清时期影响资本主义萌芽的因素主要有: ( ) ①重农抑商政策 ②海禁和闭关锁国政策 ③长期形成的自给自足的自然经
- 已知a=(λ+1,0,2λ),b=(6,2μ-1,2),若a∥b,则λ与μ的值分别为…( )A.
- 假设2014年某国流通中所需要的货币量为40万亿元,由于生产发展,2015年货币需求量增加了20%,但实际发行结果却使流
- 如图所示,透热的气缸内封有一定质量的理想气体,缸体质量M=200kg,活塞质量m=10kg,活塞面积S=100cm2。活
- 某种芳香族化合物A,其蒸气密度是相同条件下H2密度的82倍。A由碳、氢、氧三种元素组成,经测定碳、氢的质量分数分别为73
- 党和政府在少数民族聚居地区实行的一项基本政策是( ) A.民主改革 B.土地改革 C.改革开放
- 周恩来说:“我们新民主主义的制度是一个过渡的制度……走完了这个过渡阶段,就到达了社会主义社会。”后来的实践表明,这个过渡
- 右图是某兴趣小组设计的一套实验装置,装置足以维持实验过程中小白鼠的生命活动。装置气密性良好。经数小时后,U形管A、B两处
- (2019·门头沟区一模)阅读下面的文字,完成问题。 中国崛起离不开文化支撑 ①改革开放40年来,中国有了巨大发展,中华


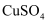 溶液
溶液


