第二节 离子反应 知识点题库
选项 | 实验操作 | 反应先后顺序 |
A | 含Fe3+、Cu2+、H+的溶液中加入锌粉 | Cu 2+、Fe3+、H+ |
B | 含I﹣、S2﹣、Br﹣的溶液中不断通入氯气 | S2﹣、I﹣、Br﹣ |
C | 含Cl﹣、Br﹣、I﹣的溶液中逐滴加入AgNO3溶液 | Cl﹣、Br﹣、I﹣ |
D | 含Al 3+、H+、NH4+的溶液中逐滴加入NaOH溶液 | H+、NH4+、Al 3+ |
选项 | 离子方程式 | 评价 |
A | 将2mol Cl2通入到含1mol FeI2的溶液中:2Fe2++2I−+2Cl2=2Fe3++4Cl−+I2 | 正确:Cl2过量,可将Fe2+、I−均氧化 |
B | Ba(HCO3)2溶液与足量的NaOH溶液反应:Ba2++HCO-+OH−=BaCO3↓+H2O | 正确:酸式盐与碱反应生成正盐和水 |
C | 过量SO2通入到NaClO溶液中:SO2+H2O+ClO−=HClO+HSO3- | 正确:说明酸性: H2SO3强于HClO |
D | 1mol/L的NaAlO2溶液和2.5mol/L的HCl 溶液等体积互相均匀混合: 2AlO-+5H+=Al3++Al(OH)3↓+H2O | 正确:AlO-与 H+均无剩余 |
-
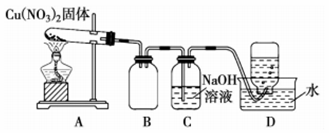
(1) 装置A发生反应中氧化产物与还原产物的体积比是(相同条件下)。
-
(2) 装置B的作用是,反应一段时间后,将带火星的木条放入B中,木条复燃,说明该红棕色气体可助燃,原因是。
-
(3) 已知NO2和NaOH溶液反应可生成两种钠盐,装置C中发生的离子方程式为。
-
(4) 将反应后试管中的固体加水充分溶解、过滤、洗涤,向滤渣中加入一定量稀硫酸,发现固体全部溶解,得到蓝色溶液,分为两份。
①一份溶液经、、、洗涤得蓝色晶体。
②另一份取20mL溶液,加入过量KI,充分反应后,用0.5000mol·L-1的Na2S2O3溶液来滴定反应产物,终点时消耗Na2S2O3溶液40.00mL,则上述溶液中c(Cu2+)= mol·L-1。(已知2Cu2++4I-=2CuI↓+I2;I2+2S2O32-=21-+S4O62-)
| 选项 | 离子组 | 加入试剂 | 加入试剂后发生的离子方程式 |
| A | Fe2+、NO3-、NH4+ | NaHSO4溶液 | 3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O |
| B | Ca2+、HCO3-、Cl- | 少量NaOH溶液 | Ca2++2HCO3-+2OH-═2H2O+CaCO3↓+CO32- |
| C | AlO2-、HCO3- | 通入少量CO2 | 2AlO2-+3H2O+CO2═2Al(OH)3↓+CO32- |
| D | NH4+、Al3+、SO42- | 少量Ba(OH)2溶液 | 2NH4++SO42-+Ba2++2OH═BaSO4↓+2NH3•H2O |
 2H++SO32-
C . CO32-的水解方程式:CO32-+H2O
2H++SO32-
C . CO32-的水解方程式:CO32-+H2O  HCO3-+OH-
D . CaCO3沉淀溶解平衡方程式:CaCO3(s)=Ca2+(aq)+CO32-(aq)
HCO3-+OH-
D . CaCO3沉淀溶解平衡方程式:CaCO3(s)=Ca2+(aq)+CO32-(aq)
-
(1) 写出碳酸氢铵的电离方程式:
-
(2) 钠与水反应的离子方程式
-
(3) 向碳酸钠溶液中逐滴加入稀盐酸至过量,写出反应过程的离子方程式,
-
(4) 标准状况下,CO与CO2的混合气体相对于O2的密度为1,则混合气体中CO与CO2的物质的量之比为。
-
(1) Ⅰ.①H2+CuO
 Cu+H2O
Cu+H2O ②CaCO3+2HCl=CaCl2+CO2↑+H2O
③3S+6NaOH
 2Na2S+Na2SO3+3H2O
2Na2S+Na2SO3+3H2O ④NH4NO3+Zn=ZnO+N2↑+2H2O
⑤Cu2O+4HCl=2HCuCl2+H2O
上述反应中,属于氧化还原反应的是(填序号)。
-
(2) 配平下面氧化还原反应的化学方程式:KMnO4+SO2+H2O—K2SO4+MnSO4+H2SO4 。
-
(3) Ⅱ.某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+中的几种离子。
不做任何实验就可以肯定原溶液中不存在的离子是。
-
(4) 取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,原溶液中肯定有的离子是。
-
(5) 取(4)的滤液加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子有,离子反应方程式为。
-
(6) 原溶液中可能大量存在的阴离子是下列的________(填序号)。A . Cl- B .
 C .
C .  D . OH-
D . OH-
 =3Fe3++2H2O+NO↑
B . 向碳酸钠溶液中加入少量氢氧化钡固体:CO
=3Fe3++2H2O+NO↑
B . 向碳酸钠溶液中加入少量氢氧化钡固体:CO  +Ba(OH)2=BaCO3↓+2OH-
C . 氧化铝与氢氧化钠溶液反应:Al2O3+2OH-=2AlO
+Ba(OH)2=BaCO3↓+2OH-
C . 氧化铝与氢氧化钠溶液反应:Al2O3+2OH-=2AlO  +H2O
D . 氯气与澄清石灰水反应:Cl2+2OH-=ClO-+Cl-+H2O
+H2O
D . 氯气与澄清石灰水反应:Cl2+2OH-=ClO-+Cl-+H2O
 =BaSO4↓
B . 金属钾与水反应:K+H2O=K++OH-+H2↑
C . 用FeCl3溶液腐蚀铜箔制造印刷电路板:Fe3++Cu=Fe2++Cu2+
D . 铜与稀硝酸和硫酸的混合酸制硫酸铜:3Cu+8H++2
=BaSO4↓
B . 金属钾与水反应:K+H2O=K++OH-+H2↑
C . 用FeCl3溶液腐蚀铜箔制造印刷电路板:Fe3++Cu=Fe2++Cu2+
D . 铜与稀硝酸和硫酸的混合酸制硫酸铜:3Cu+8H++2  =3Cu2++2NO↑+4H2O
=3Cu2++2NO↑+4H2O
-
(1) 电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式。
-
(2) 公元8世纪左右,我国炼丹士开始将硫酸亚铁加热到500℃左右,生成氧化铁和硫的氧化物,反应的化学方程式是。此法是最早生产硫酸的关键反应,当时若有m kg硫酸亚铁可生成kg50%的硫酸(填写计算表达式)。
-
(3) 高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。高铁酸钠生产方法之一是电解法,其原理为aFe+bNaOH+cH2O
 dNa2FeO4+eH2;该反应中若a=1,则e=。
dNa2FeO4+eH2;该反应中若a=1,则e=。
-
(4) 湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。
、Cl-、H2O。①在碱性条件下,湿法生产高铁酸钾的离子反应方程式是。
②若反应过程中转移了0.3 mol电子,则还原产物的物质的量为mol。
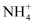 、Ca2+、Cl-、
、Ca2+、Cl-、 B . 能使酚酞变红的溶液中:Na+、Ba2+、Cl-、
B . 能使酚酞变红的溶液中:Na+、Ba2+、Cl-、 C . 与铁反应产生无色无气味气体的溶液中:Na+、K+、Cl-、
C . 与铁反应产生无色无气味气体的溶液中:Na+、K+、Cl-、 D . 常温下pH=1的溶液中:K+、Na+、
D . 常温下pH=1的溶液中:K+、Na+、 、OH-
、OH-
-
(1) 工业上以碳酸锂为原料制备
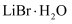 晶体的流程如下:
晶体的流程如下:
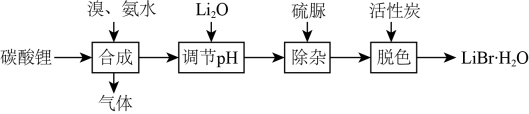
①合成LiBr时生成了两种参与大气循环的气体,反应的化学方程式为。
②加还原剂硫脲
 除去可能含有的
除去可能含有的 ,
, 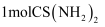 共有molσ键。
共有molσ键。③溴化锂的溶解度随温度的变化曲线如图所示。则从脱色、过滤所得溶液中提取
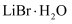 晶体的操作有:在HBr氛围下蒸发浓缩、,,洗涤后烘干。
晶体的操作有:在HBr氛围下蒸发浓缩、,,洗涤后烘干。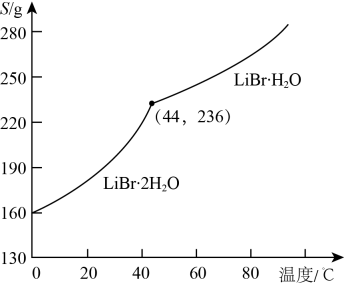
-
(2) 某学生兴趣小组在实验室用碘单质制备较纯的NaI晶体,部分装置如图所示。
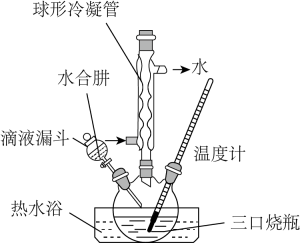
药品:
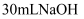 溶液(含8.2gNaOH)、25.4g碘、水合肼(还原剂,产物为N2)、1.0g活性炭和蒸馏水等。
溶液(含8.2gNaOH)、25.4g碘、水合肼(还原剂,产物为N2)、1.0g活性炭和蒸馏水等。实验步骤:向三口烧瓶中加入30mLNaOH溶液,边搅拌边加入25.4g单质碘。连接好装置并通入冷凝水,过滤后将滤液蒸发浓缩、结晶、过滤、干燥得产品24.3g。
回答问题:①碘溶于NaOH溶液生成NaI和
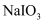 的离子方程式为。
的离子方程式为。②设计合理方案,补充完整上述实验步骤:。
- There was an _________ expression on her facewhen she came i
- PM2.5是指大气中直径小于或等于2.5微米的颗粒物,它们少部分是自然形成,绝大部分是人类行为造成的二次污染。随着经济快
- 下图中(一)、(二)、(三)是“我国部分灾害分布”示意图,(四)是“我国自然灾害区划”示意图。读图判断回答:(10分)(
- 下图为西藏怒江流域1971~2007年年降水量和年平均气温的变化趋势图(细线为历年值,点线为多年平均值,粗线为变化趋势值
- 下列各组物质的分离提纯方法正确的是A.Fe(OH)3沉淀与NaCl的混合物用渗析法分离B.除去Br2水中的KBr,用过滤
- 阅读下列材料: 材料一:(蒙古王公贵族进入中原以后)占民田千顷,不耕不稼,谓之草场,专放孽畜。 ——《续文献通考》
- 两个完全相同的长方体的长、宽、高分别为5cm,4cm,3cm,把它们重叠在一起组成一个新长方体,在这些新长方体中,最长的
- He wrote a lot of novels, none of _________ was translated i
- 家兔的一个初级精母细胞在减数分裂中,形成22个四分体,则精子中染色体数为()A.11条B.22条C.33条D.44条
- 如图是高温下某反应的微观示意图.图中的两种化合物都属于;该反应前后化合价没有发生变化的元素为;反应的化学方程式为 .
- (浙江卷理)(2).已知是实数,则“且”是“且”的 ( )A.充分而不必要条件
- 异面直线与上的单位向量分别为,, 且, 则两异面直线与所成角的大小为________.
- 下列句子翻译正确的一项是( ) ①君尝为晋君赐矣,许君焦、瑕,朝济而夕设版焉,君之所知也。 ②既东封郑,又欲肆其西
- 点燃 小明从化学方程式4P+5O2 ===== 2P2O5中总结的信息有:①参加反应的物质是磷和氧气 ②反应条件是点燃
- ......
- 在全国第六次人口普查时,某位市民给国家统计局局长发了一封电子邮件,从被调查者的角度谈了他对配合入户登记的感受及工作建议。
- 江苏省常州市横山桥高级中学10-11学年高二上学期期中考试(英语 I thought that Hannah must
- 2,5-溴尿嘧啶(Bu)是胸腺嘧啶(T)的结构类似物。在含有Bu的培养基中培养大肠杆菌,得到少数突变体大肠杆菌,突变型大
- 某气体完全燃烧,产物中有二氧化碳,则该气体组成元素中( ) A. 一定含有碳和氢
- 词汇应用;阅读下面的短文,用括号内所给词的适当形式填空,必要时可加助动词。 During the Second Worl



