第二节 离子反应 知识点题库
下列说法中,正确的是( )
A .  C和
C和  C原子的中子数相等
B . 纯水在20℃比在90℃时的pH值小
C . 正常雨水pH等于7,酸雨的pH小于7
D . 次氯酸是一种强氧化剂,是一种弱酸
C原子的中子数相等
B . 纯水在20℃比在90℃时的pH值小
C . 正常雨水pH等于7,酸雨的pH小于7
D . 次氯酸是一种强氧化剂,是一种弱酸
 C和
C和  C原子的中子数相等
B . 纯水在20℃比在90℃时的pH值小
C . 正常雨水pH等于7,酸雨的pH小于7
D . 次氯酸是一种强氧化剂,是一种弱酸
C原子的中子数相等
B . 纯水在20℃比在90℃时的pH值小
C . 正常雨水pH等于7,酸雨的pH小于7
D . 次氯酸是一种强氧化剂,是一种弱酸
下列实验室制取气体的反应中,属于非离子反应,且生成的气体为非电解质的是( )
A . 实验室制取氯气
B . 实验室制取氧气
C . 实验室制取二氧化碳
D . 实验室制取氨气
下列叙述正确的是( )
A . 某溶液中加入硝酸银溶液时,生成白色沉淀,说明溶液中有Cl﹣
B . 某溶液中加入稀硫酸溶液时,生成无色气体,说明溶液中有CO32﹣
C . 某溶液中加入氯化钡溶液时,生成白色沉淀,说明溶液中有SO42﹣
D . 某溶液中加入盐酸溶液,无明显现象,再加入氯化钡溶液时,生成白色沉淀,说明溶液中有SO42﹣
常温下,在下列给定条件的溶液中,一定能大量共存的离子组是( )
A . c(OH-)=1×10-13mol·L-1的溶液中:K+、Mg2+、Cl-、NO3-
B . 0.1mol/L的NaNO3溶液中:H+、Fe2+、Cl-、SO42-
C . 含有大量Al3+的水溶液中:Na+、NH4+、HCO3-、Br-
D . 水电离产生的c(H+)为1×10-l2mol·L-1的溶液:NH4+、Na+、Cl-、CO32-
在下列条件下,一定能大量共存的离子组是( )
A . 无色透明的水溶液中,K+ , Mg2+ , I- , MnO4-
B . 滴入酚酞显红色的水溶液中,NH4+ , Fe2+ , SO42- , Cl-
C . c(HCO3-)=0.1mol/L的溶液中,Na+ , K+ , CO32- , Br-
D . 使红色石蕊试纸变蓝的溶液中,H+ , Al3+ , Cl- , NO3-
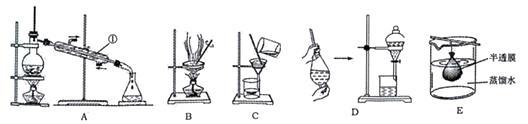
混合物分离和提纯常用下图装置进行,按要求回答下列问题:
-
(1) 仪器1的名称。
-
(2) 除去澄清石灰水中悬浮的CaCO3颗粒应选用(填字母,下同)。
-
(3) 分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物应选用。
-
(4) 明胶是水溶性蛋白质混合物,溶于水形成胶体。分离明胶的水溶液与Na2SO4溶液应选用,设计实验证明SO42-已分离出来。
-
(5) 有一混合物的水溶液,只可能含有以下离子中的若干种;K+、NH4+、Cl-、Ba2+、CO32-、SO42- , 现取三份100mL溶液进行如下实验:①第一份加入AgNO3溶液有沉淀产生;②第二份加足量NaOH溶液加热后,收集到气体0.04mol;③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。请根据上述实验结果,原溶液中肯定有离子,肯定无离子,可能有离子。
已知锌及其化合物的性质与铝及其化合物相似。如图横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4 ]2-的物质的量浓度的对数。25℃时,下列说法中错误的是( )
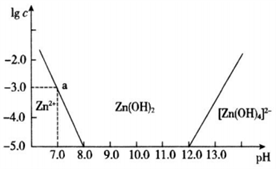
A . 往ZnCl2溶液中加入过量氢氧化钠溶液,反应的离子方程式为Zn2++4OH-=[Zn(OH)4]2-
B . 若要从某废液中完全沉淀Zn2+ , 通常可以调控该溶液的pH在8.0—12.0之间
C . pH=8.0与pH=12.0的两种废液中,Zn2+浓度之比为108
D . 该温度时,Zn(OH)2的溶度积常数(Ksp)为1×10-10
根据所学的知识填空。
-
(1) 实验室用锌粒与稀硫酸反应制取H2 , 要加快产生H2的速率,可采用的方法是(任写一种)。
-
(2) FeCl2溶液滴入KSCN溶液,出现红色,向变色的溶液中加入铁粉,溶液颜色变浅,直至褪色。原因是Fe3+被铁粉还原生成了Fe2+ , 写出该反应的离子方程式: 。
-
(3) 洁厕灵(主要成分是盐酸)与84消毒液(主要成分是次氯酸钠)是家庭生活中常备的两种清洁剂,但两种液体不能混合使用,两者混合会产生有毒气体Cl2 , 其发生的化学反应方程式为2HCl+NaClO=NaCl+Cl2↑+H2O。当有1mol的HCl参加反应时生成的氯气在标准状况下的体积为L。
某强碱性溶液中含有的离子是K+、NH4+、Al3+、AlO2-、CO32-、SiO32-、Cl-中的某几种,现进行如下实验:
①取少量的溶液用硝酸酸化后,该溶液无沉淀生成;
②另取一定量原溶液,逐滴加入盐酸至过量,发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失;
③另取一定量的原溶液中加入5mL0.2mol/L盐酸时,沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.187g。
下列说法中正确的是( )
A . 该溶液中一定不含NH4+、Al3+、SiO32-、Cl-
B . 该溶液中一定含有Al3+、CO32-、Cl-
C . Cl-可能含有
D . 该溶液中一定含有AlO2-、CO32-、Cl-
下列离子方程式正确的是( )
A . 过量氯气通入碘化亚铁溶液中:Cl2+Fe2++2I-=2Cl-+Fe3+ +I2
B . 向NaHCO3溶液中加入少量澄清石灰水:HCO3-+Ca2++OH-=CaCO3↓+H2O
C . H218O中投入少量Na2O2固体:2H218O+2Na2O2=4Na++4OH-+18O2↑
D . 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀:Ba2++OH-+SO42-+H+=BaSO4↓+H2O
下列各组离子,在指定的环境中一定能大量共存的是( )
A . 某无色透明溶液中:NH4+、Ca2+、Cl-、CO32-
B . 与金属铝反应放出氢气的溶液:K+、NH4+、NO3-、Cl-
C . 滴加酚酞试液显红色的溶液:K+、Na+、CO32-、Cl-
D . c(Fe2+)=1mol/L的溶液:K+、NH4+、MnO4-、SO42-
下列指定反应的离子方程式正确的是( )
A . 氢氧化镁与盐酸反应:  B . 将铝片打磨后立即放入氢氧化钠溶液中:
B . 将铝片打磨后立即放入氢氧化钠溶液中: 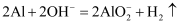 C .
C .  溶液中加入足量稀
溶液中加入足量稀 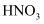 (必要时可加热):
(必要时可加热): 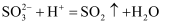 D . 硫酸氢铵溶液中滴加少量
D . 硫酸氢铵溶液中滴加少量 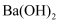 溶液:
溶液: 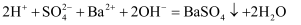
 B . 将铝片打磨后立即放入氢氧化钠溶液中:
B . 将铝片打磨后立即放入氢氧化钠溶液中: 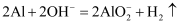 C .
C .  溶液中加入足量稀
溶液中加入足量稀 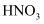 (必要时可加热):
(必要时可加热): 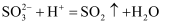 D . 硫酸氢铵溶液中滴加少量
D . 硫酸氢铵溶液中滴加少量 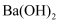 溶液:
溶液: 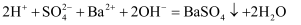
下列有关物质分类的说法中,正确的是( )
A . SiO2不能和水反应,所以它不是酸性氧化物
B . 只由一种元素组成的物质必然是纯净物
C . 烧碱、冰醋酸、石墨均为电解质
D . 海水、氯水、氨水均为混合物
下列各组两种物质在溶液中的反应, 可用同一离子方程式表示的是( )
A . Cu(OH)2和盐酸;Cu(OH)2 和CH3COOH
B . BaCl2 和Na2SO4;Ba(OH)2 和CuSO4
C . NaHCO3和NaHSO4;Na2CO3 和NaHSO4
D . 石灰石与硝酸;碳酸钙与盐酸
为纪念元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。下图是扇形元素周期表的一部分,针对元素①~⑩按要求作答。
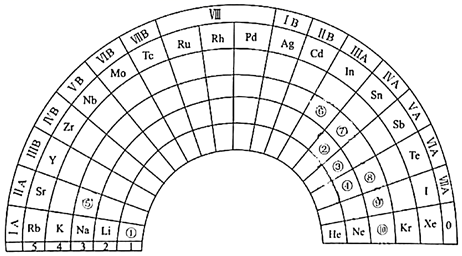
-
(1) ⑩的原子结构示意图为。
-
(2) ①和②组成的最简单化合物的电子式为。
-
(3) ④和⑤的简单离子半径较大的是(填序号)。
-
(4) ③的简单氢化物与其最高价氧化物对应水化物反应得到的盐的化学式为。
-
(5) 某元素原子的M层电子数为K层电子数的两倍,则该元素是(填序号)。
-
(6) 把⑥投入烧碱溶液中发生反应的化学方程式为。
-
(7) 写出一个能证明⑧的非金属性小于⑨的离子方程式。
下列关于物质分类正确的是( )
A . 混合物:水煤气、冰醋酸、冰水混合物
B . 电解质:氯化氢、硫酸钡、水
C . 正盐:小苏打、纯碱、氯化钠
D . 碱性氧化物:氧化钙、四氧化三铁、过氧化钠
高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中湿法制备高铁酸钠的原理为:
3NaClO + 2Fe(OH)3 +4NaOH = 2Na2FeO4 +3NaCl+5H2O
-
(1) 高铁酸根(
 )中铁元素的化合价为;该反应中氧化剂是;被氧化的元素是(填名称);氧化产物是;
)中铁元素的化合价为;该反应中氧化剂是;被氧化的元素是(填名称);氧化产物是;
-
(2) 请用双线桥表示该氧化还原反应中电子转移的方向和数目:;
-
(3) 写出NaOH的电离方程式:;
-
(4) 写出湿法制备高铁酸钠的离子方程式:;
某无色透明溶液中可能大量存在离子为 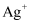 、
、  、
、 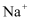 、
、  、
、  、
、  、
、 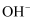 、
、  中的几种,回答下列回答(用离子符号填空):
中的几种,回答下列回答(用离子符号填空):
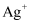 、
、  、
、 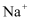 、
、  、
、  、
、  、
、 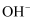 、
、  中的几种,回答下列回答(用离子符号填空):
中的几种,回答下列回答(用离子符号填空):
-
(1) 不做任何实验就可以确定原溶液中不存在的离子是。
-
(2) 取少量溶液,加入过量盐酸,有白色沉淀生成;再加入过量稀硝酸,沉淀不消失。根据此现象你得出的结论是。
-
(3) 取(2)中的滤液,加入过量稀氨水,出现白色沉淀,说明原溶液中肯定存在的离子是。生成白色沉淀的离子方程式是。
-
(4) 原溶液中一定含有的离子有;可能存在的离子有。
下列微粒在溶液中能大量共存的是( )
A .  、
、 、
、 、
、 B .
B .  、
、 、
、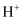 、
、 C .
C .  、
、 、
、 、
、 D .
D . 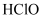 、
、 、
、 、
、
 、
、 、
、 、
、 B .
B .  、
、 、
、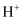 、
、 C .
C .  、
、 、
、 、
、 D .
D . 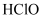 、
、 、
、 、
、
下列物质,既属于电解质,又能导电的是( )
A . 熔融NaCl
B . H2SO4
C . 蔗糖
D . NaOH溶液
最近更新
- 已知等比数列{an}的公比q=﹣,则等于() A. ﹣ B
- The great _____ of this computer is that it’s so cheap compa
- (本小题 7 分)计算:
- 甲生物核酸的碱基组成为:嘌呤占46%,嘧啶占54%,乙生物遗传物质的组成为:嘌呤占34%,嘧啶占66%,则甲、乙生物可能
- Advertising is a highly developed twentieth-century industry
- 若正比例函数的图象经过点(-1,2),则其解析式为 ;
- (16届湖北省利川市文斗乡长顺初级中学九年级上学期第一次月考)阅读下面诗歌,完成后面题目 错误 郑愁予 我打江南走过
- “观察DNA、RNA在细胞中分布”的实验中,正确的实验步骤是 ( ) A.水解→制片→冲洗→染色→观察 B.制片→
- 下列关于制备牛肉膏蛋白胨固体培养基,叙述错误的是( ) A.操作顺序为计算、称量、溶化、倒平板、灭菌
- ―What are you going to do this afternoon? ―I am going to
- 请选用C、H、O、Ca四种元素中的一种或几种元素写出符合下列要求的化学式:(1)可作建筑材料的盐__________;
- 2012年6月,国务院批准设立海南省三沙市,下辖西沙群岛、南沙群岛、中沙群岛的岛礁及其海域。读南沙群岛部分珊瑚岛礁分布图
- 已知四个实数成等差数列,-4,b1,b2,b3,-1五个实数成等比数列,则=
- 如图所示,小车A上放一木块B,在下列情况下,A、B均相对静止,试分析A对B的摩擦力.(1)小车A在水平面上匀速运动.(2
- 陈旭麓在《近代中国的新陈代谢》指出:“这场战争,自西方人1514年到中国起,是他们积325年窥探之后的一逞。对于中国人来
- I alwayswanted to fly a plane, but back to 1930s, it was alm
- 下列关于生命起源和生物进化的叙述中,错误的是( )A.原始大气成分与现代大气相同 B.原始生命在原始海洋中经漫长
- 在正常情况下,下列有关X染色体的叙述错误的是 A.女性体细胞内有两条X染色体 B.男性体细胞内有一条X染
- 三氯化磷分子的空间构型是三角锥形而不是平面正三角形,下列关于三氯化磷分子空间构型理由的叙述,不正确的是
- 小张在2013年将30万资金全部用于投资股票,年底赚了10万,而2014年同样的投资却亏了16万。小王在这两年内将30万



