第二章 化学物质及其变化 知识点题库
某溶液仅含  、
、  、
、  、
、  、
、  、
、  、
、  中的4种离子,所含离子的物质的量均为
中的4种离子,所含离子的物质的量均为 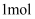 。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。下列说法错误的是( )
。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。下列说法错误的是( )
 、
、  、
、  、
、  、
、  、
、  、
、  中的4种离子,所含离子的物质的量均为
中的4种离子,所含离子的物质的量均为 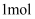 。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。下列说法错误的是( )
。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。下列说法错误的是( )
A . 该溶液中所含的离子是:  、
、  、
、  、
、  B . 若向该溶液中加入过量的稀硫酸和
B . 若向该溶液中加入过量的稀硫酸和  溶液,溶液显血红色
C . 若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色
D . 若向该溶液中加入足量的
溶液,溶液显血红色
C . 若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色
D . 若向该溶液中加入足量的  溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为
溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为 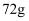
 、
、  、
、  、
、  B . 若向该溶液中加入过量的稀硫酸和
B . 若向该溶液中加入过量的稀硫酸和  溶液,溶液显血红色
C . 若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色
D . 若向该溶液中加入足量的
溶液,溶液显血红色
C . 若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色
D . 若向该溶液中加入足量的  溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为
溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为 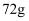
根据物质的组成与性质进行分类,NaOH属于( )
A . 氧化物
B . 酸
C . 碱
D . 盐
下列各组离子一定能大量共存的是:( )
A . 含有大量Ba2+的溶液中:Cl-、K+、SO  、CO
、CO  B . 含有大量H+的溶液中:Mg2+、Na+、HCO
B . 含有大量H+的溶液中:Mg2+、Na+、HCO  、SO
、SO  C . 含有大量OH—的溶液中:NH
C . 含有大量OH—的溶液中:NH  、NO
、NO  、SO
、SO  、CO
、CO  D . 含有大量Na+的溶液中:H+、K+、SO
D . 含有大量Na+的溶液中:H+、K+、SO  、NO
、NO 
 、CO
、CO  B . 含有大量H+的溶液中:Mg2+、Na+、HCO
B . 含有大量H+的溶液中:Mg2+、Na+、HCO  、SO
、SO  C . 含有大量OH—的溶液中:NH
C . 含有大量OH—的溶液中:NH  、NO
、NO  、SO
、SO  、CO
、CO  D . 含有大量Na+的溶液中:H+、K+、SO
D . 含有大量Na+的溶液中:H+、K+、SO  、NO
、NO 
NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 5.6 g铁粉与硝酸反应失去的电子数一定为0.3NA
B . 1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA
C . 向FeI2溶液中通入适量Cl2 , 当有1 mol Fe2+被氧化时,共转移的电子的数目为NA
D . 1 mol Cl2参加反应转移电子数一定为2NA
下列物质的水溶液因电离而呈酸性的是( )
A . CaCl2
B . NaHSO4
C . CH3COONa
D . NH4Cl
下列说法错误的是( )
A . 煤中含有苯、甲苯、二甲苯等化合物,这些物质可以通过煤的干馏,从煤焦油中蒸馏而得
B . 石油催化裂化是为提高轻质油的产量与质量
C . 沼气的主要成分是甲烷,是一种生物质能
D . Fe(OH)3胶体能凝聚水中的悬浮物并使之沉降,因而常用于净水
下表是元素周期表的一部分,针对所给的8种元素,完成下列各小题。
|
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
|
1 |
① |
|||||||
|
2 |
② |
③ |
④ |
|||||
|
3 |
⑤ |
⑥ |
⑦ |
⑧ |
||||
-
(1) 单质化学性质最不活泼的是 (填化学式),最高价氧化物对应的水化物酸性最强的是 (填化学式)。
-
(2) ⑥的原子结构示意图为 。
-
(3) ③⑤的简单离子半径由大到小的顺序为 (填离子符号)。
-
(4) 如图所示模型表示的分子中,不可能由①和②形成的是 (填标号)。
a.
 b.
b.  c.
c.  d.
d. 
-
(5) ⑤单质在足量的③单质中充分燃烧的产物的电子式为 。
-
(6) ⑤的最高价氧化物对应水化物与⑦的氧化物之间发生反应的离子方程式为 。
-
(7) 可用来比较⑥⑦两种元素金属性强弱的是 (填标号)。
a.比较两种元素形成单质的熔、沸点
b.比较两种元素的单质与水反应的难易程度
c.比较两种元素的单质与Cl2反应时转移电子数的多少
d.向两种元素的最高价氧化物对应的水化物中滴加NaOH溶液至过量
某学生以铁丝和  原料进行如图所示三个实验。从分类的角度来分析,下列说法正确的是( )
原料进行如图所示三个实验。从分类的角度来分析,下列说法正确的是( )
 原料进行如图所示三个实验。从分类的角度来分析,下列说法正确的是( )
原料进行如图所示三个实验。从分类的角度来分析,下列说法正确的是( ) 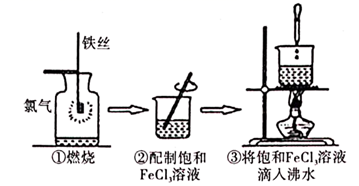
A . 实验①、③制得的物质均为纯净物
B . 实验②、③均未发生氧化还原反应
C . 实验①、②、③均发生了放热反应
D . 实验①、②所涉及的物质均为电解质
下列离子方程式正确的是( )
A . 碳酸钙中加盐酸:CO  +2H+=CO2↑+H2O
B . 稀硫酸中加氢氧化钡溶液:SO
+2H+=CO2↑+H2O
B . 稀硫酸中加氢氧化钡溶液:SO  +H++Ba2++OH-=H2O+BaSO4↓
C . 制作印刷电路板的原理是:2Fe3++Cu=2Fe2++Cu2+
D . 二氧化锰和浓盐酸制氯气:MnO2 + 4H++4Cl-
+H++Ba2++OH-=H2O+BaSO4↓
C . 制作印刷电路板的原理是:2Fe3++Cu=2Fe2++Cu2+
D . 二氧化锰和浓盐酸制氯气:MnO2 + 4H++4Cl- 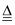 Mn2+ + Cl2↑+ 2H2O
Mn2+ + Cl2↑+ 2H2O
 +2H+=CO2↑+H2O
B . 稀硫酸中加氢氧化钡溶液:SO
+2H+=CO2↑+H2O
B . 稀硫酸中加氢氧化钡溶液:SO  +H++Ba2++OH-=H2O+BaSO4↓
C . 制作印刷电路板的原理是:2Fe3++Cu=2Fe2++Cu2+
D . 二氧化锰和浓盐酸制氯气:MnO2 + 4H++4Cl-
+H++Ba2++OH-=H2O+BaSO4↓
C . 制作印刷电路板的原理是:2Fe3++Cu=2Fe2++Cu2+
D . 二氧化锰和浓盐酸制氯气:MnO2 + 4H++4Cl- 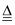 Mn2+ + Cl2↑+ 2H2O
Mn2+ + Cl2↑+ 2H2O
某小组用如图装置探究  的性质。下列离子方程式书写错误的是( )
的性质。下列离子方程式书写错误的是( )
 的性质。下列离子方程式书写错误的是( )
的性质。下列离子方程式书写错误的是( ) 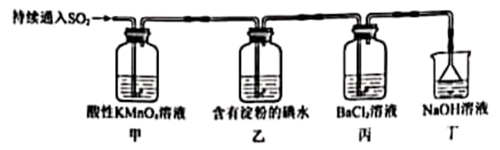
A . 甲中紫色褪去: 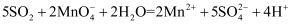 B . 乙中蓝色逐渐变浅:
B . 乙中蓝色逐渐变浅: 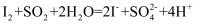 C . 丙中产生少量白色沉淀:
C . 丙中产生少量白色沉淀: 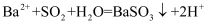 D . 丁中可能的反应:
D . 丁中可能的反应: 
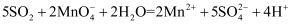 B . 乙中蓝色逐渐变浅:
B . 乙中蓝色逐渐变浅: 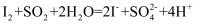 C . 丙中产生少量白色沉淀:
C . 丙中产生少量白色沉淀: 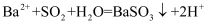 D . 丁中可能的反应:
D . 丁中可能的反应: 
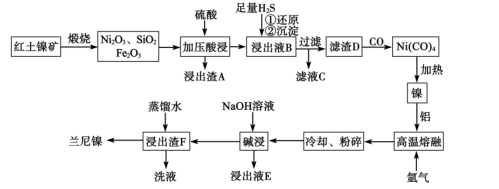
兰尼镍是一种带有多孔结构的细小晶粒组成的镍铝合金,具有优良的储氢性能。以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的工艺流程如图:
-
(1) 形成Ni(CO)4时碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为,Ni(CO)4含有的化学键类型。
-
(2) Ni2O3有强氧化性,加压酸浸时,有气体产生且镍被还原为Ni2+ , 则产生的气体为(填化学式)。
-
(3) 滤渣D为单质镍、硫的混合物,请写出向浸出液B中通入H2S气体生成单质镍的离子方程式:。
-
(4) “高温熔融”时通入氩气的目的是。
-
(5) 检验滤液C中金属阳离子的试剂是(填标号)。
a.KSCN溶液 b.K3[Fe(CN)6] c.酸性高锰酸钾 d.苯酚
-
(6) 碱浸的目的是使镍铝合金产生多孔结构,其原理(用化学方程式表示)。
下列对于某些离子的检验及结论正确的是( )
A . 加入稀盐酸产生气体,将气体通入澄清石灰水,溶液变浑浊,一定有CO32-
B . 加入稀盐酸无明显现象,再加氯化钡溶液,有白色沉淀产生,一定有SO42-
C . 加硝酸银溶液产生白色沆淀,一定有Cl-
D . 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
下列反应的离子方程式错误的是( )
A . 石灰水与Na2CO3溶液混合:Ca2++  = CaCO3↓
B . 实验室用石灰石和盐酸制取二氧化碳:CaCO3+2H+= Ca2++H2O+CO2↑
C . 硫酸铜与烧碱溶液混合:CuSO4+2OH-= Cu(OH)2↓+
= CaCO3↓
B . 实验室用石灰石和盐酸制取二氧化碳:CaCO3+2H+= Ca2++H2O+CO2↑
C . 硫酸铜与烧碱溶液混合:CuSO4+2OH-= Cu(OH)2↓+  D . 氯化钾溶液与硝酸银溶液混合:Ag++Cl-= AgCl↓
D . 氯化钾溶液与硝酸银溶液混合:Ag++Cl-= AgCl↓
 = CaCO3↓
B . 实验室用石灰石和盐酸制取二氧化碳:CaCO3+2H+= Ca2++H2O+CO2↑
C . 硫酸铜与烧碱溶液混合:CuSO4+2OH-= Cu(OH)2↓+
= CaCO3↓
B . 实验室用石灰石和盐酸制取二氧化碳:CaCO3+2H+= Ca2++H2O+CO2↑
C . 硫酸铜与烧碱溶液混合:CuSO4+2OH-= Cu(OH)2↓+  D . 氯化钾溶液与硝酸银溶液混合:Ag++Cl-= AgCl↓
D . 氯化钾溶液与硝酸银溶液混合:Ag++Cl-= AgCl↓
下列变化中,属于氧化还原反应且属于吸热反应的是( )
①液态水汽化②将胆矾加热变为白色粉末③浓H2SO4稀释④KClO3分解制O2⑤生石灰跟水反应生成熟石灰⑥CaCO3高温分解⑦ 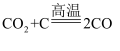 ⑧
⑧  与固体NH4Cl混合⑨
与固体NH4Cl混合⑨ 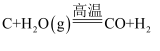 ⑩Al与盐酸反应
⑩Al与盐酸反应
A . ④⑦⑨
B . ④⑥⑦⑧⑨
C . ①④⑧⑨⑩
D . ①②④⑧⑨
常温下,下列各组离子在指定溶液中能大量共存的是( )
A . pH=1 的溶液中: HCO  、 K+、 Cl-、 Na+
B . 无色溶液中: NH
、 K+、 Cl-、 Na+
B . 无色溶液中: NH  、K+、MnO
、K+、MnO  、NO
、NO  C . 含有SO
C . 含有SO  的溶液中: NO
的溶液中: NO  、 OH-、Na+、 Ba2+
D . c(OH-) = 10-2 mol/L的溶液中: Na+、CO
、 OH-、Na+、 Ba2+
D . c(OH-) = 10-2 mol/L的溶液中: Na+、CO  、Cl-、K+
、Cl-、K+
 、 K+、 Cl-、 Na+
B . 无色溶液中: NH
、 K+、 Cl-、 Na+
B . 无色溶液中: NH  、K+、MnO
、K+、MnO  、NO
、NO  C . 含有SO
C . 含有SO  的溶液中: NO
的溶液中: NO  、 OH-、Na+、 Ba2+
D . c(OH-) = 10-2 mol/L的溶液中: Na+、CO
、 OH-、Na+、 Ba2+
D . c(OH-) = 10-2 mol/L的溶液中: Na+、CO  、Cl-、K+
、Cl-、K+
已知有如下反应∶ ①ClO +5Cl- +6H+=3Cl2↑+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2③2FeCl2+Cl2=2FeCl3。下列各微粒氧化能力由强到弱的顺序正确的是( )
+5Cl- +6H+=3Cl2↑+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2③2FeCl2+Cl2=2FeCl3。下列各微粒氧化能力由强到弱的顺序正确的是( )
 +5Cl- +6H+=3Cl2↑+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2③2FeCl2+Cl2=2FeCl3。下列各微粒氧化能力由强到弱的顺序正确的是( )
+5Cl- +6H+=3Cl2↑+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2③2FeCl2+Cl2=2FeCl3。下列各微粒氧化能力由强到弱的顺序正确的是( )
A . ClO >Cl2>Fe3+>I2
B . Cl2>ClO
>Cl2>Fe3+>I2
B . Cl2>ClO >I2>Fe3+
C . ClO
>I2>Fe3+
C . ClO >Cl2>I2>Fe3+
D . ClO
>Cl2>I2>Fe3+
D . ClO >Fe3+ >Cl2>I2
>Fe3+ >Cl2>I2
 >Cl2>Fe3+>I2
B . Cl2>ClO
>Cl2>Fe3+>I2
B . Cl2>ClO >I2>Fe3+
C . ClO
>I2>Fe3+
C . ClO >Cl2>I2>Fe3+
D . ClO
>Cl2>I2>Fe3+
D . ClO >Fe3+ >Cl2>I2
>Fe3+ >Cl2>I2
下列各组离子在指定溶液中一定能大量共存的是( )
A . 使紫色石蕊试液变红的溶液:Fe2+、Mg2+、SO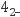 、Cl-
B . 澄清透明的溶液中:Na+、Fe3+、 SO
、Cl-
B . 澄清透明的溶液中:Na+、Fe3+、 SO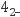 、I-
C . 在强酸性溶液中: Na+、 K+、ClO-、SO
、I-
C . 在强酸性溶液中: Na+、 K+、ClO-、SO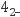 D . 使酚酞试液变红的溶液:Na+、Ca2+、Cl-、NO
D . 使酚酞试液变红的溶液:Na+、Ca2+、Cl-、NO
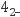 、Cl-
B . 澄清透明的溶液中:Na+、Fe3+、 SO
、Cl-
B . 澄清透明的溶液中:Na+、Fe3+、 SO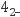 、I-
C . 在强酸性溶液中: Na+、 K+、ClO-、SO
、I-
C . 在强酸性溶液中: Na+、 K+、ClO-、SO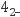 D . 使酚酞试液变红的溶液:Na+、Ca2+、Cl-、NO
D . 使酚酞试液变红的溶液:Na+、Ca2+、Cl-、NO
向等物质的量浓度的NaOH和Na2S的混合溶液中加入稀硫酸,下列离子方程式与事实不相符的是( )
A . OH-+S2-+2H+→HS-+H2O
B . 2OH-+ S2- +4H+→H2S↑+2H2O
C . 2OH-+ S2-+3H+→HS-+2H2O
D . OH-+ S2-+3H+→H2S↑+ H2O
近年来,我国大力弘扬中华优秀传统文化,体现了中华民族“文化自信”。下列说法错误的是( )
A . “春蚕到死丝方尽,蜡炬成灰泪始干”,诗中涉及氧化还原反应
B . “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
C . “粉身碎骨浑不怕,要留清白在人间”,该过程中只发生分解反应
D . 《荷塘月色》中“薄薄的青雾浮起在荷塘里”中的“青雾”属于胶体
科学家发现了利用泪液来检测糖尿病的方法,其原理是用氯金酸钠 (NaAuCl4)溶液与泪液中的葡萄糖发生反应,生成纳米金单质颗粒(直径为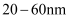 )。下列有关说法错误的是( )
)。下列有关说法错误的是( )
 )。下列有关说法错误的是( )
)。下列有关说法错误的是( )
A . 氯金酸钠中金元素的化合价为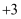 B . 检测时,葡萄糖发生了还原反应
C .
B . 检测时,葡萄糖发生了还原反应
C . 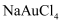 在反应中体现氧化性
D . 纳米金单质颗粒分散在水中所得的分散系属于胶体
在反应中体现氧化性
D . 纳米金单质颗粒分散在水中所得的分散系属于胶体
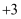 B . 检测时,葡萄糖发生了还原反应
C .
B . 检测时,葡萄糖发生了还原反应
C . 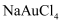 在反应中体现氧化性
D . 纳米金单质颗粒分散在水中所得的分散系属于胶体
在反应中体现氧化性
D . 纳米金单质颗粒分散在水中所得的分散系属于胶体
最近更新
- 关于温度、热量和内能,下列说法中正确的是:A.物体的温度越高,所含的热量越多B.温度高的物体,内能不一定大C.0OC的冰
- 下列变化属于物理变化的是( ) A.火箭发射 B.节日烟火 C.风力发电 D.葡萄酿酒
- Life isn't meant to beeasy and you have to _____ some pain t
- Everyone arrived on time thetraffic was so terribl
- 如图16-14所示,MN为裸金属杆,在重力的作用下,贴着竖直平面内的光滑金属长直导轨下滑,导轨的间距L=10 cm,导轨
- 在0,-1,2,-3这四个数中,绝对值最小的数是() A. 0 B. C. 2
- It seems that theaged people ________ the H7N9 more easily f
- 在某一温度下,连接在电路中的两段导体A和B中的电流与其两端电压的关系如图9所示。由图中信息可知()A.A导体的电阻为10
- 3.下列句子中,加点词语使用恰当的一项是( ) A.草原的清晨,别有情趣,你站在高岗,极目远眺,烟雾朦胧,茫茫无际
- 完形填空 Tom and Fred were talking about the year 2050. “What wi
- (a+2b)(a-2b)(a2+4b2).
- 下列各句中,加点的词语使用恰当的一项是( ) A.“中国怎么样,很大程度上决定了2015年世界会怎么样。
- 在平面直角坐标系xOy中,已知点A(6,0),点B(0,6),动点C在以半径为3的⊙O上,连接OC,过O点作OD⊥OC,
- Look out for cars _____ the street. A. when crossed B. when
- 当两极都用银片作电极电解硝酸银水溶液时,阳极的产物是( ) A.只有银 B.银和氧气
- 电能表上铝盘时慢时快,在使用一只普通灯泡时铝盘一般比使用电热水器转得______,说明铝盘转动的快慢跟用电器有关,其实跟
- 下列各句中加点的成语使用不恰当的一句是 ( ) A.我是自然界最伟大的奇迹,不可能象动物一样容易满足,我心中燃烧
- 在纸上剪一个很小的方形孔,让太阳光垂直照射在方形孔上,那么地面上形成的光斑是( )A.方形,是太阳的虚像
- 阅读下面的文字,按要求作文。 有人说:真正成功的人,本质上流着叛逆的血,摆脱一切限制。也有人说:一支笔,可以画,可以写,
- 某动物体中的甲细胞比乙细胞RNA的含量多,可能的原因是() A.甲合成的蛋白质种类和数量比乙多 B.甲中的遗传物质是RN



