第二节 溶液组成的定量表示 知识点题库
根据右图判断,下列说法错误的是: ()
A . NaCl和NH4Cl的溶解度都随温度升高而增大
B . 20℃时,20克NaCl加入到50克水中,充分搅拌后将部分溶解
C . t℃时,NH4Cl饱和溶液和NaCl饱和溶液溶质质量分数相等
D . 将20℃时某NH4Cl溶液降温到0℃,其溶质质量分数一定减小
在溶质质量分数为20%的KNO3溶液中加入3gKNO3和12g水完全溶解后,所得溶液中溶质的质量分数为 .
某环保小组监测到一工厂向河水中排放的酸性废液中含有CuSO4 , 为了测定废液中CuSO4的质量分数,该小组取了100g废液,逐滴加入NaOH溶液至过量,测得生成Cu(OH)2沉淀(无其它沉淀),其质量与所加NaOH溶液的质量关系如图所示:

-
(1) 图中的OA段未生成Cu(OH)2沉淀的原因:
-
(2) 计算废液中CuSO4的质量分数.(写出计算过程)
如表是KCl的部分溶解度数据,下列说法正确的是( )
温度(℃) | 0 | 20 | 40 | 60 |
溶解度(g) | 27.6 | 34 | 40 | 45.5 |
A . 20℃时,100g KCl饱和溶液中含KCl 34g
B . 任何温度下的KCl饱和溶液都不能再溶解其它物质
C . 40℃的KCl溶液的浓度一定大于20℃的KCl饱和溶液的浓度
D . 将60℃的KCl溶液降温至40℃时,不一定有晶体析出
氯化钠在20℃时溶解度为36g,该温度下,氯化钠溶液的溶质质量分数不可能是( )
A . 20%
B . 25%
C . 26.5%
D . 36%
水和溶液在生命活动和生产、生活中起着十分重要的作用.
-
(1) 如图为电解水的实验装置图,此实验说明水是由组成.

-
(2) 如表是NaOH和Ca(OH)2的溶解度数据,请回答下列问题.
温度(℃)
0
20
40
60
80
100
溶解度
(g)
NaOH
31
91
111
129
313
336
Ca(OH)2
0.19
0.17
0.14
0.12
0.09
0.08
①石灰水中的溶质是.
②把80℃时NaOH和Ca(OH)2的饱和溶液降温至20℃,析出的晶体是;现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后,恢复到原温得到的溶液(乙溶液),此时溶液的溶质质量分数甲 乙(填>、<、=),其原因是.
③在20℃时,向盛有100g水的烧杯中加入111gNaOH,欲使其完全溶解变成不饱和溶液.下列说法中正确的是.
A.溶液的质量可能不变 B.溶液中溶质的质量分数一定减小
C.溶液中溶质的质量一定增大D.可以升温到40℃以上.
根据问题填空:
-
(1) 为了预防佝偻病,幼儿及青少年每日必须摄入足够量的元素;
-
(2) 用来给病人输液的生理盐水是浓度为0.9%的氯化钠溶液,其配制方法为:取氯化钠加注射用水配成20%浓溶液→加活性炭搅匀→10℃以下静置→粗滤去炭→稀释至氯化钠浓度为0.9%→调节pH5.5~6.5→精滤→分装最后经热压灭菌即得.
①生理盐水呈性;(选填:“酸”、“碱”或“中”
②加活性炭是利用活性炭的性;
③若要生产一批次(200瓶)标签如图的生理盐水,需20%的浓氯化钠溶液g;

-
(3) 葡萄糖是生命活动中不可缺少的物质,它在人体内能直接参与新陈代谢过程,是机体所需能量的主要来源.葡萄糖在人体内参与新陈代谢的化学方程式为.
为测定某石灰石样品(杂质不溶于水,也不溶于稀盐酸)中碳酸钙的含量,取10g样品放入烧杯中,加入94.96g稀盐酸,恰好完全反应,经测定气体的质量为3.96g.试计算:
-
(1) 样品中碳酸钙的含量;
-
(2) 所得溶液的溶质质量分数.
向含CuCl2和HCl的100g混合溶液中,逐滴加溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图.据图回答:

-
(1) 在滴加NaOH溶液过程中,原溶液中离子个数不变.(填离子符号)
-
(2) P点溶液中的溶质是.
-
(3) m1的值为.
-
(4) M点溶液中的溶质质量分数是多少?
将100g、10%的蔗糖溶液中溶质的质量分数增大一倍,可采用的方法有( )
A . 蒸发掉50g水
B . 加入20g蔗糖
C . 加入10g蔗糖
D . 加入100g、20%的蔗糖溶液
将一定质量的金属锌投入到200g稀硫酸中恰好完全反应,放出气体的质量与反应时间的关系如图所示.

试求:
-
(1) 完全反应后产生H2的质量为 g;
-
(2) 所用硫酸溶液中溶质的质量分数为(写出计算过程).
往100 g含有盐酸和氯化钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图,试分析计算:

-
(1) a→b段表示碳酸钠与混合溶液中的反应。
-
(2) 请计算原混合溶液中 CaCl2的溶质质量分数(写出计算过程,精确到 0.1%)。
制作“叶脉书签”需要100g溶质质量分数为10%的氢氧化钠溶液。请问:
-
(1) 配制时需要氢氧化钠固体的质量是g,水的质量是g
-
(2) 若用20%的氢氧化钠溶液和水配制上述所需溶液,需要20%的氢氧化钠溶液质量是多少克?(规范写出计算过程)
为探究复分解反应发生的条件,实验小组的同学将20g硫酸钠和氯化钠的混合物加入到103.3g氯化钡溶液中,完全反应后,过滤,所得滤液质量为100g。请计算:
-
(1) 反应后生成沉淀的质量为g。
-
(2) 原混合物中氯化钠的质量分数。
草木灰是一种常见的农家肥。为测定某草木灰中碳酸钾的质量分数,化学兴趣小组同学称取100.0g该草木灰样品放入烧杯中,加足量的水充分溶解后过滤,取滤液
59.0g于烧杯中,向其中逐滴加入氯化钙溶液,产生沉淀的质量与所加入氯化钙溶液的质量的关系如图所示(假定滤液中只有碳酸钾能与氯化钙反应)。请回答:

-
(1) 生成沉淀的质量是g。
-
(2) 草木灰中碳酸钾的质量分数是 。
-
(3) 恰好完全反应时所得氯化钾溶液中溶质的质量分数。(写出计算过程)
如图是硝酸钾(KNO3)和氯化钾(KCl)的溶解度曲线,请回答下列问题。

-
(1) 10℃时,KNO3和KCl的溶解度大小关系是:KNO3KCl(填“>”“<”或“=”)。
-
(2) 60℃时,将120g KNO3固体放入100g水中,充分溶解后,所得溶液的质量为g。
-
(3) KNO3中混有少量的KCl,可用的方法提纯KNO3。
-
(4) 据题图,下列有关说法正确的是。
a.KCl的不饱和溶液只能采用蒸发溶剂的方法才可变成饱和溶液
b.60℃时,KNO3溶液的溶质质量分数一定比KCl溶液的大
c.将60℃时KNO3和KCl两种溶液分别降温至10℃,析出晶体较多的是KNO3溶液
d.60℃时,从KNO3和KCl两种饱和溶液中获得等质量晶体,蒸发水较多的是KCl溶液
为预防禽流感,某同学为养鸡场配制消毒液,在用量筒量取浓的氯胺(NH4Cl)消毒液的体积时仰视读数,量取水的体积时俯视读数(其他操作过程均符合题意),则所配消毒液的质量分数( )
A . 无影响
B . 偏大
C . 偏小
D . 无法确定
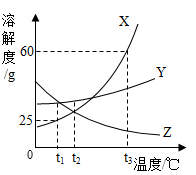
如图所示为X、Y、Z三种固体物质(不含结晶水)的溶解度曲线,请回答下列问题:
-
(1) Y中含有少量X,应采用的方法提纯Y。
-
(2) t3℃时,溶质质量分数为15%的X溶液降温到t1℃,所得溶液中溶质质量分数是。
如图是甲、乙、丙三种物质的溶解度曲线。下列说法正确的有( )

① t1℃时,甲,乙、丙三种溶液的溶质质量分数的大小关系为丙>乙=甲
② 甲中混有少量乙,可采用降温结晶的方法提纯甲
③ t2℃时,将等质量的甲、乙、丙三种物质加水溶解配成饱和溶液,所得溶液质量大小关系为丙>甲>乙
④ 将t3℃时100g溶质质量分数为30%的甲溶液降温至t2℃,有晶体析出
A . ①②
B . ③④
C . ②③
D . ②④
-
(1) 20℃时NaCl的溶解度是36g,则20℃时NaCl饱和溶液中溶质的质量分数是
-
(2) 被汗水浸湿的衣服晾干后,常出现斑迹,原因是
最近更新
- 政府的权威,是指政府在社会管理和公共服务过程中形成的威望和公信力。从根本上讲, 一个政府能否具有威信是由
- ―The Chengdu city is taking on a new look every day.―So it i
- 分解因式:2x2-4x= .
- 下列实验基本操作中,正确的是 A.倾倒液体 B.过滤 C.加热液体
- 下图四幅图中分别表示世界洋流模式图、三圈环流模式图、海陆间水循环示意图和地球公转运动示意图,其中正确的是A.①
- --- Do you have enough to ___________all yourdaily expenses
- I’m thinking about _____ a school party in my house.A. have
- 图为嫁接过程示意图,请据图回答⑴请填写下列结构的名称: [ 1 ] [2 ] [ 3 ]
- 宁西铁路是我国跨世纪铁路建设中的一条横贯东西的铁路干线,东起南京,西至西安,五个省区,全长1030.2千米,是中国“十五
- 下列反应既属于氧化还原反应又属于化合反应的是 A.Na2CO3+CO2+H2O===2NaHCO3 B.4Fe(OH)2
- 下图示生态系统各成分间的相互关系,A、B、C代表生态系统的生物部分,请分析回答:(8分)⑴若A、B、C包括地球上所有的生
- (10内江2)20℃时,碳酸氢钠的溶解度为9.7g,其含义是在20℃时___________________;工业上用氨
- 阅读下面文字,完成下题 元曲,作为一种韵文,向来与唐诗、宋词鼎足而立,它不但是那一个时代灿烂文化的象征,而且是中国传统文
- (8分)(1)以下均为中学化学中的常见实验装置,下列有关说法正确的是______。A.装置①,用于分离沸点不同的两种液态
- 如图所示,若两匹马各用1000N的力沿完全相反的方向拉同一弹簧测力计,则此时弹簧测力计的读数为A.2000N
- 阅读下面课内语段,完成10—13题。(20分) “你没有心。”高个子的党卫队队员说。 “啊,我有心的。”我说。我因为还有
- 以测定的CO2吸收量与释放量为指标,研究温度对某绿色植物光合作用与呼吸作用的影响,结果如图所示。下列分析正确的是(
- . 如图所示,物重30 N,用OC绳悬挂在O点,OC绳能承受最大拉力为20N,再用一绳系OC绳的A点,BA绳能承受的最大
- David apologized for to inform me of the change in t
- . 孔雀石的主要成分为CuCO3·Cu(OH)2。某同学设计从孔雀石中冶炼铜的方案如下:回答下列问题: (1)将孔雀石粉



