1 酸及其性质 知识点题库
在一定条件下,托盘天平的两盘上各放一盛有等质量分数等体积稀盐酸的烧杯,天平成平衡状态,当加入下列各物质反应后,天平一定保持平衡的是( )
A . 分别加入等质量的Mg、Al,金属Mg完全溶解,金属Al有剩余
B . 分别加入等质量的Al、Zn,两种金属完全溶解
C . 分别加入等质量的Na2CO3和CaCO3 , 盐酸有剩余
D . 分别加入24.75g Al和24g Mg ,两种金属完全溶解
为了探究酸碱性对唾液淀粉酶催化作用的影响,小明利用蒸馏水、1%淀粉溶液、稀释的唾液、稀盐酸、氢氧化钠溶液、碘液等材料进行实验.请你完成相应的实验设计和问题分析.
【实验设计】
【实验设计】
| 实验操作 | 设计要求 |
| 步骤一:取3 支洁净的试管标为A、B、c,在各试管中分别加入1%淀粉溶液2毫升;向A 试管加入l 毫升稀盐酸和l 毫升唾液;向B试管加入1 毫升氢氧化钠溶液和1 毫升唾液;向C试管加入 | 设置对照实验 |
| 步骤二: | 控制实验条件 |
| 步骤三:10分钟后,往3支试管中分别滴入1滴碘液,观察颜色变化. | 获取实验证据 |
【问题与分析】
正确操作后,小明观察到A试管呈蓝色,而B试管没有出现预期的蓝色.他想:为什么B试管不呈蓝色?他推测可能是氢氧化钠溶液变质或者B试管中液体碱性太弱.在老师的帮助下,他证实了氢氧化钠溶液没有变质,且B试管中液体碱性强度足以抑制酶的催化作用.请你对B试管没有出现蓝色作出一种合理的猜测: .
小明同学欲做一个无壳鸡蛋,可将鸡蛋泡在某种溶液中,几天后就得到无壳鸡蛋.该溶液可能是( )
A . 白酒
B . 酱油
C . 醋
D . 食盐水
如图所示装置,将液体X滴加到固体Y中,U形管中的液面变得右高左低,则X、Y对应的试剂组是

选项试剂 | A | B | C | D |
X | H2O | H2O | H2O | 稀H2SO4 |
Y | NaCl | NH4NO3 | NaOH |
列物质敞口放置在空气中较长时间后,质量会增加且没有生成新物质的是( )
A . 浓硫酸
B . 浓盐酸
C . 烧碱
D . 生石灰
下表所列各组物质中,物质之间较如图箭头方向,通过一步反应不能实现的是( )
物质 选项 | 甲 | 乙 | 丙 | 丁 |
A | Cu | CuO | CuSO4 | Cu(OH)2 |
B | Na2CO3 | CaCO3 | CaO | Ca(OH)2 |
C | H2SO4 | Na2SO4 | BaSO4 | Ba(OH)2 |
D | CO2 | CaCO3 | H2O | O2 |

A . A
B . B
C . C
D . D
下列气体能用浓硫酸干燥,而不能用氢氧化钠固体干燥的是( )
A . H2
B . O2
C . CO2
D . N2
下列现象描述不正确的是( )
A . 碳在空气中燃烧,发出白光
B . 铁丝在氧气中燃烧,火星四射,生成黑色固体
C . 盐酸除铁锈,观察到铁锈溶解,溶液呈黄色
D . 向氢氧化钠溶液中滴加硫酸铜溶液,产生蓝色沉淀
有一种纳米润滑添加剂,由铝粉、铜粉、氧化铝粉末中的一种或几种组成,取少量该添加剂,加入足量稀盐酸,有红色固体残留并产生大量气泡;另取少量该添加剂,加入定量的硝酸银溶液,充分反应后过滤,得到滤渣和蓝色滤液,关于以上实验,有下列几种说法:
①该添加剂中一定有铜,可能有铝和氧化铝
②若向滤渣中加入足量稀盐酸,滤渣部分溶解,则该添加剂中一定有氧化铝
③滤液中最多含有三种溶质
④滤渣中一定有银和铜,滤液中一定有硝酸铝和硝酸铜
⑤通过以上实验可以证明铝、铜、银三种金属的活动性顺序
上述说法正确的有( )
A . ①②⑤
B . ②③⑤
C . ①③④
D . ②④⑤
如图所示的实验操作中,错误的是( )
A .  放置洁净试管
B .
放置洁净试管
B .  添加酒精
C .
添加酒精
C .  稀释浓硫酸
D .
稀释浓硫酸
D .  滴加液体
滴加液体
 放置洁净试管
B .
放置洁净试管
B .  添加酒精
C .
添加酒精
C .  稀释浓硫酸
D .
稀释浓硫酸
D .  滴加液体
滴加液体
欲除去氯化钙溶液中含有少量的盐酸,在不用酸碱指示剂的条件下,应加入的试剂是( )
A . 石灰水
B . 生石灰
C . 纯碱
D . 石灰石粉末
实验室中常需要使用硫酸.
-
(1) 实验室配制49g溶质质量分数为20%的稀硫酸,需要98%的浓硫酸g.
-
(2) 用温度计的液泡蘸取少量浓硫酸,放置在空气中一会儿,可观察到温度计显示温度升高,请解释其原因.
下列图示操作中错误的是( )
A .  气密性检查
B .
气密性检查
B .  pH测定
C .
pH测定
C .  浓硫酸稀释
D .
浓硫酸稀释
D .  滴加液体
滴加液体
 气密性检查
B .
气密性检查
B .  pH测定
C .
pH测定
C .  浓硫酸稀释
D .
浓硫酸稀释
D .  滴加液体
滴加液体
一辆客车夜晚行驶在公路上,发现油箱漏油,车厢里充满了汽油的气味,这时应该采取的应急措施是( )。
A . 洒水降温溶解汽油蒸汽
B . 打开所有车窗,严禁一切烟火,疏散乘客
C . 让车内的乘客集中到车厢后部
D . 开灯查找漏油部位
实验室有溶液样品 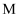 ,其中可能含有
,其中可能含有  、
、  、
、  、
、 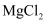 、
、  五种物质中的一种或几种。为确定样品
五种物质中的一种或几种。为确定样品 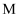 的成分,设计并完成了如下图所示的实验(假设除标有“过量”外,均恰好完全反应)。
的成分,设计并完成了如下图所示的实验(假设除标有“过量”外,均恰好完全反应)。
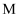 ,其中可能含有
,其中可能含有  、
、  、
、  、
、 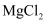 、
、  五种物质中的一种或几种。为确定样品
五种物质中的一种或几种。为确定样品 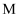 的成分,设计并完成了如下图所示的实验(假设除标有“过量”外,均恰好完全反应)。
的成分,设计并完成了如下图所示的实验(假设除标有“过量”外,均恰好完全反应)。 
-
(1) 气体
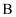 为(填化学式,下同)。
为(填化学式,下同)。
-
(2) 溶液
 中一定含有的阳离子为。
中一定含有的阳离子为。
-
(3) 该溶液样品
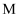 中一定含有的物质为。
中一定含有的物质为。
利用98%的浓硫酸,配制一定溶质质量分数的稀硫酸,下列描述正确的是()
A . 实验的主要步骤是计算、称量、量取、溶解
B . 用量筒量取所需的水,注入盛有浓硫酸的烧杯中
C . 实验中用到的玻璃仪器只有烧杯、量筒和胶头滴管
D . 量取浓硫酸时仰视读数,会使配得的溶液溶质质量分数偏大
稀释浓硫酸时,一定要( )
A . 迅速将水倒入浓硫酸中后搅拌
B . 把浓硫酸沿器壁慢慢地注入水中,并不断搅拌
C . 把水缓缓地倒入浓硫酸中,并不断搅拌
D . 迅速将浓硫酸倒入水中后搅拌
下列实验操作正确的是( )
A . 测定溶液pH值  B . 闻药品气味
B . 闻药品气味  C . 配制氯化钠溶液
C . 配制氯化钠溶液  D . 稀释浓硫酸
D . 稀释浓硫酸 
 B . 闻药品气味
B . 闻药品气味  C . 配制氯化钠溶液
C . 配制氯化钠溶液  D . 稀释浓硫酸
D . 稀释浓硫酸 
钢铁锈蚀的过程,实际上是铁与空气中的氧气、水蒸气等发生化学反应的过程。
防止钢铁生锈最常用的方法是在钢铁表面涂上一层保护膜。有一种防锈蚀的工艺叫烤蓝,
烤蓝的原理是在钢铁表面生成一定厚度和强度的致密的氧化层。主要工艺流程如下:

-
(1) 烤蓝工艺在钢铁表面形成的氧化膜也是磁铁矿的主要成分,其化学式为.。
-
(2) 除锈液与铁锈反应的化学方程式为.。除锈前若无水洗步骤,除锈液的使用量将.(填“增大”、“减小”或“不变”)。
-
(3) 除锈时,工件浸入除锈液 3~5min 就要取出水洗,不能长时间浸在其中的原因是.(用化学方程式表示) 。
-
(4) 烤蓝液为含有氧化剂和苛性钠的混合溶液,该过程发生多个反应,其中一个反应的化学方程式为:8Fe + 3NaNO3 + 5NaOH + 2H2O = 4Na2Fe2O4 + 3。
-
(5) 质检时将工件浸入 2%的硫酸铜溶液里,在室温下保持 20s 后取出,用水洗净表面,若不显示铜色则合格。出现铜色反应的化学方程式为.。
-
(6) 搪瓷,又称珐琅,也是防锈方法之一。它是将无机玻璃质材料(增强材料)通过熔融凝于金属(基体)上并与金属牢固结合在一起。搪瓷是一种.材料。
归纳推理是一种重要的化学思维方法。下列有关归纳推理中正确的是( )
A . 溶液是均一稳定的,所以均一稳定的物质一定是溶液
B . 中和反应能生成盐和水,所以生成盐和水的反应一定是中和反应
C . 碳酸盐能与稀盐酸反应放出气体,能与稀盐酸反应生成气体的物质一定是碳酸盐
D . 复分解反应中有沉淀或气体或水生成,而生成上述物质的反应不一定是复分解反应
最近更新
- 雨滴在下降过程中,由于水汽的凝聚,雨滴质量将逐渐增大,同时由于速度逐渐增大,空气阻力也将越来越大,最后雨滴将以某一收尾
- 人们在展望2012年的国际形势时,用到最多的一个词就是“动荡”。欧洲债务危机进一步加剧和蔓延;西亚和北非内外矛盾错综复杂
- 阅读下面的文言文,完成后面题目。(9分,每小题3分) 木假山记 【宋】苏洵 (1)木之生,或孽①而殇,或拱②而夭;幸而至
- 氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如右图。 4NH3(g)+
- 某程序框图如图所示,现输入如下四个函数,其中可以输出的函数是 . A. B.
- 是硫的原子结构示意图,其核电荷数为 A.2 B.6 C.
- 13、下列各句中,没有语病的一句是( )(3分) A.新修订的《机动车驾驶证申领和使用规定》突出规范驾驶行为、
- Susan is good at English and she _____sing English songs.
- 唐代诗人刘禹锡在一首诗中写到:“沉舟侧畔千帆过,病树前头万木春。”此诗说明的哲理是 …( ) A.事物是不断发展的
- 下列关于蛋白质工程的叙述中,错误的是( ) A.蛋白质工程的实现需要多学科技术的参与 B.蛋白质工程创造
- (11分)已知:在矩形AOBC中,OB=4,OA=3,分别以OB、OA所在直线为x轴和y轴,建立如图所示的平面直角坐标系
- My 23-year-old son Dan stood in the doorway, ready to say go
- 春节作为中华民族第一大节日,蕴含着辞旧迎新、合家团圆的寓意,是中华民族自我认同的一个文化符号。与春节“合家团圆”关系最为
- “层出不穷的诉讼案件使得法律人才辈出,许多职业传授法律知识和诉讼技巧的‘民法教授’应运而生,律师成为一种收入颇丰的社会
- 随机选取15家销售公司,由营业报告中查出其上年度的广告费x(占总费用的百分比)及盈利额y(占销售总额的百分比)列表如下:
- 全面建成小康社会,不能让一个人掉队。国家拿出更加有力的政策措施大力支持脱贫攻坚,加大中央财政对贫困地区转移支付力度,设立
- I don’t take any ______ withme. A. book B.
- 2014年以来,我国以立法的形式确立了4个国家级纪念日:抗日战争胜利纪念日(9月3日)、中国烈士纪念日(9月30日)、中
- 若某肽链的第一个氨基酸的密码子为AUG,那么控制这个氨基酸的DNA模板链上相应的三个碱基的顺序应为( ) A.UAC
- 下列有关环境、健康及能源的叙述中,不正确的是( ) A.氮的氧化物是光化学烟雾的



