第三单元 走进溶液世界 知识点题库
某同学在油菜地不慎被蜜蜂蜇伤,蜜蜂的刺液呈酸性,为了减轻痛痒,在蜇伤处涂抹的物质是( )
A . 牛奶(pH≈6)
B . 苹果汁(pH≈3)
C . 牙膏(pH≈9)
D . 矿泉水(pH≈7)
逻辑推理可以实现知识迁移,下列推理正确的是( )
A . 硝酸铵溶于水吸收大量的热,食盐溶于水也吸收大量的热
B . 铵盐与碱研磨放出氨气,尿素[CO(NH2)2]与碱研磨也能放出氨气
C . 中和反应有盐和水生成,有盐和水生成的反应一定是中和反应
D . 氢气与空气混合点燃可能爆炸,CO与空气混合点燃也可能爆炸
在宏观、微观和符号之间建立联系是化学特有的思维方式。经过一年的学,同学们对水有了更深刻的认识。根据所学知识,回答下列问题。
-
(1) 下列各种“水”中,属于纯净物的是。
a.矿泉水
b.自来水
c.蒸馏水
d.运河水
-
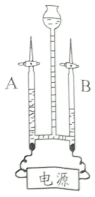
(2) 水通电可分解生成氢气和氧气。在如图的实验装置中,生成的氢气存在于玻璃管(填“A”或“B”)中。
-
(3) 水和天然气重整可以得到合成气,其反应的微观示意图如图所示:

①在微观模型A、B、C、D中,表示水分子的是(填字母代号)。
②生成物中,C和D的质量比为。
-
(4) 保护水资源是全人类的责任,下列做法合理的是。
a.大量开采利用地下水
b.农业推广节水灌溉
c.洗菜水、淘米水浇花
d.工业废水直接排放
t℃时,120g 某硝酸钾溶液蒸发17.5g 水析出2.5g硝酸钾,若原溶液蒸发掉27.5g水并恢复到t℃,则析出5g硝酸钾晶体,由此判断下列说法正确的是( )
A . 原溶液为饱和溶液
B . 蒸发后溶液溶质质量分数为25%
C . t℃时硝酸钾溶解度为25g
D . 从原溶液中蒸发水的质量与析出晶体的质量之比是一个定值
化学与人类的生产生活密切相关,请你利用所学知识回答下面问题:
-
(1) 衣服上沾有油污时可以用洗涤灵清洗,这是利用了洗涤灵的作用。
-
(2) 要想检验一团毛线是腈纶毛线还是羊毛线,方法是。
-
(3) 疫情期间常用75%的医用酒精居家消毒,但要注意不能在室内大量喷洒,使用时 注意远离火源,因为酒精是易燃物质,写出酒精燃烧的化学方程式。
-
(4) 打开汽水瓶盖常有大量气泡冒出,这是因为。
已知20℃时,氯化钠的溶解度为36 g,则在100g氯化钠的饱和溶液中,氯化钠的质量约为g,水的质量约为g。另有20℃时氯化钠固体18g,则需加入水才能配制成饱和溶液。
下列说法或做法正确的是( )
A . 所有的碱都能使酚酞试液变红
B . 亚硝酸钠是生活中常用的食盐
C . 生活中的肥皂对油污具有乳化作用
D . 电器着火,用泡沫灭火器灭火
运用分类、类比等方法学习化学,可以起到事半功倍的作用。
-
(1) 下列化学实验中都用到了玻璃棒,根据实验中所用玻璃棒的作用,应将 C 中物质归为组(填 A 或 B),理由是。
A组
B组
C





蒸发
浓硫酸稀释
过滤
测定溶液的 pH
物质的溶解
-
(2) 像氯化钠这样由(填符号)通过静电作用形成的化合物叫离子化合物。而氯化氢的形成过程则不同,氢原子趋向于得一个电子,氯原子也趋向于得一个电子,双方各拿出一个电子组成共用电子对,为两个原子所共用。像氯化氢这样以共用电子 对形成分子的化合物叫共价化合物。下列属于离子化合物的是(填字母)。
A、CO B、 H2O C、 ZnS
水是生命之源。
-
(1) 如图1是一个自制简易净水器。A 、B两层需要放置细沙或活性炭,根据净化材料的特性,A层最好放置(填“细沙”或“活性炭”)。

-
(2) 长期饮用硬水对人体健康不利,生活中常用鉴别硬水和软水。
-
(3) 电解水实验揭示了水的组成。如图2实验中得到氧气的试管是(填“1”或“2”)。
下列说法正确的是( )
A . 合成橡胶、光导纤维都属于有机高分子材料,氟、碘、锌都是人体必需的微量元素
B . 洗涤剂去油污是因为具有乳化功能,而汽油去油污是因为能溶解油污形成溶液
C . 随着铁制品的不断锈蚀,自然界中铁元素的含量不断减少
D . 金刚石、石墨、活性炭都是由碳元素组成的碳单质,物理性质不同的原因是碳原子排列方式不同
不同的物质溶于水后会形成酸碱性不同的溶液。下列溶液显酸性的是( )
A . 食醋
B . 氨水
C . CaCl2 溶液
D . Na2CO3 溶液
氢能源逐渐被推广使用。
-
(1) 氢气被称为“最清洁的燃料”是因其在空气中燃烧生成,该反应可说明水是由组成的。
-
(2) 电解水可产生氢气,反应的化学方程式为,该反应除可证明水的组成,还证明分子在化学变化中。
推理是学习化学的重要方法。下列推理合理的是( )
A . 溶液具有均一性和稳定性,则具有均一性和稳定性的液体一定是溶液
B . 常温下碱溶液的pH>7,所以该温度下pH>7的溶液一定显碱性
C . 盐是由金属离子和酸根离子组成的,所以盐中一定含有金属离子
D . CO2使饱和石灰水变浑浊是化学变化,则升温使饱和石灰水变浑浊也是化学变化
生活离不开水,水是重要的自然资源。
-
(1) 如图所示电解水的实验中,试管a、b中产生气体的体积比约为,该实验证明水是由组成的,每个水分子是由构成的。

-
(2) 城市的生活用水是经自来水厂净化处理过的。下图是自来水厂净化水的过程示意图。

①在自来水厂净化自来水的过程中,a池的作用主要是(填序号)。
A.沉淀 B.过滤 C.吸附 D.蒸馏
②取水后加入絮凝剂(明矾)的作用是。
③在处理过的水样中加入一定量的肥皂水并振荡,观察到泡沫较少,浮渣较多,说明该水样属于(填“硬水”或“软水”)。
④水资源短缺会影响人们生活,制约经济发展。请举出一种节水的措施:。
下列人体内一些液体的正常pH范围中,碱性最强的是( )
液体 | 血浆 | 胆汁 | 胰液 | 胃液 |
pH | 7.35~7.45 | 7.1~7.3 | 7.5~8.0 | 0.9~1.5 |
A . 血浆
B . 胆汁
C . 胰液
D . 胃液
水是一切生命生存所必需的物质。下列有关水的说法正确的是( )
A . 水由氢气和氧气组成
B . 正常雨水一般显中性
C . 水分子是保持水化学性质的最小粒子
D . 硬水经活性炭处理可以转化为软水
如图是A、B、C三种固体物质的溶解度曲线,下列叙述错误的是( )

A . 将t2℃时A的饱和溶液降到t1℃,可析出A固体
B . t1℃时,B物质的溶解度是60g
C . 温度低于t1℃时,能配制溶质的质量分数为37.5%的B溶液
D . t1℃时,将10gC固体投入50g水中,充分溶解后得到不饱和溶液
每年3月22日是“世界水日”。下列关于水的说法正确的是( )
A . 在净水过程中明矾作消毒杀菌剂
B . 在水中加入肥皂水振荡,浮渣较多说明是软水
C . 过滤可使硬水转化为软水
D . 电解水实验中,正、负电极产生的气体体积比约为1:2
为测定某CuSO4溶液中溶质的质量分数,取150g CuSO4溶液,平均分为三份,每份样品均按如图所示进行实验,实验数据见下表。化学方程式:CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4

|
实验1 |
实验2 |
实验3 |
|
|
样品质量/g |
50 |
50 |
50 |
|
NaOH溶液质量/g |
20 |
40 |
60 |
|
电子秤读数m/g |
42.45 |
44.9 |
44.9 |
请计算:
-
(1) 50g CuSO4溶液完全反应时,所得沉淀的质量为g。
-
(2) CuSO4溶液中溶质的质量分数。
如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。

-
(1) 图中A点表示的含义是。
-
(2) 乙中含有少量的甲,提纯乙的方法是。
-
(3) 30℃时,将9g固体甲配制成甲的溶液,至少需要加入水的质量为g。
-
(4) 下列说法正确的是(填字母序号)。
a.10℃时,用甲、乙两种固体配制等质量的饱和溶液,所需水的质量大小关系是乙>甲
b.30℃时,向乙溶液中加入固体乙,所得溶液中溶质质量分数一定增大
c.30℃时,将甲、乙饱和溶液降温到10℃,甲析出晶体的质量一定比乙多
d.在不改变溶质质量分数的情况下,要使丙的不饱和溶液变成饱和溶液,可采取升温的方法
e.10℃时,分别将100g甲和乙的饱和溶液,蒸发掉10g水,所得溶液的质量大小关系是甲>乙
最近更新
- 如果执行右面的程序框图,那么输出的 A.1 B.C.D.
- 将二氧化碳通入紫色石蕊试液,使其变 色,如将此溶液加热则溶液由 色变为 色。
- 日本血吸虫的中间寄主和终寄主分别是 A.锥实螺和人 B.人和纹沼螺 C.钉螺和人 D.扁卷螺和钉螺
- 现有可逆反应.2NO2(g) N2O4(g),△H<0,试根据下列图象,判断t2、t3、t4时刻采取的措施。 t2:
- 如图,将一副三角板拼接,使他们有公共边BC,且使这两个三角形所在的平面互相垂直,,,,BC=6. (1)证明:平面ADC
- 以下是西方的历史学家对辛亥革命的评论,其中与我们的观点相违背的是( ) ①“尽管革命以新军中士兵的爆发而开端,革命
- 一矩形线圈面积S=10-2m2,它和匀强磁场方向之间的夹角θ1=30 °,穿过线圈的磁通量Ф=1×10-3Wb,则磁场的
- 15、1926年,有报纸评论说:“自从蒋介石抬出三名主义,大出风头以后,许多人都觉得主义是值钱的,于是乎孙传芳标榜三爱(
- 观察下列一组图形中的个数,其中第1个图中共有4个点,第2个图中共有10个点,第3个图中共有19个点,……,按此规律第5个
- 党和国家领导人多次强调:“我国必须坚持人民民主专政”。这是因为①人民民主专政是民主与专政的统一 ②人民民主专政的本质
- 若(x+3y)n的展开式中各项系数的和等于(7a+b)10的展开式中二项式系数的和,则n的值为________.
- 试选用“>” 或“<”或“=”填空。(1)酸雨的pH 蒸馏水的pH; (2)碳原子中核内质子数
- On hearing the news that his father had returned from abroa
- 五四运动是中国近代史上重要的历史事件,它的历史意义有 A.打响了武装反抗国民党统治的第一枪 B.建立了中国近代第一个全国
- 中国文化传统中有许多脍炙人口、流传至今的古训,它们不仅寓意深刻,而且对人们有警示作用,例如:“人有欲,则无刚。刚则不屈于
- 请你写出一个反比例函数的解析式,使它的图象在第二、四象限 .
- 某省去年上半年受企业效益下滑、农产品价格回落等因素的影响,城乡居民收入增长同比回落6.0个和7. 6个百分点,消费预期不
- 读2005年我国人口年龄构成统计图。图中黑圆点表示我国人口年龄构成状况,其中60岁及以上的人口比重约为 ( )
- 材料一:近几届世博会的主题 1998葡萄牙 里斯本海洋—未来的财富 1999中国云南人与自然—迈向21世纪 2000德国
- 人们在吃了大鱼大肉之后发现这样的饮食方式有损健康,因此,人们又开始喜欢上了粗粮,远离了细粮。虽然粗粮确实含有大量的维生素



