第十一单元 盐 化肥 知识点题库

-
(1) 推出下列物质的化学式:BY。
-
(2) 蓝色溶液与C反应的化学方程式为。
-
(3) 黑色固体甲与X反应的化学方程式为。
| 选项 | 实验目的 | 实验方法 |
| A | 鉴别氢氧化钠溶液和碳酸钠溶液 | 分别滴加无色酚酞溶液 |
| B | 鉴别CaO和NH4NO3两种固体 | 加水、触摸烧杯外壁 |
| C | 除去MnO2中的少量KCl固体 | 加足量水溶解、过滤、蒸发 |
| D | 除去氧气中的氮气 | 将气体通过足量灼热的铜网 |
-
(1) 酸具有相似的性质,因为不同的酸在水溶液中都能解离出。
-
(2) 检验敞口放置的氢氧化钠溶液是否变质,可以选用的一种试剂是。
-
(3) 利用数字化实验设备,测定盐酸与氢氧化钠溶液反应时溶液pH变化,实验结果如图,当滴入溶液为V2mL时,所得溶液中溶质化学式为,所得溶液能使紫色石蕊溶液变成色。

-
(4) 氯化钠是生活中常见的盐,为除去某粗盐水中的MgCl2、CaCl2杂质,得到NaCl溶液,某化学小组设计了如下实验方案。

①过滤操作中所用到的玻璃仪器有烧杯、漏斗和.
②以上方案中有关反应的化学方程式为(写一个即可)
③写出溶液乙中含有的杂质,并将以上方案补充完整。
-
(5) 某实验室用40g、20%的NaOH溶液洗涤一定量石油产品中残余的H2SO4 , 消耗NaOH溶液呈中性,请计算该一定量石油产品H2SO4的质量。

-
(1) 反应①中加入焦炭时要将其粉碎,其目的是。请将反应中发生反应的化学方程式补充完整:2FeTiO3+5Cl2+6C
 2+2TiCl2+6CO
2+2TiCl2+6CO
-
(2) 钛酸亚铁(FeTiO3)中钛元素的化合价为价
-
(3) 反应②中H2比和CO在催化剂和高温的条件下发生了化合反应,请写出反应②中发生的化学方程式。
-
(4) 若要使反应②中的原料全部转化为甲醇,理论上H2和CO投料的质量比为。
| 实验目的 | 实验方法 | |
| A | 除去氯化钾固体中的氯酸钾 | 加入少量二氧化锰固体,加热 |
| B | 鉴别过氧化氢溶液和水 | 各取少量的液体,分别加入二氧化锰,观察现象 |
| C | 比较人体吸入空气和呼出气体中氧气的含量 | 将带火星的木条分别插入两种气体中 |
| D | 鉴别空气、氧气、和二氧化碳 | 在三瓶气体中倒入澄清石灰水,振荡 |
|
清洁剂 |
洁厕灵 |
去污粉 |
炉具清洁剂 |
|
功能 |
| | |
| 有效成分 | HCl | NaHCO3 | NaOH |
-
(1) 清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是。
-
(2) 洁厕灵与去污粉混合后产生大量气泡,用化学方程式表示其原因是。
 向一定质量的二氧化锰中加入过氧化氢
B .
向一定质量的二氧化锰中加入过氧化氢
B .  加热一定质量的高锰酸钾固体
C .
加热一定质量的高锰酸钾固体
C .  向一定质量的稀硫酸中加入锌片
D .
向一定质量的稀硫酸中加入锌片
D .  向一定质量的氢氧化钠溶液中加入稀硫酸至过量
向一定质量的氢氧化钠溶液中加入稀硫酸至过量

-
(1) 仪器①的名称是。
-
(2) 在过滤粗盐水时,除用到⑤⑥⑦⑧,还需要用到图中的一种玻璃仪器是(填名称)。
-
(3) 蒸发结晶食盐,除用到①②⑧⑨,还需用到图中的仪器有(填序号)。
-
(4) 下列有关蒸发结晶操作描述正确的是。
A当加热至有晶体析出时,即停止加热
B当蒸发皿中出现较多固体时,即停止加热
C当水分完全蒸干时,即停止加热
D蒸发皿应放在石棉网上加热,防止破损
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别硫酸钾和碳酸氢铵 | 闻气味 |
| B | 检测正常雨水的pH是否等于5.6 | 用pH试纸测定 |
| C | 由氧化铜制取氢氧化铜 | 直接加入NaOH溶液 |
| D | 除去氢氧化钠溶液中的氢氧化钡 | 加入过量稀硫酸 |
| A | B | C | D |
| | | | |
| 向硝酸钾饱和溶液中加入硝酸钾 | 用酒精灯加热一定量KMnO4固体 | 向一定质量的稀硫酸中加入锌片 | 向盛有MnO2的烧杯中加入H2O2溶液 |
-
(1) 进入冬季,时常有一氧化碳中毒事件发生,碳及许多含碳化合物不充分燃烧时会产生一氧化碳,一氧化碳是一种污染空气的有毒气体,它使人中毒的原因是一氧化碳与人体血液中的结合,使人体缺氧,通常采用燃烧法处理尾气中的一氧化碳。某兴趣小组同学对一氧化碳与一定量的氧气反应后所得的气体成分进行了如下实验探究:
-
(2) (提示信息)氢氧化钠溶液可吸收CO2 , 浓硫酸用于吸收水干燥气体。
(提出猜想)反应后气体的组成可能是:①CO和CO2;②只有CO2;③;
-
(3) (实验探究)该同学为了验证自己的猜想,用如图装置进行实验:

装置A中出现的现象是,发生反应的化学方程式是;
-
(4) 装置B中氢氧化钠溶液的作用是;
-
(5) 用带火星的木条伸入D中出现的现象是;
(实验结论)通过实验验证,猜想③成立。
 B . 过滤
B . 过滤 C . 量取5.5mL液体
C . 量取5.5mL液体 D . 称量固体药品
D . 称量固体药品

-
(1) 写出下列物质的化学式:B.,E.;
-
(2) 试写出上图中F+G→H的化学方程式:。
 B .
B .  、K+、Na+、Cl-
C . Cu2+、OH-、
、K+、Na+、Cl-
C . Cu2+、OH-、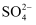 、Ba2+
D .
、Ba2+
D .  、
、 、Na+、Cl-
、Na+、Cl-
大家对这些现象很感兴趣,并进行了相关的探究:
【提出问题】锌和硫酸溶液反应后生成的气体是什么?
【查阅资料】①锌与浓硫酸反应生成硫酸锌、二氧化硫和一种常见氧化物:
②SO2有刺激性气味,易溶于水,能使品红溶液褪色。SO2与CO2化学性质相似,都能与NaOH等碱溶液反应。
③品红常作为染色剂
④相同条件下,气体的密度决定于该气体的相对分子质量,气体的相对分子质量越大密度也越大:空气的平均相对分子质量为29。
-
(1) 【猜想假设】猜想I:气球内的气体是SO2
猜想Ⅱ:气球内的气体是H2
猜想Ⅲ:气球内的气体是。
-
(2) 【实验探究】针对上述猜想,同学们在老师的指导下设计了如图的装置(部分夹持器材略去),分别用不同的气球内的气体进行探究:

实验步骤
实验现象
实验结论
①先从左端持续通入一段时间的N2点燃C装置处的酒精灯,目的是。
②甲组同学用微下沉的气球内的气体从左端缓缓鼓入,观察现象
A中品红溶液
C中无明显现象
猜想Ⅰ成立
③乙组同学用悬浮的气球内的气体用相同
装置实验,观察现象
A中品红溶液褪色
C中
猜想Ⅲ成立
-
(3) 【反思与评价】
①本次实验中锌粒于硫酸溶液反应先、后生成。
②D装置的作用是。
-
(4) 【拓展与延伸】请写出锌和浓硫酸反应的化学方程式。

-
(1) C→B的转化,一定是化合反应,该说法(填“正确”或“不正确”)。
-
(2) E→F的化学方程式为,该类反应在工业上的应用为。
- Theheadmaster suggested that a good preparation ________ ahe
- 电磁打点计时器是一种使用________(直流或交流)电源的计时仪器,它的工作电压在4~6V.当电源频率为50hz时,它
- 下列句子中,没有活用现象的一项是( ) A.园日涉以成趣。 B.或棹孤舟。 C.臣具以表闻。 D.
- (共5分)分离沸点不同但又互溶的液体混合物,常用的方法是 ;分离固液混合物的常用的方法是 ;分离两种溶解度相差很大的溶质
- 环境条件变差时对植物群落结构的影响是() A.层次不变,层次结构简单 B.层次减少,层次结构不变 C.层次减少,层次结构
- 下列植物依靠风力传播花粉的是( )A、牡丹花 B、桃花 C、玉米花
- 周王将商代贵族分封为诸侯,主要目的是( ) A.保护贵族的世袭血统 B.调和
- 下列词语中加点的字,读音完全正确的一项是 A.越俎(zǔ)代庖忧心忡忡(chōnɡ) 词清讼(sònɡ)简 飒(sà)爽
- 已知力F为两个力F1、F2的合力,如果F1和F2的夹角保持不变(两个力夹角α≤180°),则当F1、F2中的一个力增大时
- (6分)小明利用如图所示的装置探究光在平面表面的反射规律,M是一个小平面镜,E、F是两块硬纸板可以绕ON前后转动.实验时
- 随着珠三角经济的崛起,广州方言“埋单”、“打包”等餐饮用语逐渐风行全国,且发展出其本义以外的涵义。这表明( )
- (05北京卷)运动员在长跑比赛中,会出现呼吸极度困难、腿酸痛,甚至有不想再跑的念头,但是当听到震耳的“加油”声后,却能加
- 如图是有关生物的生理过程的描述,下列针对这四幅图象的叙述不正确的是( )A.图1中光照强度为B时,光合作用强度与呼吸
- 20世纪60年代以来,环境问题越来越引起人们的重视。据此完成下面试题。 图4所示城市规划建设一个化工厂(图中阴影部分表示
- SO2通入下列溶液中,溶液褪色或变浅。说明SO2具有漂白作用的组合是 ( ) ①KMnO4(H+,aq) ②溴水
- 有关受精作用的叙述,不正确的是 A.受精作用是卵细胞和精子相互识别、融合成受精卵的过程 B.受精作用对维持生物前后代体细
- 读图,回答问题。从B大洲最大港至G大洲最大港,沿最短海上航线所经过的海峡依次是下图中的( )A.①②③④
- 《百家姓》在不同朝代有不同的排序。宋代为:赵钱孙李、周吴郑王、……明代为:朱奉天运、富有万方……”这种排列主要体现了
- Hebelieved that these creatures are linked to a common ance
- The secretary is very carefuland never ________ any little p









