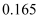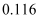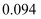课题3 溶液的浓度 知识点题库
某校化学兴趣小组用一瓶含有少量氯化钠的硫酸钠固体样品,进行如图所示的实验.

请根据以上信息计算(结果保留到小数点后两位):
-
(1) 反应生成沉淀的质量为 .
-
(2) 样品中氯化钠的质量.
-
(3) 滤液中溶质的质量分数.
如图所示是甲、乙、丙三种固体物质的溶解度曲线.

-
(1) t2℃时,甲、乙、丙三种物质的溶解度大小关系是;
-
(2) t1℃时,50g水中加入30g的甲物质充分溶解后,可得到g溶液;
-
(3) 下列说法正确的是(填序号) .
①t1℃时,甲、丙两溶液的溶质质量分数一定相等
②t3℃时,向100g20%甲的溶液中加100g水,充分搅拌,溶液的溶质质量分数为10%
③t2℃时,升高丙溶液的温度,一定有晶体析出
④t3℃时,用等质量的甲、乙、丙分别配制成三种物质的饱和溶液,所需溶剂的质量为甲<乙<丙.
某小组同学在整理化学试剂时,发现一瓶标签残缺的无色液体(如图).
![]()
-
(1) 小组的同学对这瓶液体是什么进行了猜想.
猜想一:水 猜想二:稀硫酸 猜想三:过氧化氢溶液.
小组同学对标签又进行了仔细的观察、分析,他们一致认为猜想一不合理.理由是.
-
(2) 同学们结合所学知识设计出探究方案并进行实验:
向盛有少量二氧化锰的试管中加入适量的该液体,并将带火星的木条放在试管口,发现有大量气泡产生,带火星的木条复燃.以上事实证明猜想是正确的
-
(3) 为避免在今后的实验中出现标签残缺的情况,在倾倒液体时应注意.
如图是a、b两种固体物质的溶解度曲线.从图中获得的信息错误的是( )

A . a物质的溶解度随温度升高而增大
B . 30℃时,b物质的溶解度为20g
C . t℃时,a、b的饱和溶液溶质质量分数相等
D . 30℃时的b物质饱和溶液降温至10℃,溶液中溶质质量分数不变
现将50g溶质质量分数为98%的浓硫酸稀释成20%的稀硫酸,需加水 g.
图1为甲、乙两种物质(均不含结晶水)的溶解度曲线图.请回答下列问题.

-
(1) 在10℃时,甲的溶解度乙的溶解度.(选填“>”“<”或“=”)
-
(2) 在20℃时,向盛有50g水的烧杯中加入25g甲物质,充分搅拌后溶液质量是g.
-
(3) 取乙进行如图2实验,属于饱和溶液的是,溶质质量分数最大的是.

如图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述正确的是( )

A . t1℃时,等质量的甲、乙溶液中所含溶质的质量为乙>甲
B . t2℃时,20g丙能溶解于50g水中形成70g溶液
C . 若要将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法
D . t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t2℃,所得溶液溶质质量分数的大小关系为乙>甲>丙
向盛有26.4g硫酸钠和碳酸钠混合物的烧杯中加入218g稀硫酸,恰好完全反应,固体全部消失,反应后所得溶液总质量为240g.请计算:
-
(1) 原混合物中碳酸钠的质量.
-
(2) 反应后所得溶液中溶质的质量分数(写出计算过程)
下列四个图象的变化趋势,能正确描述对应操作的是( )
A . 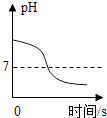 向一定量的氢氧化钠溶液中不断地滴加水
B .
向一定量的氢氧化钠溶液中不断地滴加水
B . 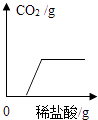 向一定量久置于空气中的氢氧化钠固体中不断地滴加稀盐酸
C .
向一定量久置于空气中的氢氧化钠固体中不断地滴加稀盐酸
C . 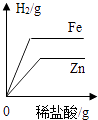 向等质量的锌、铁颗粒中分别滴加足量相同浓度的稀盐酸
D .
向等质量的锌、铁颗粒中分别滴加足量相同浓度的稀盐酸
D . 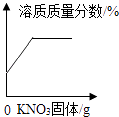 向t℃一定量饱和硝酸钾溶液中不断加入硝酸钾固体
向t℃一定量饱和硝酸钾溶液中不断加入硝酸钾固体
 向一定量的氢氧化钠溶液中不断地滴加水
B .
向一定量的氢氧化钠溶液中不断地滴加水
B . 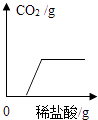 向一定量久置于空气中的氢氧化钠固体中不断地滴加稀盐酸
C .
向一定量久置于空气中的氢氧化钠固体中不断地滴加稀盐酸
C . 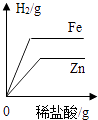 向等质量的锌、铁颗粒中分别滴加足量相同浓度的稀盐酸
D .
向等质量的锌、铁颗粒中分别滴加足量相同浓度的稀盐酸
D .  向t℃一定量饱和硝酸钾溶液中不断加入硝酸钾固体
向t℃一定量饱和硝酸钾溶液中不断加入硝酸钾固体
图1是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线,图2是30℃时,取其中两种固体各1g分别放进盛有10g水的两支试管中,充分振荡后的溶解情况,下列说法正确的是( )

A . 甲物质的溶解度比乙物质的溶解度大
B . 加入试管1的固体是丙
C . 向烧杯中加入NH4NO3固体后,试管2中一定有晶体析出
D . 将30℃时甲、乙、丙三种物质的饱和溶液降温至20℃,所得溶液中溶质的质量分数的大小关系是乙>甲=丙
根据表中内容回答下列问题。
温度 溶解度 物质 | 0 | 20 | 40 | 60 | 80 |
| | | | 110 | 169 |
NaCl | | | | | |
| | | | | |
-
(1) 随温度升高,
 溶解度的变化趋势是
溶解度的变化趋势是  填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变”  。
。
-
(2) 根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是。
-
(3) 取
 、NaCl两种固体各36g分别放入
、NaCl两种固体各36g分别放入 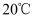 时的100g水中充分溶解,
时的100g水中充分溶解, 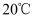 时存在如图1所示的实验现象,烧杯b中溶解的物质是;烧杯a所得溶液溶质的质量分数是
时存在如图1所示的实验现象,烧杯b中溶解的物质是;烧杯a所得溶液溶质的质量分数是  结果精确到
结果精确到  ,若要使其溶质质量分数增大可采用的方法是。
,若要使其溶质质量分数增大可采用的方法是。
-
(4) 如图2所示,若向烧杯中加入足量的硝酸铵固体并使之充分溶解,在试管中可观察到的现象是。
在实验室里配制100g溶质的质量分数为10%的NaCl溶液。
-
(1) 用NaCl固体和蒸馏水配制溶液时,用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和;
-
(2) 用浓溶液配制稀溶液时,计算的依据是稀释前后的质量保持不变;
-
(3) 下列配制方法可以达到上述实验目的的是___________。A . 将10gNaCl固体与100g水混合溶解 B . 向50g溶质的质量分数为20%的NaCl溶液中加入50g水
有a、b、c三种物质溶解度曲线如图所示,请据图回答:

-
(1) 在t2℃时,三种物质溶解度的大小顺序是:。
-
(2) 如果将a物质的饱和溶液从t2℃降温到t1℃,所得到溶液 (填“是”或“不是”)饱和溶液。
-
(3) t1℃ 时,将12克a物质加入到50克水中,将得到 克溶液。
-
(4) t1℃ a、b、c的饱和溶液升温到t2℃后,质量分数的大小顺序是:。
用氢氧化钠溶液测定某硫酸溶液溶质的质量分数。实验如下:取25g该硫酸溶液,加入到烧杯中,然后把50g质量分数为10%的氢氧化钠溶液不断滴入烧杯中,同时用电子pH计不断读取反应时的pH,得出如图所示的关系(硫酸钠溶液显中性),求该硫酸溶液溶质的质量分数。

下图为几种固体的溶解度曲线,回答下列问题:

-
(1) NaCl的溶解度随温度变化的规律是。
-
(2) 30℃时,KNO3溶液的最大浓度(溶质质量分数)为(只列计算式,不需要计算结果)。
-
(3) 60℃时,10g NaCl和90g KNO3完全溶解于100g蒸馏水, 冷却到30℃后,(“有”或“没有”)NaCl析出,有g KNO3结晶析出。
下图是M、N两种物质的溶解度曲线,由溶解度曲线得出以下几条信息,你认为不正确的是( )

A . t1℃时,M、N两物质溶液的溶质质量分数相等
B . N物质的溶解度随温度的升高而降低
C . t2℃时,M物质的溶解度大于N物质的溶解度
D . 由t1℃升温到t2℃时,N物质溶液的溶质质量分数可能改变
蔬菜水果是人类餐桌上的必备食物。
-
(1) 蔬菜水果中富含(填序号),该营养素可调节新 陈代谢、预防疾病、维持身体健康。
A 油脂 B 维生素 C 蛋白质
-
(2) 食用果蔬前,用清水浸泡可适当降低农药残留。 浸泡时间对农药去除率的影响如图,分析如图得到的结论是。

-
(3) 在 500g 清水中加入 5g 小苏打,完全溶解后, 配制成的果蔬清洗剂,其溶质质量分数的计算式为。
电动自行车、小汽车等交通工具中都有为其提供电能的铅蓄电池(又称“电瓶”),它的优点是可以充电循环使用。电瓶的正极材料是二氧化铅(PbO2),
负极材料是金属铅(Pb),电瓶内所加液体是溶质质量分数为36%的稀硫酸,放电(为外界供电)时发生反应的化学方程式如下:  。当放电时,反应物反应掉一定量后,就会导致电压下降,不能正常使用,这时就必须及时充电。
。当放电时,反应物反应掉一定量后,就会导致电压下降,不能正常使用,这时就必须及时充电。
 。当放电时,反应物反应掉一定量后,就会导致电压下降,不能正常使用,这时就必须及时充电。
。当放电时,反应物反应掉一定量后,就会导致电压下降,不能正常使用,这时就必须及时充电。
-
(1) PbO2中铅元素与氧元素的质量比为。
-
(2) 若用86.4%的浓硫酸来配制该稀硫酸1200克,需要加水多少克?
-
(3) 假如某个电瓶中内装36%的稀硫酸1200克,当有414克的铅恰好反应完时,求反应后溶液中硫酸的质量分数(最后结果保留一位小数)。
甲、乙两种固体物质的溶解度曲线如下图所示。

-
(1) t1℃时,甲、乙饱和溶液中溶质的质量分数:甲乙(填“>”“<”或“=”)。
-
(2) t2℃时,将60g乙物质放入100g水中,所得溶液中,溶质与溶剂的质量比为(填最简整数比)。
-
(3) 现有t2℃时,甲、乙两种物质的饱和溶液各100,将这两种溶液分别降温到t1℃,所得溶液中溶质的质量分数甲乙(填“>”、“<”或“=”)。
-
(4) 小明同学进行了如下图所示的实验:

上述实验过程中所得的溶液,属于不饱和溶液的是(填序号),溶液中溶质的质量分数相同的是(填序号)。
-
(5) 喝了汽水以后,常常会打嗝。这说明随温度升高气体的溶解度。
a、b、c三种固体物质的溶解度曲线如图所示。下列说法正确的是( )

A . t1℃时,a物质的溶解度是30g
B . t2℃时,b的饱和溶液中溶质的质量分数为50%
C . t3℃时,各取15ga、b、c三种物质分别加入到50g水中充分溶解,能得到饱和溶液的是c
D . t3℃时:a、b、c三种物质的饱和溶液均降温到t1℃,三种物质溶质质量分数大小关系为b>c>a
最近更新
- 在一个种群随机抽出一定数量的个体,其中基因型AA的个体占24%,基因型Aa的个体占72%,则基因A和a的频率分别是(
- (2015•攀枝花)在某生态环境中有不同毛色的同种兔子,调查其数量如图甲,多年后再调查其数量如图乙,下列叙述不合理的是(
- 下列各选项中所述的两个量,前者一定大于后者的是 ()
- 所谓“人口红利”,是指一个国家的劳动年龄人口占总人口比重较大、抚养率比较低,为经济发展创造了有利的人口条件的局面。201
- (本小题满分12分) 如图,在长方体中,,为的中点,为的中点。 (1)证明:; (2)证明:平面;
- 若的内角满足,则是( ). A. 直角三角形 B. 等腰三角形 C. 等边三角形 D.
- γ -氨基丁酸是一种神经递质,能增强突触后膜对Cl-的通透性,造成Cl-内流。下列说法正确的是 A.突触间隙中的Cl
- 读图3完成10—11题10.图中两条小河的流量相当。进入小镇的引水线最合理的是 A.① B.② C.③ D.④ 11.小
- 2009年下半年,中国国内黄金价格随世界黄金市场走暖而持续上扬,加上人们对通货膨胀的心理预期,黄 金成为投资者投资、收藏
- 27现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的
- 将下面的长句改写为4个语意连贯的短句,使句意更清楚,行文更流畅。(不能改变原意,可以增删、调换个别词语) 以“传承民族文
- 李白的诗歌的特点是 A.直白如话 B.沉郁悲怆 C.豪迈奔放 D.委婉清新
- 点M(x,y)在函数y=-2x+8的图象上,当x∈[2,5]时,求的取值范围.
- 现有等量的A、B两个品种的小麦种子,将它们分别置于两个容积相同、密闭的棕色广口瓶内,各加入适量(等量)的水。在25℃的条
- 函数的单调减区间为
- 高温下超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为-2价。如右图所示为超氧化钾晶体的一个晶胞(晶体中最小
- 如图,以数轴的单位长度线段为边作一个正方形,以表示数1的点为圆心,正方形对角线长为半径画弧,交数轴于点A,则点A表示的数
- There’s a small cross by the side of Highway128, near the to
- 10多年前,消费者视温州鞋为假冒伪劣产品的代名词,不屑一顾。10多年后的今天,温州有900多家皮鞋企业实行品牌经营,有的
- 在灾害强度相同情况下,自然灾害的危害程度存在地域差异,以下说法正确 的是