第3章 空气与生命 知识点题库
-
(1) 当生成0.7g氢气时,氢气与氧气在相同条件下的体积比约为.
-
(2) 电解水过程中,当生成1g氢气时水溶液中氢氧化钠的质量分数(请写出解题过程)
(1 )碳酸→水+二氧化碳
(2 )镁+氧气  氧化镁
氧化镁
(3 )氧化钙+水→氢氧化钙
(4 )酒精+氧气  水+二氧化碳
水+二氧化碳
(5 )氢气+氧气  水
水
(6 )高锰酸钾 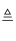 锰酸钾+二氧化锰+氧气.
锰酸钾+二氧化锰+氧气.
选项 | A | B | C | D |
甲 | 离子 | 茎 | 氧化反应 | 原子核 |
乙、丙、丁 | NH4+、K2MnO4、 Na+ | 树皮、韧皮部、 形成层 | 呼吸作用、铁生 锈、塑料老化 | 质子、电子、中子 |

-
(1) 图甲装置内物质充分反应后,冷却至室温,气球仍胀大的是(填“A”“B”或“A和B”)。
-
(2) 若图乙装置内Na2CO3溶液的质量为5克,滴入试管的稀盐酸质量也是5克,装置内物质充分反应后,发现NaOH浓溶液质量增加0.22克,试管中滴入紫色石蕊试液变红。根据上述已知条件,通过分析可以确定的是(填序号)。
①原稀盐酸的溶质质量分数
②原Na2CO3溶液的溶质质量分数
③原NaOH溶液的溶质质量分数
④反应后试管中NaCl的溶质质量分数
-
(3) 请你选择(2)所填的其中一项,通过计算确定其溶质质量分数是多少?
 B .
B .  C .
C .  D .
D . 

-
(1) 判断①处化学反应所属的基本反应类型是。
-
(2) 上述反应流程中,可循环利用的物质是 。
-
(3) 若CO2捕捉室中有溶质质量分数为40%的NaOH溶液100千克,求理论上可捕捉CO2的质量(要求列式计算)。



-
(1) 若 X 为 Na2SO4,则对应的图象应为(填标号),所发生的反应的化学方程式为。
-
(2) 若 X 为 Na2CO3,则对应的图象应为(填标号)。
【查阅资料】①铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液;
②铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮。
|
实验一 |
实验二 |
实验三 |
|
|
实验 方案 |
| | |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色。 | 无现象 | 铝片表面产生气泡较快。 |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢。 | 铜不与稀硫酸反应 | 铝能与稀硫酸反应,反应速率较快。 |
| 三种金属在金属活动性顺序中的相对位置关系是 | |||
【回答问题】
-
(1) 三种金属在金属活动性顺序关系是。
-
(2) 实验一所发生的反应的化学方程式是。
-
(3) 小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是。

-
(1) 步骤①和步骤②均用到的操作是。
-
(2) 溶液A中所含的阳离子有。
-
(3) 步骤③制得Mg(OH)2的化学方程式为 。
请回答:

-
(1) A物质的类别是。(选填“酸”或“碱”)
-
(2) E的化学式是。
-
(3) C−D的化学方程式是。

-
(1) 樱桃中的食用部分是由花结构中的发育而来。
-
(2) 图甲中C在结构层次上属于。
-
(3) 樱桃储存的有机物主要是从叶通过叶脉中运输来的。
-
(4) 分析图乙可知,为提高大棚中樱桃产量,可以采取的措施有。

-
(1) 实验过程:
序号
实验步骤
实验现象
1
连接好仪器后,检査气密性:关闭A的活塞,用酒精灯微热硬质玻璃管一 会儿,再撤掉。
说明气密性良好
2
在C中加入样品W克,称得D检查气密性后总质量为m1克
/ 3
打开A的活塞,慢慢滴加溶液。
B、E中有气泡产生
4
对C进行加热,当C中药品充分反应后,关闭A的活塞,停止加热。
/ 5
冷却后,称得D的质量为m2克
/ -
(2) 计算:样品中铜的质量分数=(用含W、m1、m2的代数式表示)。
-
(3) 问题和讨论:实验完成后,老师指出按上述实验设计,即使C中反应完全,D中吸收完全,也不会得出正确的结果,所测得的铜的质量分数会 (填“偏大”或“偏小”)。经讨论,小江提出在B与C之间加入一个洗气瓶,则其中盛放的药品是。

-
(1) 区分袋里装的蔬菜是否被烫过的依据是。
对比观察到的实验现象,能验证新鲜蔬菜进行的生理活动是。
-
(2) 实验时,为什么要用黑色塑料袋装蔬菜?。

-
(1) 茶树从土壤中获得生长所需的养料和水分。高山上的枯枝落叶等通过土壤中的分解作用,转化为茶树根可以吸收的。
-
(2) 一定高度的山区有较大的昼夜温差,有利于茶树积累有机酸、茶多酚和生物碱等有效成分,这是因为。

-
(1) 配制18%的稀盐酸100 g,需要这种浓盐酸的体积约为mL(保留一位小数)
-
(2) 某同学想测试一包含有杂质的碳酸钙固体的纯度,取该固体8 g,加入以上配制的质量分数为18%的盐酸至不再产生气泡为止,共生成气体的质量为2.2 g,试计算该包固体中所含碳酸钙的质量分数? (可能用到的相对原子质量:H-1、C-12、O-16、Ca-40、Cl-35.5)

-
(1) 图一中②代表的气体为,[A]代表的细胞器为,A处进行的生理活动能(填“储存”或“释放”)能量。
-
(2) 图二中表示光合作用的曲线为(填“甲”或“乙”),乙所表示的生理活动强度白天比夜间。在此一昼夜内,有机物累积最多的点是图中的(填“M”或“P”或“Q”或“N")。

[提出问题]碳和氧化 铜反应生成的气体是什么?
[作出猜想]猜想①:CO;猜想②:CO2;猜想③:CO和CO2;猜想④;SO2和CO2
[定性分析]
-
(1) 小明认为猜想④是不合理的,他的判断依据是。
-
(2) 若观察到 (填写现象) ,则可排除猜想①。
[定量分析]用电子天平测定表格中的四个数据如表所示:
反应前质量
反应后质量
A(试管+固体)
m1
m2
B+C+D(广口瓶+溶液)
m3
m4
-
(3) 若猜想②成立,则理论上m1、m2、 m3、m4数值满足的关系是。
- 下图a、b表示种群在不同条件下的增长曲线,c为b曲线对应的种群增长率。下列叙述错误的是( )
- 在有机反应中,反应物相同而条件不同,可得到不同的主产物。下式中R代表烃基,副产物均已略去。请写出实现下列转变的各步反应的
- 某温度下,在一个2L的密闭容器中,加人4molA和2molB进行如下反应:3A(g)+2B(g)4C(?)+2D(?),
- X、Y、Z、R、W是5种短周期元素,原子序数依次增大;它们可组成离子化合物Z2Y和共价化合物RY3、XW4;已知Y、R同
- ________is expected that it will be fine tomorrow,when we ca
- 已知两个不同的平面,和两条不重合的直线,,有下列四个命题: ①若,则 ②若,且,则 ③若,则 ④若,,则 其
- 设NA代表阿佛加德罗常数,下列说法中正确的是( ) ①常
- So difficult ______ it to live in an English-speaking countr
- 阅读下面的宋词,完成14-15题。 览卢子蒙侍御旧诗,多与微之唱和,感今伤昔
- 读图,结合所学知识回答20-21题20. 正确反映我国城市化水平的曲线是( ) A.甲 B.乙
- 小虫从某点O出发在一直线上来回爬行,假定向右爬行的路程记整数为正数,向左爬行的路程记为负数,爬行的各段路程依次为(单位:
- 18世纪初,一位名叫伯纳德•曼德维尔的荷兰医生写了一本《蜜蜂的寓言》,叙述了一个蜂群的兴衰史。最初,蜜蜂们追求奢侈的生活
- 3―甲基―2―戊烯的结构简式是
- It was the district sports meet. My foot still hadn’t healed
- 2011年11月30日,我国首艘高速客滚轮“________”,从福建平潭首航台湾台中,单程航行只需2小时30分钟,此
- 直线与直线相交于点(1,-2),则=_____,b=____。
- 已知,运算原理如右图所示,则输出的值为 A. B. C. D.
- 下列离子方程式中,属于水解反应的是( ) A.CH3COOH+H2OCH3COO--+H3O+ B.C
- 下列对称图形中,是轴对称图形,但不是中心对称图形的有() A. 1个
- 如图所示,一足够长的固定斜面与水平面的夹角为37°,质点A以初速度v1从斜面顶端水平抛出,距离斜面顶端L=15m的质点B






