高考化学真题重组卷 7+4专题冲刺 专题7 水溶液中的离子平衡及pH计算
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
(14分)(砷(As)是一些工厂和矿山废水中的污染元素,使用吸附剂是去除水中砷的有效措 施之一.
|
|
| 2. 综合题 | 详细信息 |
|
(14分)H2S和SO2会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列方法中的问题.
Ⅰ.H2S的除去 方法1:生物脱H2S的原理为: H2S+Fe2(SO4)3═S↓+2FeSO4+H2SO4 4FeSO4+O2+2H2SO4
|
|
| 3. 综合题 | 详细信息 |
|
硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下:
回答下列问题:
|
|
| 4. 单选题 | 详细信息 |
|
某温度下,
 和 和  的电离常数分别为 的电离常数分别为  和 和  。将 。将  和体积均相同的两种酸溶液分别稀释,其 和体积均相同的两种酸溶液分别稀释,其  随加水体积的变化如图所示。下列叙述正确的是( ) 随加水体积的变化如图所示。下列叙述正确的是( )
A . 曲线Ⅰ代表
 溶液
B . 溶液中水的电离程度:b点>c点
C . 从c点到d点,溶液中 溶液
B . 溶液中水的电离程度:b点>c点
C . 从c点到d点,溶液中  保持不变(其中 保持不变(其中  、 、  分别代表相应的酸和酸根离子)
D . 相同体积a点的两溶液分别与 分别代表相应的酸和酸根离子)
D . 相同体积a点的两溶液分别与  恰好中和后,溶液中 恰好中和后,溶液中  相同 相同
|
|
| 5. 单选题 | 详细信息 | |||||||||||||||
|
室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 6. 单选题 | 详细信息 |
|
以酚酞为指示剂,用0.1000 mol·L−1的NaOH溶液滴定20.00 mL未知浓度的二元酸H2A溶液。溶液中,pH、分布系数
 随滴加NaOH溶液体积VNaOH的变化关系如图所示。[比如A2−的分布系数: 随滴加NaOH溶液体积VNaOH的变化关系如图所示。[比如A2−的分布系数:  ] ]
下列叙述正确的是( )
A . 曲线①代表
 ,曲线②代表 ,曲线②代表  B . H2A溶液的浓度为0.2000 mol·L−1
C . HA−的电离常数Ka=1.0×10−2
D . 滴定终点时,溶液中
B . H2A溶液的浓度为0.2000 mol·L−1
C . HA−的电离常数Ka=1.0×10−2
D . 滴定终点时,溶液中 
|
|
| 7. 单选题 | 详细信息 |
|
二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理如下图所示。下列叙述错误的是
A . 海水酸化能引起
 浓度增大、 浓度增大、  浓度减小
B . 海水酸化能促进CaCO3的溶解,导致珊瑚礁减少
C . CO2能引起海水酸化,其原理为 浓度减小
B . 海水酸化能促进CaCO3的溶解,导致珊瑚礁减少
C . CO2能引起海水酸化,其原理为   D . 使用太阳能、氢能等新能源可改善珊瑚的生存环境
D . 使用太阳能、氢能等新能源可改善珊瑚的生存环境
|
|
| 8. 综合题 | 详细信息 |
|
吸收工厂烟气中的SO2 , 能有效减少SO2对空气的污染。氨水、ZnO水悬浊液吸收烟气中SO2后经O2催化氧化,可得到硫酸盐。
已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、HSO3-、SO32-的物质的量分数随pH的分布如图-1所示。
|
|
| 9. 单选题 | 详细信息 |
|
常温下,已知H3PO3溶液中含磷物种的浓度之和为0.1mol·L-1 , 溶液中各含磷物种的pc—pOH关系如图所示。图中pc表示各含磷物种的浓度负对数(pc=-lgc),pOH表示OH-的浓度负对数[pOH=-lgc(OH-)];x、y、z三点的坐标:x(7.3,1.3),y(10.0,3.6),z(12.6,1.3)。下列说法正确的是( )
A . 曲线①表示pc(H3PO3)随pOH的变化
B . H3PO3的结构简式为
 )<0.1mol·L-1-2c(HPO )<0.1mol·L-1-2c(HPO 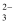 )
D . H3PO3+HPO )
D . H3PO3+HPO 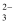  2H2PO 2H2PO  的平衡常数K>1.0×105 的平衡常数K>1.0×105
|
|
| 10. 单选题 | 详细信息 |
|
常温下,一元酸
 的 的 。在某体系中, 。在某体系中, 与 与 离子不能穿过隔膜,未电离的 离子不能穿过隔膜,未电离的 可自由穿过该膜(如图所示)。 可自由穿过该膜(如图所示)。
设溶液中
A . 溶液Ⅰ中
 B . 溶液Ⅱ中的
B . 溶液Ⅱ中的 的电离度 的电离度 为 为 C . 溶液Ⅰ和Ⅱ中的
C . 溶液Ⅰ和Ⅱ中的 不相等
D . 溶液Ⅰ和Ⅱ中的 不相等
D . 溶液Ⅰ和Ⅱ中的 之比为 之比为
|
|
- 2017-2018学年高中化学人教版 选修五 第一章 第一节 有机化合物的分类
- 湖北省黄冈市2019-2020学年高二下学期化学期末考试试卷
- 人教(新课标)高中化学一轮复习:专题1化学计量在实验中的运用
- 2015-2016学年吉林省白城市通榆一中高二下学期期中化学试卷
- 备考2018年高考化学二轮专题复习 专题九:化学反应速率与化学平衡
- 高中化学人教版(2019)选择性必修1第二章实验活动1探究影响化学平衡移动的因素
- 河北省石家庄市2017-2018学年高二下学期化学期末考试试卷
- 浙江省绍兴市2019-2020学年高二下学期化学期末考试试卷
- 2016年江西省宜春市靖安县高考化学五模试卷
- 2016-2017学年辽宁省辽师大附中高三上学期期中化学试卷
- 2015-2016学年山东省临沂市莒南三中高一下学期第一次月考化学试卷(3月份)
- 2015-2016学年湖北省襄阳市四校联考高一下学期期中化学试卷
- 阅读下面一首唐诗,回答问题。 赤壁 杜牧 折戟沉沙铁未销,自将磨洗认前朝。 东风不与周郎便,铜雀春深锁二乔。 (1)《赤
- The _____ of his clothes indicated too clearly that he had b
- 读图,回答下列问题。(每空1分,共8分)(1) 图中共包括________级天体系统。 (2)彗星的出现与流星现象在我
- “让我们荡起双浆,小船儿推开波浪,海面倒映着美丽的白塔,四周环绕着绿树红墙,小船轻轻飘荡在水中,迎面吹来了凉爽的风……”
- __________he sees people in trouble, he always lends them a
- 依次填人下列各句横线处的词语,恰当的一组是 ①广大群众认为:綦江市彩虹桥倒塌案公开审理是 公平性、公正性的体
- 用双氧水制取氧气时,若忘记加二氧化锰,其结果是 ( ) A.不放出氧气 B.放
- 化简:等于(). A. B.xy4z2C.xy4z4
- 在一条不完整的数轴上从左到右有点,,,其中,,如图所示.设点,,所对应数的和是.(1)若以为原点,写出点,所对应的数,并
- 印度的“绿色革命”指的是() A.植树种草 B.引进、培育作物的优良品种,提高粮食产量 C.大力培植牧草,发展畜牧业 D
- 两位小学生在计算“125×8÷125×8”时,得出两个不同的结果。甲同学算的结果等于64,而乙同学算的结果等于1。由此可
- — Eliza is a very girl, isn’t she? — Yes, she is.
- The designer's aimis to produce ____ shape and texture.A.mix
- 我国北方沿海航线的中心城市是:A.青岛、大连B.天津、烟台C.连云港、南通D.上海、大连
- 两条相交直线的平行投影是( ) A.两条相交直线
- 蛋白质经消化后,转变成可以被小肠吸收的
- 某同学以新鲜洋葱鳞片叶内表皮为材料,经不同处理和染色体剂染色,用高倍显微镜观察.下列描述正确的是() A.
- 下面是小明同学家本月的电费单据。据此单据,你可以得到哪些数据信息(说出两点)?××市供电局电费发票户名:×××
- 等于() A.ʃln2xdx B.2ʃln xdx C.2ʃln(1+x)dx
- The wedding took place in a Birmingham hotel. The bride and


 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
 Na2SO3溶液
Na2SO3溶液
 H++B(OH)−4 , Ka=5.81×10−10 , 可判断H3BO3是酸;在“过滤2”前,将溶液pH调节至3.5,目的是。
H++B(OH)−4 , Ka=5.81×10−10 , 可判断H3BO3是酸;在“过滤2”前,将溶液pH调节至3.5,目的是。





 生成速率越大,其主要原因是;随着氧化的进行,溶液的pH将(填“增大”、“减小”或“不变”)。
生成速率越大,其主要原因是;随着氧化的进行,溶液的pH将(填“增大”、“减小”或“不变”)。


 , 当达到平衡时,下列叙述正确的是( )
, 当达到平衡时,下列叙述正确的是( )


