备考2018年高考化学二轮专题复习 专题九:化学反应速率与化学平衡
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应2A(g)+B(g)
A . ①③
B . ①④
C . ②③
D . ③④
|
|
| 2. 单选题 | 详细信息 |
|
在372K时,把0.5mol N2O4通入体积为5L的真空密闭容器中,立即出现红棕色.反应进行到2s时,NO2的浓度为 0.02mol•L﹣1 . 在60s时,体系已达平衡,此时容器内压强为开始时的1.6倍.下列说法正确的是( )
A . 前2s以N2O4的浓度变化表示的平均反应速率为0.01 mol•L﹣1•s﹣1
B . 在2s时体系内压强为开始时的1.1倍
C . 在平衡时体系内含有N2O40.25 mol
D . 平衡时,N2O4的转化率为40%
|
|
| 3. 单选题 | 详细信息 |
|
硝酸生产中,500℃时,NH3和O2可能发生如下反应:
①4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)+9072kJ/K=1.1×1026 ②4NH3(g)+4O2(g)⇌2N2O(g)+6H2O(g)+1105kJ/K=4.4×1028 ③4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g)+1269kJ/K=7.1×1034 其中,②、③是副反应.若要减少副反应,提高NO的产率,最合理的措施是( )
A . 减小压强
B . 降低温度
C . 增大O2浓度
D . 使用合适的催化剂
|
|
| 4. 填空题 | 详细信息 |
|
请运用化学反应原理的相关知识研究元素及其化合物的性质. (1)工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为: CO(g)+2H2(g)⇌CH3OH(g)△H1=﹣116KJ•mol﹣1 又知:CO(g)+ H2(g)+ H2(g)+ 则甲醇的燃烧热为 . (2)T℃时,向2L密闭容器中充入4mol CO和6mol H2 , 5min后达平衡时CH3OH物质的量为2mol.该反应的速率v(H2)为 ;下列措施中有利于增大该反应的反应速率且提高转化率的是 . a.随时将CH3OH与反应混合物分离 b.降低反应温度 c.使用高效催化剂 d.增大体系压强 (3)在密闭容器中充有10mol CO与20mol H2 , 在催化剂作用下反应生成甲醇,CO的转化率(a)与温度(T)、压强(P)的关系如图所示. ①A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间,tA tc(填“大于”、“小于’’或“等于“). ②若A点时容器的体积为10L,该温度下B点的平衡常数K= . (4)Na2SO3的水溶液呈 (填“酸”、“中”、‘‘碱”)性,原因是(用离子方程式表示): ;把CaCO3浊液滴入l.0mol/L的Na2SO3溶液中,能否产生CaSO3沉淀?若不能,说明原因;若可行,请简述判断依据及转化过程 (已知:Ksp(CaSO3)=1.4×10﹣7 , Ksp(CaCO3)=2.8×10﹣9).
|
|
| 5. 综合题 | 详细信息 | ||||||||||||||||||||
|
催化还原CO2是解决温室效应及能源问题的重要手段之一,研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H1=﹣53.7kJ•mol﹣1 Ⅰ CO2(g)+H2(g)⇌CO(g)+H2O(g)△H2 Ⅱ 某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
[备注]Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性;转化的CO2中生成甲醇的百分比 已知:①CO和H2的标准燃烧热分别为﹣283.0kJ•mol﹣1和﹣285.8kJ•mol﹣1 . ②H2O(1)═H2O(g)△H3=44.0kJ•mol﹣1 请回答(不考虑温度对△H的影响):
|
|||||||||||||||||||||
| 6. 单选题 | 详细信息 |
|
在一定条件下,反应X(g)+3Y(g)⇌2Z(g)△H=﹣92.4 kJ/mol,X的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
A . 图中A,B两点,达到相同的平衡体系
B . 上述反应在达到平衡后,增大压强,H2的转化率提高
C . 升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小
D . 将1.0 mol X、3.0 mol Y,置于1 L密闭容器中发生反应,放出的热量为92.4 kJ
|
|
| 7. 单选题 | 详细信息 |
|
某密闭容器中,A(s)+3 B(g)⇌2 C(g)+D(g)△H>0在一定条件下达到平衡,下列说法正确的是( )
A . 加入少量A,B的转化率增大
B . 升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动
C . 增大压强,平衡不移动,正、逆反应速率不变
D . 加入催化剂,反应速率增大,平衡常数不变
|
|
| 8. 单选题 | 详细信息 |
|
下列说法正确的是( )
A . 增大体系压强,活化分子数增加,化学反应速率一定增大
B . 加入反应物,使活化分子百分数增加,化学反应速率增大
C . 活化分子间所发生的分子间的碰撞均为有效碰撞
D . 升高温度,活化分子百分数增加,化学反应速率一定增大
|
|
| 9. 单选题 | 详细信息 |
|
某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+mY(g)⇌3Z(g),平衡时,X,Y,Z的体积分数分别为30%、60%、10%,在此平衡体系中加入1molZ(g),再将达到平衡后,X,Y,Z的体积分数不变.下列叙述不正确的是( )
A . m=2
B . 两次平衡的平衡常数相同
C . X与Y的平衡转化率之比为1:1
D . 第二次平衡时,Z的浓度为0.4mol•L﹣1
|
|
| 10. 单选题 | 详细信息 |
|
在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g)⇌
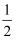 N2(g)+CO2(g)△H=﹣373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( ) N2(g)+CO2(g)△H=﹣373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
A . 加催化剂同时升高温度
B . 加催化剂同时增大压强
C . 升高温度同时充入N2
D . 降低温度同时增大压强
|
|
- 浙江省台州市2020-2021学年高一上学期化学期末考试试卷
- 山东省济宁市2022届高三第二次模拟考试化学试题
- 陕西省咸阳市2021年高考化学一模试卷
- 山东省临沂市平邑县、沂水县2020-2021学年高二上学期化学期中考试试卷
- 江苏省南京市盐城市2021年高考化学一模试卷
- 黑龙江省大庆市重点中学2021-2022学年高二下学期2月月考化学试题
- 云南省罗平县第二中学2021-2022学年高一上学期10月月考化学试题
- 河北省邢台市2020-2021学年高一上学期化学期中考试试卷
- 云南省玉溪市2020-2021学年高一下学期期末教学质量检测化学试题
- 2021年高考理综化学真题试卷(全国乙卷)
- 河南省洛阳市2020-2021学年高二上学期化学期中考试试卷
- 浙江省丽水市2020-2021学年高一上学期化学期末考试试卷
- 若(x-4)0=1,则x的取值范围是 .
- X、Y两种元素,原子序数均小于20;X、Y原子的最外层电子数相等,且原子半径X<Y,下列说法正确的是(选项中m、n
- 在△ABC中,AB=2,BC=3,∠ABC=π,若使△ABC绕直线BC旋转一周,则所形成的几何体的体积是 (A)6
- .陈独秀在《青年杂志》发刊词中宣称,“盖改造青年之思想,辅导青年之修养,为本志之天职。批评时政,非其旨也。”据此可知,此
- 秘鲁渔场是世界著名的渔场,其主要形成原因是( )A.位于寒暖流交汇处 B.深层海水上涌带来
- One day a mother brought home a small 26 and gave it to h
- 下列加点字的注音完全正确的一项( ) A. 嫩芽(nèn) 一霎那(chà) 整宿(sù) 挽回(wǎn)
- 如图是被西方视作“神秘之师”的一支中国部队,这支部队担任的主要任务是A.保卫海疆B.核讹诈C.核反击D.军备竞赛
- 若,其中是虚数单位,则 .
- (一)文言文阅读(19分) 阅读下面的文言文,完成10——13题。 萧相国何者,沛丰(沛县丰邑)人也。以文无害①为沛主吏
- 下列物质中属于纯净物的是() A.自来水
- 阅读下面的文字,完成14―17题。在西域读李白 夏立君
- 下列符号与其叙述对应一致的是() A.3H﹣﹣﹣3个氢元素 B.C60﹣﹣﹣60个碳原子 C.﹣﹣﹣铁的化合价显+
- 下图中表示北半球海洋表面水温分布图中有暖流经过的是
- 下列说法符合辩证法思想的有( ) ①动中有静,静中有动 ②是亦彼也,彼亦是也 ③对症下药,量体裁衣 ④因时制
- 下列选项中加点字的词类活用分类正确的一项是( ) ①吾从而师之 ②宁许以负秦曲 ③大将军邓陟奇其才 ④空以身膏
- 与我国陆地相邻,并且均为内陆国的有( ) A.俄罗斯、蒙古、巴基斯坦 B.哈萨克斯坦、印度、缅
- 将给定的25个数排成如图1所示的数表,若每行5个数按从左至右的顺序构成等差数列,每列的5个数按从上到下的顺序也构成等差数
- 近年来,政府在财政拨款、学校建设方面向农村倾斜,加大对革命老区、民族地区、 边疆地区、贫困地区义务教育的财政转移支付力
- 下列说法正确的有:( )A.经济全球化的主要受益者是发达国家,对发展中国家则有害无益B.最能体现经济全球化的世界性
 2C(g),若2 s(秒)后测得C的浓度为0.6 mol/L,现有下列几种说法:
2C(g),若2 s(秒)后测得C的浓度为0.6 mol/L,现有下列几种说法: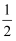 O2(g)═CO2(g)△H2=﹣283KJ•mol﹣1
O2(g)═CO2(g)△H2=﹣283KJ•mol﹣1





