高中化学人教版(2019)选择性必修1第二章实验活动1探究影响化学平衡移动的因素
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 填空题 | 详细信息 | ||||||||||||||||||||||||
|
已知Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O.甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响.设计实验如表(所取溶液体积均为10mL):
其他条件不变时:探究温度对化学反应速率的影响,应选择(填实验编号); 探究浓度对化学反应速率的影响,应选择(填实验编号); 若同时选择①②③溶液变浑浊的时间,探究对化学反应速率的影响. |
|||||||||||||||||||||||||
| 2. 多选题 | 详细信息 | ||||||||||||||||||||||||||||
|
温度为T1℃时,在四个容积均为1L的恒容密闭容器中发生反应:2NO(g)+2H2(g)
 N2(g)+2H2O(g) ΔH,该反应的速率表达式为v=k·cm(NO)·cn(H2)(k、m、n为常数),测得有关实验数据如下: N2(g)+2H2O(g) ΔH,该反应的速率表达式为v=k·cm(NO)·cn(H2)(k、m、n为常数),测得有关实验数据如下:
下列说法正确的是( )
A . m=2,n=1
B . 达到平衡时,容器Ⅱ与容器Ⅳ的总压强之比为1:2
C . 温度升高为T2℃,测得平衡时,容器Ⅱ中c(H2O)=3.8×10-4mol/L,则ΔH>0
D . T1℃时,容器Ⅲ中达到平衡后再充入NO、H2O(g)各2×10-4mol,则反应将向逆反应方向进行
|
|||||||||||||||||||||||||||||
| 3. 多选题 | 详细信息 | ||||||||||||||||||||||||||||
|
(双选)以反应5H2C2O4+2
 +6H+=10CO2↑+2Mn2++8H2O为例探究“外界条件对化学反应速率的影响”。实验时,分别量取H2C2O4溶液和酸性KMnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。 +6H+=10CO2↑+2Mn2++8H2O为例探究“外界条件对化学反应速率的影响”。实验时,分别量取H2C2O4溶液和酸性KMnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。
下列说法错误的是( )
A . 实验①②③所加的H2C2O4溶液均要过量
B . 若实验①测得KMnO4溶液的褪色时间为40s,则这段时间内平均反应速率
 (KMnO4)=2.5×10-4mol/(L·s)
C . 实验①和实验②是探究温度对化学反应速率的影响,实验②和实验③是探究浓度对化学反应速率的影响
D . 实验①和实验②起初反应均很慢,过一会儿反应速率突然增大,可能是生成的Mn2+对反应起催化作用 (KMnO4)=2.5×10-4mol/(L·s)
C . 实验①和实验②是探究温度对化学反应速率的影响,实验②和实验③是探究浓度对化学反应速率的影响
D . 实验①和实验②起初反应均很慢,过一会儿反应速率突然增大,可能是生成的Mn2+对反应起催化作用
|
|||||||||||||||||||||||||||||
| 4. 单选题 | 详细信息 |
|
为比较Fe3+和Cu2+对H2O2分解反应的催化效果,两位同学分别设计了如图甲、乙所示的实验。下列叙述错误的是( )
A . 图甲所示实验可通过观察产生气泡的快慢来比较反应速率的大小
B . 若图甲所示实验中反应速率为①>②,则说明Fe3+一定比Cu2+对H2O2分解的催化效果好
C . 用图乙所示装置测定反应速率,可测定反应产生的气体体积及反应时间
D . 为检查图乙所示装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位
|
|
| 5. 单选题 | 详细信息 | |||||||||||||||
|
下列生产或实验事实引出的相应结论错误的是
 
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 6. 单选题 | 详细信息 | ||||||||||||||||||||
|
某同学做浓度对化学反应速率的影响的实验时,将3支试管分别编号为①②③,实验结束后记录的数据如表所示。
下列叙述错误的是( )
A . 反应的化学方程式为
 B .
B .  的浓度越大,反应速率越快
C . 的浓度越大,反应速率越快
C . 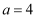 D .
D . 
|
|||||||||||||||||||||
| 7. 单选题 | 详细信息 | |||||||||||||||
|
下列有关化学反应速率的实验探究方案设计合理的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 8. 实验探究题 | 详细信息 | ||||||||||||||||||||||||||||||||||||||||||||||
|
某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
(实验原理) (实验内容及记录)
请回答:
|
|||||||||||||||||||||||||||||||||||||||||||||||
| 9. 单选题 | 详细信息 |
|
为研究某溶液中溶质 R的分解速率的影响因素,分别用三份不同初始浓度 R溶液在不同温度下进行实验,c(R)随时间变化如图。下列说法错误的是( )
A . 25℃时,10~30min 内,R 的分解平均速率为 0.030 mol·L-1·min-1
B . 对比 30℃和 10℃曲线,在同一时刻,能说明 R的分解速率随温度升高而增大
C . 对比 30℃和 25℃曲线,在 0~50min 内,能说明R 的分解平均速率随温度升高而增大
D . 对比 30℃和 10℃曲线,在 50min 时,R 的分解率相等
|
|
| 10. 单选题 | 详细信息 | ||||
|
为了探究温度对化学反应速率的影响,下列实验方案可行的是。( )
A . A
B . B
C . C
D . D
|
|||||
- 陕西省渭南韩城市2019-2020学年高二上学期化学期中考试试卷
- 湖南省衡阳市2016-2017学年高二上学期化学期末考试试卷
- 吉林省榆树一中2017-2018学年高一上学期化学期中考试试卷
- 2015-2016学年安徽省六安市舒城县晓天中学高一下学期第一次月考化学试卷
- 2017_2018学年高中化学人教版选修四 第四章电化学基础4.1原电池b
- 专题14:化学反应速率与化学平衡
- 河南省信阳市2019-2020学年高一下学期化学期末考试试卷
- 湖南省张家界市2019-2020学年高一下学期化学期末考试试卷
- 备考2019年高考化学二轮专题 15 物质结构与性质
- 广东省佛山市普通高中2017-2018学年高三化学第二次模拟考试试卷
- 福建省宁德市2019-2020学年高一下学期化学期末考试试卷
- 浙江省台州市2016-2017学年高一上学期期末考试试卷
- 下列句子中,没有语病的一句是 A.据我的愚见,斜线号是近些年才发展起来,逐渐被采用,但还没有被国家语言文字工作委员会认定
- 图为“探究求合力的方法”的实验装置.1.下列说法中正确的是 A.在测量同一组数据F1、F2和合力F的过程中,
- 如图所示,在□ABCD中,对角线AC与BD相交于点O,过点O任作一条直线分别交AB,CD于点E,F.(1)求证:OE=
- 从2007年下半年开始,山东省县乡两级人大换届选举陆续进行,这是社会主义民主一次最广泛、最深刻的实践。在县、乡和不设区的
- 下列各句中,没有语病的一句是 A.要造就一批大师,政治家能做的最有价值的贡献,是创造海纳百川的人文环境,确立鼓励追求真
- 如图4-3-4所示,在水平桌面上放一个重为GA=20 N的木块,木块与桌面间的动摩擦因数μA=0.4,使这个木块沿桌面做
- (2010北京文数)⑴ 集合,则= (A) {1,2} (B) {0,1,2} (C){1,2,3}
- 《次北固山下》中表现时序变迁、新旧交替这一自然规律的哲理句是 , 。
- 2010年春天,西南大旱提醒我们节约每一滴水,下列关于水的说法中不正确的是A.工业废水、生活污水经处理达标后再排入河中
- 下列加点的“乃”字意义和用法不相同的是【 】 A.必以长安君为质,兵乃出B.而陋者乃以斧斤考击而求之C.大王亦宜斋戒五
- 细胞的生物膜系统指的是 A、由细胞膜、核膜以及细胞器膜形成的统一膜结构 B、由内质网、高尔基体和核膜形成的具有特定功能的
- “绿色化学”要求从根源上减少或杜绝污染,下列对农作物收割后留下的秸秆的处理方法中,不符合“绿色化学”的是A.加工成饲料
- 下表为我国不同地区2000年粮食生产效率表。回答下面试题。 项目 资本投入量 人力投入量 人力效率 化肥量(千克╱公顷)
- 当m= 时,函数是反比例函数.
- 一条河流沿北纬35°自西向东流(如下图),河中有一沙坝,下列叙述正确的是A.南岸沉积作用强烈 B.北岸受冲刷严重 C.
- 材料一 2010年6月2日,世界贸易组织第三次对华贸易政策审议结束。在审议会上,引导讨论的瑞典代表发言说,加入世贸组织推
- Afterthe serious earthquake, the remote village is _____ on
- 不等式组的解集在数轴上表示为( ) A.
- 民族区域自治制度是我国基本政治制度。国务院公布《全国年节及纪念日放假办法》第四条规定少数民族习惯的节日,由少数民族聚居地
- Every possible means _______to prevent the air pollution, bu

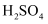 溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短
溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短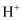 浓度相同的盐酸和醋酸分别与等质量的形状相同的锌粒反应
浓度相同的盐酸和醋酸分别与等质量的形状相同的锌粒反应 ,把容积的体积缩小一半
,把容积的体积缩小一半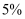 的
的  溶液,在B试管中加入
溶液,在B试管中加入  滴
滴  溶液,B试管中产生气泡快
溶液,B试管中产生气泡快












 溶液
溶液 稀硫酸
稀硫酸 溶液
溶液

 ,
,  .
.
 的浓度变化表示的反应速率为:
的浓度变化表示的反应速率为:  .
.
 随时间变化趋势的示意图,如图1所示.但有同学查阅已有的实验资料发现,该实验过程中
随时间变化趋势的示意图,如图1所示.但有同学查阅已有的实验资料发现,该实验过程中 










