高考二轮复习知识点:化学平衡移动原理1
高考二轮复习知识点:化学平衡移动原理1
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 多选题 | 详细信息 |
|
下列说法正确的是( )
A . 向稀醋酸溶液中加入少量醋酸钠固体,醋酸的电离程度增大
B . 电镀时,通常把待镀金属制品作阴极,镀层金属作阳极
C . 常温下,2NO2(g)=2NO(g)+O2(g)不能自发进行,则该反应的△H>0
D . 工业通过反应“Na(l)+KCl(l)
 NaCl(l)+K(g)”冶炼钾,说明钠的金属性强于钾 NaCl(l)+K(g)”冶炼钾,说明钠的金属性强于钾
|
|
| 2. 多选题 | 详细信息 | ||||||||||||||||||||||||||||||||||||
|
在三个容积均为2L的密闭容器中按不同方式投入反应物,发生反应:
CO(g)+H2O(g) 相关反应数据如下:
下列说法正确的是()
A . 容器Ⅰ中反应经10min建立平衡,0~10min内,平均反应速率v(CO)=0.04mol·L-1·min-1
B . 若向容器Ⅰ平衡体系中再加入CO、H2O、CO2、H2各0.1mol,平衡将正向移动
C . 达到平衡时,容器Ⅱ中反应吸收的热量小于0.1akJ
D . 达平衡时,容器Ⅲ中n(CO)<0.48mol
|
|||||||||||||||||||||||||||||||||||||
| 3. 多选题 | 详细信息 |
|
CH4与CO2重整生成H2和CO的过程中主要发生下列反应
在恒压、反应物起始物质的量比
A . 升高温度、增大压强均有利于提高CH4的平衡转化率
B . 曲线B表示CH4的平衡转化率随温度的变化
C . 相同条件下,改用高效催化剂能使曲线A和曲线B相重叠
D . 恒压、800K、n(CH4):n(CO2)=1:1条件下,反应至CH4转化率达到X点的值,改变除温度外的特定条件继续反应,CH4转化率能达到Y点的值
|
|
| 4. 多选题 | 详细信息 |
|
温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和1mol NO2 , 发生反应:2C(s)+2NO2(g)⇌N2(g)+2CO2(g)反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。下列说法正确的是( )
A . T℃时,该反应的化学平衡常数为
 B . 图中c点所示条件下,v(正)>v(逆)
C . 向a点平衡体系中充入一定量的NO2 , 达到平衡时,NO2的转化率比原平衡大
D . 容器内的压强:Pa:Pb>6:7
B . 图中c点所示条件下,v(正)>v(逆)
C . 向a点平衡体系中充入一定量的NO2 , 达到平衡时,NO2的转化率比原平衡大
D . 容器内的压强:Pa:Pb>6:7
|
|
| 5. 多选题 | 详细信息 |
|
烟气中的NO经过O3预处理,再用CaSO3悬浊液吸收去除。预处理时发生反应:NO(g)+O3(g)
 NO2(g)+O2(g)。测得:v正=k正c(NO)·c(O3),v逆=k逆c(NO2)·c(O2),k正、k逆为速率常数,受温度影响。向容积均为2L的甲、乙两个密闭容器中充入一定量的NO和O3 , 测得NO的体积分数随时间的变化如图所示。下列说法正确的是( ) NO2(g)+O2(g)。测得:v正=k正c(NO)·c(O3),v逆=k逆c(NO2)·c(O2),k正、k逆为速率常数,受温度影响。向容积均为2L的甲、乙两个密闭容器中充入一定量的NO和O3 , 测得NO的体积分数随时间的变化如图所示。下列说法正确的是( )
A . 高温有利于提高容器中NO的平衡转化率
B . T1时,反应在t1min内的平均速率v(O2)=
 mol·L-1·min-1
C . T1时,NO(g)+O3(g) mol·L-1·min-1
C . T1时,NO(g)+O3(g)  NO2(g)+O2(g)的k正>3k逆
D . T2时,向2L密闭容器中充入0.6molNO、0.4molO3 , 到达平衡时c(NO2)小于乙容器中平衡时c(NO2) NO2(g)+O2(g)的k正>3k逆
D . T2时,向2L密闭容器中充入0.6molNO、0.4molO3 , 到达平衡时c(NO2)小于乙容器中平衡时c(NO2)
|
|
| 6. 多选题 | 详细信息 |
|
在容积为2.0L的恒容密闭容器中充入3.0molCl2和4.0molPCl5 , 473K 时发生反应:PCl5(g)
 PCl3(g)+Cl2(g)△H= 92.5 kJ·mol-1 , 各物质的物质的量随时间变化关系如图所示:( ) PCl3(g)+Cl2(g)△H= 92.5 kJ·mol-1 , 各物质的物质的量随时间变化关系如图所示:( ) 下列说法正确的是( )
A . 0.0~5.0min,PCl5分解的平均速率为0.6mol·L-1·min -1
B . 起始时,若用3.0mol37Cl2和4.0mol P35Cl5 , 达平衡时,PCl3 中不含37Cl
C . 图中14.0min时,改变的外界条件可能是缩小容器的体积
D . 若在14.0min时,向容器中各充入1.0mol 的Cl2、PCl5 及PCl3 , 维持其他条件不变,重新达到平衡前,v(正)>v(逆)
|
|
| 7. 综合题 | 详细信息 |
|
不锈钢具有良好的耐腐蚀性和耐磨性,铬(Cr)是不锈钢的重要成分。完成下列填空:
|
|
| 8. 单选题 | 详细信息 |
|
硫酸是一种重要的基本化工产品。接触法制硫酸生产中的关键工序是
 的催化氧化: 的催化氧化:  。研究表明, 。研究表明, 催化氧化的反应速率方程为 催化氧化的反应速率方程为 式中:k为反应速率常数,随温度t升高而增大;α为 式中:k为反应速率常数,随温度t升高而增大;α为 平衡转化率,α′为某时刻 平衡转化率,α′为某时刻 转化率,n为常数。在α′=0.90时,将一系列温度下的k、α值代入上述速率方程,得到的v-t曲线如图所示。下列说法正确的是( ) 转化率,n为常数。在α′=0.90时,将一系列温度下的k、α值代入上述速率方程,得到的v-t曲线如图所示。下列说法正确的是( )
A . 该反应在任何温度下都能自发
B .
 与足量 与足量 充分反应,放出的热量为 充分反应,放出的热量为 C . 升高温度,能增大单位体积内活化分子百分数和活化分子数
D . 反应速率先随温度的升高而增大,原因是温度升高导致k、α均增大
C . 升高温度,能增大单位体积内活化分子百分数和活化分子数
D . 反应速率先随温度的升高而增大,原因是温度升高导致k、α均增大
|
|
| 9. 综合题 | 详细信息 | ||||||||||||
|
烟气脱硫脱硝技术是环境科学研究的热点。某小组模拟O3氧化结合(NH4)2SO3溶液吸收法同时脱除SO2和NO的过程示意图如下。
|
|||||||||||||
| 10. 单选题 | 详细信息 |
|
对于反应2SO2(g)+O2(g)⇌2SO3(g),下列说法正确的是( )
A . 该反应在任何条件下都能自发进行
B . 反应达平衡后再通入O2 , SO3的体积分数一定增加
C . 反应在高温、催化剂条件下进行可提高SO2的平衡转化率
D . 2mol SO2(g)和1mol O2(g)所含键能总和比2mol SO3(g)所含键能小
|
|
高中化学 试卷推荐
- 浙江省宁波市2021年高考化学模拟试卷
- 浙江省宁波市慈溪市2020-2021学年高一下学期期末考试化学试题
- 黑龙江省大庆市2021年高考化学一模试卷
- 福建省龙岩市2022届高中毕业班第三次教学质量检测化学试题
- 重庆市九校联盟2021-2022学年高二上学期12月联考化学试题
- 天津市南开区2020-2021学年高三上学期化学期中考试试卷
- 河南省洛阳市2021年高考化学3月试卷
- 四川省绵阳市2022届高三第三次诊断性考试理综化学试题
- 陕西省汉中市镇巴县2021-2022学年高一下学期期中考试化学试题
- 辽宁省辽阳市2022届高三一模化学试题
- 广东省深圳市第七高级中学2020-2021学年高二上学期化学第一次月考试卷
- 广东省广州市荔湾区2020-2021学年高二上学期化学期末考试试卷
最近更新
- 化学用语是学习和交流化学知识的通用语言,以下化学符号所表示的意义最多的是( ) A.Fe B.H C
- “走转改”成果丰硕。目前,全国新闻界大批编辑作者深入基层蹲点调研、采访写作,在了解基层实际、反映群众意愿、树立良好形象
- 某校实验小组的同学在探究斜面的机械效率时,他们用弹簧测力计拉着物块沿斜面向上运动,如图所示,并收集了下表中的实验数据:(
- (本小题满分12分) 2011年4月28日,世界园艺博览会已在西安正式开园,正式开园前,主办方安排了4次试运行,为了解前
- 具有结构简单,无根、茎、叶分化特征的植物类群是 A.藻类植物 B.蕨类植物 C.裸子植物 D.被子植
- 一物体自空中的A点以一定的初速度竖直向上抛出,1s后物体的速率变为10m/s,则物体此时的位置和速度方向是(不计空气阻力
- 如图所示为某新型夹砖机,它能用两支巨大的“手臂”将几吨砖夹起,大大提高了工作效率。己知该新型夹砖机能夹起质量为m的砖,两
- 函数y=2cos2x+1(x∈R)的最小正周期为………………………………()A. B.π
- 最近,一篇《法治社会不容“微博先审判”》的文章引发关注,该文针对网络上一些民众对关注度较高的案件进行围观施压的做法提出委
- Theco-operation is tothe success of the scheme. A.c
- 读“我国东部某地的等高线示意图”和“该地区的气候资料表”,图中等高线所示高度分别为100 m、200 m、300 m、4
- A、B、C、D四种元素原子的核电荷数依次增大(均小于20),其单质及相应的化合物能发生如下反应关系:(1)写出F的电子式
- 平行六面体中,既与共面也与共面的棱的条数为 .
- 默写。(5分)【小题1】曲径通幽处, 。【小题2】
- 如图所示,距水平地面高为=0.4m处,水平固定一根长直光滑杆,杆上P点固定一可绕水平轴无摩擦转动且不计大小的定滑轮,一半
- 下列措施中哪一种对保护生态环境最有利?( )A.把未经净化的工业废水直接排入河流中 B.把大片沼泽地开垦为农田
- 请回答15-16题:下图为四地区的农业产值结构和商品率示意图,读图回答下列问题。15.四地区可能的农业地域对应正确的一组
- 以下对我国法制化的历程叙述不正确的是( ) A.1949年通过的《中国人民政治协商会议共同纲领》具有临时宪法的性
- .“在最小的空间内用最简单的耕作方式养活尽可能多的人是中国的终极目标,为此,他们将土地分成小块,劳动者把全部精力都投入到
- 设NA为阿伏加德罗常数的值,下列说法正确的是 ( ) A.7.8g Na2


 条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是( )
条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是( )



 可以得到较纯的铬,
可以得到较纯的铬,  的熔点比
的熔点比  。(选填“高”或“低”),某工厂用
。(选填“高”或“低”),某工厂用  含
含  的铬铁矿粉
的铬铁矿粉  制备
制备  ,最终得到产品bkg,产率为。(用含a和b的代数式表示)
,最终得到产品bkg,产率为。(用含a和b的代数式表示)
 (绿色)、
(绿色)、  (橙红色)、
(橙红色)、  (黄色)等形式存在,
(黄色)等形式存在,  为难溶于水的灰蓝色固体。
为难溶于水的灰蓝色固体。  与
与  的化学性质相似,在
的化学性质相似,在  溶液中逐滴加入
溶液中逐滴加入  溶液直至过量,可观察到的现象是。
溶液直至过量,可观察到的现象是。 溶液中
溶液中  随
随  的变化如图所示。
的变化如图所示。 
 溶液中的转化平衡。
溶液中的转化平衡。




 , 则
, 则 。
。

 与NO2反应生成
与NO2反应生成 和
和 的离子方程式是。
的离子方程式是。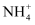 被转化为N2 , 反应中
被转化为N2 , 反应中


