高考二轮复习知识点:物质的结构与性质之间的关系
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
元素周期表中,除了22种非金属元素外,其余的都是金属,请根据元素周期表回答下列问题:
|
|
| 2. 综合题 | 详细信息 |
|
|
| 3. 综合题 | 详细信息 |
|
[化学——选修3:物质结构与性质]
一种Ru络合物与g-C3N4复合光催化剂将CO,还原为HCOOH的原理图如下。
|
|
| 4. 实验探究题 | 详细信息 |
|
化学·选修3:物质结构与性质
2019年8月13日中国科学家合成了首例缺陷诱导的晶态无机硼酸盐单一组分白光材料 Ba2 [Sn(OH)6][B(OH)4] 2并获得了该化合物的LED器件,该研究结果有望为白光发 射的设计和应用提供一个新的有效策略。
|
|
| 5. 综合题 | 详细信息 |
|
【化学——选修3:物质结构与性质】
钴及其化合物有着广泛的应用前景。回答下列问题:
|
|
| 6. 综合题 | 详细信息 |
|
硒是动物和人体所必需的微量元素之一,在周期表中信息如图所示。完成下列填空:
|
|
| 7. 综合题 | 详细信息 |
|
镁、铝、硅、银、铁的单质及其化合物在建筑业、飞机制造业、电子工业和石油化工等方面应用广泛。回答下列问题:
|
|
| 8. 综合题 | 详细信息 | ||||||||
|
磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
|
|||||||||
| 9. 综合题 | 详细信息 |
|
12月 17日凌晨,嫦娥五号完成“ 挖土” 之旅返回地球。查阅资料,月球玄武岩是构成月球的岩石之一,主要由辉石(主要成分硅酸盐)和钛铁矿(主要成分 FeTiO3)等组成。回答下列问题:
|
|
| 10. 单选题 | 详细信息 |
|
SF6可用作高压发电系统的绝缘气体,分子呈正八面体结构,如图所示。有关SF6的说法正确的是( )
A . 是非极性分子
B . 键角
 都等于90°
C . 都等于90°
C .  与 与  之间共用电子对偏向S
D . 之间共用电子对偏向S
D .  原子满足8电子稳定结构 原子满足8电子稳定结构
|
|
- 吉林省长春市农安县2019-2020学年高一下学期化学期末考试试卷
- 2016-2017学年黑龙江省哈尔滨市四校联考高一上学期期中化学试卷
- 2015-2016学年河南省信阳市明港一中高三下学期第一次月考化学试卷
- 陕西省咸阳市2020年高考理综-化学二模试卷
- 江苏省宿迁市2019-2020学年高二下学期化学期末考试试卷
- 安徽省蚌埠市田家炳中学、五中2019-2020学年高三上学期理综-化学期中考试试卷
- 浙江省绍兴市2020年高考化学联考模拟试卷
- 2015-2016学年浙江省湖州市高一下学期期末化学试卷
- 陕西省咸阳市西藏民族大学附属中学2019-2020学年高二上学期化学第二次月考试卷
- 四川省广安市2017-2018学年高一下学期化学期末考试试卷
- 2015-2016学年山东省枣庄十八中高三上学期期末化学模拟试卷(一)
- 四川省绵阳市2017-2018学年高三理综-化学三模考试试卷
- 有一个物体以初速度v0沿倾角为θ的足够长的粗糙斜面上滑,到达最高点之后又加速下滑,那么能正确表示该物体的速度v随时间t变
- 下列物质属于纯净物的是( ) A.牛奶 B.冰红茶 C.冰水混合物 D
- Prime Minister’s speech is deeply impressed _________ my mem
- I’ll never forget the moment _____I first met Mary and _____
- 有炭粉和氧化铜的黑色固体20g,加热后将生成的气体通入足量的石灰水中,气体全被吸收,产生了10g沉淀,求原混合物的组成。
- The little girl could look after ________ though she was onl
- —If I go to see my friends, I'll bring them some flowers.—__
- 若数列满足,则 .
- 拉萨与重庆的纬度相差不大,但前者的年太阳辐射总量比后者大得多。其主要原因在于拉萨的 A.气候寒冷,大气对太阳辐射的吸收强
- . When cutting the cloth for my suit, leave enough at the ed
- 已知a,b,c分别为△ABC的三个内角A,B,C的对边,m=(sinA,1),n=(cos A,),且m∥n. (1)求
- 在纪念“5.12汶川大地震”周年之际,某生态工作者,为了加速当地生态资源的恢复,在过去的一年中大量引进外来物种并造成外来
- )假设我们已经进入了航天时代,某高中学生组成的航天兴趣小组乘外星科学考察飞船到达了X星球(已知该星球与地球极其相似),他
- 下列说法中正确的是()A. 跳水运动员入水时的速度为瞬时速度B. 物体做单向直线运动时,其位移就是路程C. 凡轻小的物体
- 计算: .
- 19.填入下面文段空白处的词语,最恰当的一组是 ( )(3分) 智能互联是未来发展大势,
- 求值:tan10°+tan50°+tan10°tan50°=.
- 据有关资料介绍,儿童缺钙会得佝偻病,成年人缺钙会得软骨病,血液中也有少量钙,它对皮肤伤口血液的凝固起着重要作用;人体缺碘
- (7分)如图所示,底面积为100cm2,重10N的容器放在水面上,容器中装有2.5kg的水,水深20cm。求(1)距容器
- 根据打点计时器打出的纸带,我们可以不利用公式计算就能直接得到的物理量是( )A.时间间隔 B.位






 ,因为这违背了原理(规则)。
,因为这违背了原理(规则)。
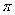 键 b.σ键 c.配位键 d.极性键
键 b.σ键 c.配位键 d.极性键


 ,从而实现对K+的定量测定。
,从而实现对K+的定量测定。 








