高考二轮复习知识点:化学研究方法与工业化学
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 实验探究题 | 详细信息 |
|
工业上制取硝酸铵的流程图如下,请回答下列问题:
|
|
| 2. 综合题 | 详细信息 | ||||||||||||||||||||
|
硫酸的年产量高低常用于衡量一个国家化工生产水平的高低.
|
|||||||||||||||||||||
| 3. 实验探究题 | 详细信息 |
|
根据题意填空:
|
|
| 4. 综合题 | 详细信息 |
|
工业上用氨催化氧化制硝酸
|
|
| 5. 实验探究题 | 详细信息 |
|
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解,易水解,可用作肥料、灭火剂、洗涤剂等。实验室制备氨基甲酸铵的反应如下:2NH3(g)+CO2(g)
 NH2 COONH4(s) △H<0,该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则水解生成碳酸铵或碳酸氢铵。某化学兴趣小组按下图装置进行如下实验: NH2 COONH4(s) △H<0,该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则水解生成碳酸铵或碳酸氢铵。某化学兴趣小组按下图装置进行如下实验:
步骤1:按图连接好实验装置,……………………….。 步骤2:在相应仪器中装入药品,其中1在三颈烧瓶中加入足量的氢氧化钠固体,在恒压滴液漏斗中装入浓氨水。 步骤3:滴加浓氨水并搅拌,调节反应速率,在反应器中得到产品。 …… 请回答下列问题:
|
|
| 6. 单选题 | 详细信息 |
|
下列化学用语对事实的表述错误的是( )
A . 硬脂酸与乙醇的酯化反应:C17H35COOH+C2H518OH
 C17H35COOC2H5+H218O
B . 常温时,0.1mol·L-1氨水的pH=11.1:NH3·H2O⇆NH4++OH-
C . 由Na和Cl形成离子键的过程: C17H35COOC2H5+H218O
B . 常温时,0.1mol·L-1氨水的pH=11.1:NH3·H2O⇆NH4++OH-
C . 由Na和Cl形成离子键的过程: |
|
| 7. 综合题 | 详细信息 |
|
合成氨是目前最有效工业固氮的方法,解决数亿人口生存问题。回答下列问题:
|
|
| 8. 实验探究题 | 详细信息 |
|
Li-SOCl2电池采用LiAlCl4的SOCl2溶液为电解质溶液,是目前比能量最高的化学电源,具有电压高.储存寿命长.工作温度范围宽.成本低等优点。
|
|
| 9. 单选题 | 详细信息 |
|
印刷电路板(PCB)是用腐蚀液将覆铜板上的部分铜腐蚀掉而制得。一种用FeCl3溶液制作PCB并将腐蚀后废液回收再生的流程如图:
下列说法错误的是( )
A . 腐蚀池中发生反应的化学方程式是:Cu+2FeCl3=CuCl2+2FeCl2
B . 腐蚀后的废液中,主要的金属阳离子有Fe3+、Cu2+、Fe2+
C . 置换池中发生的主要反应为:Fe+Cu2+=Cu+Fe2+和Fe+2Fe3+=3Fe2+
D . 再生池中加入酸化的H2O2 , 反应过程中pH降低
|
|
| 10. 综合题 | 详细信息 | ||||||||||||||||||||||
|
氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。
|
|||||||||||||||||||||||
- 宁夏吴忠市吴忠中学2018-2019学年高一上学期期末化学模拟试卷
- 北京市延庆区2019-2020学年高一下学期化学期末考试试卷
- 广西南宁市2020年高考理综-化学二模试卷
- 2016-2017学年浙江省湖州市高一下学期期中化学试卷
- 河北省邯郸市2017-2018学年高考理综-化学一模考试试卷
- 广东省梅州市2019-2020学年高二下学期化学期末考试试卷
- 2016-2017学年湖北省宜昌市部分示范高中联考高一下学期期中化学试卷
- 高中化学人教版(2019)选择性必修1第二章第三节化学反应的方向
- 吉林省辽源市田家炳高中2019-2020学年高二下学期化学6月月考试卷
- 高中化学鲁科版(2019)必修第二册 第3章第1节 认识有机化合物
- 甘肃省兰州市联片办学2019-2020学年高二上学期(文)化学期中考试试卷
- 2016-2017学年广西桂林市全州高中高一上学期期中化学试卷
- 图为黄河沿岸某城市示意图。读图回答下列问题。
- 已知各项均为正的数列为等比数列,;为等差数列的前n项和,. (1) 求和的通项公式; (2) 设,求.
- 图20是常见的厕所自动冲水装置原理图,水箱内有质量为0.4kg,体积为3×10-3m3的浮筒P,另有一厚度不计,质量为0
- 下列特色食品中,富含维生素的是()A.砀山苹果 B.淮南豆腐 C.巢湖白鱼
- If I _________, I will go to the tea party thisevening. A.i
- 2010年1月12日,海地发生7.3级地震,造成重大人员伤亡和财产损失。联合国秘书长潘基文紧急呼吁国际社会向海地提供援助
- 在用单摆测定重力加速度的实验中,下列说法正确的是( )A.测周期时,测得完成n次全振动所用时间为t,则周期为B.在
- 下表反映了甲午战争前中国洋纱输入的情况,由此可以推断,洋纱的输入()A.使传统土纱退出了中国市场 B.标志着中国
- 下列说法正确的是【 】A.用甲醛溶液浸泡海产品保鲜 B.微量元素是人体必需的营养素,多吃
- 如图2所示,以下成语与其物理知识相符的是( )A.凿壁偷光——光的折射
- Einstein liked Bose’s paper so much that he his own
- 均匀导线制成的单匝正方形闭合线框abcd,每边长为L,总电阻为R,总质量为m。将其置于磁感强度为B的水平匀强磁场上方h处
- I can hardly imagine Peter ______ across the Atlantic Ocean
- ,材料一:2008年8月8日晚8时08分第29届夏季奥运会在北京开幕,经过16天的精彩角逐,圆满完成各项赛事,于8月24
- 针对最近社会上出现的关于恢复“五一”长假的议论及个别地方也在考虑出台相关调整措施,2009年3月26日,国务院办公厅发出
- 阅读下面的文字,完成后面题目。(15分) 选择 武献卫 海啸来的毫无征兆。 监狱长海尔默面对突如其来的灾难显得惊慌失措,
- + ......
- 曲线上的点为切点的切线的倾斜角的取值范围是( )A. B. C. D.
- 右图是某兴趣小组设计的一套实验装置,装置足以维持 实验过程中小白鼠的生命活动。装置气密性良好。经数小时后,U形管A、B两
- Many people in this country eat _______________ as they act






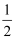 N2(g)+
N2(g)+  H2(g)
H2(g) 








