高考二轮复习知识点:离子浓度大小的比较1
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 多选题 | 详细信息 |
|
常温下,用0.10 mol·L-1盐酸分别滴定20.00 mL浓度均为0.10 mol·L-1 CH3COONa溶液和NaCN溶液,所得滴定曲线如右图(忽略体积变化)。下列说法正确的是( )
A . 溶液中阳离子的物质的量浓度之和:点②等于点③
B . 点①所示溶液中:c(CN-)+ c(HCN)=2c(Cl-)
C . 点②所示溶液中:c(Na+)> c(Cl-)> c(CH3COO-)> c(CH3COOH)
D . 点④所示溶液中:c(Na+)+ c(CH3COOH)+ c(H+)>0.10 mol·L-1
|
|
| 2. 多选题 | 详细信息 |
|
25 ℃时,NaCN溶液中CN-、HCN浓度所占分数(δ)随pH变化的关系如下图甲所示。向10 mL 0.01 mol·L-1 NaCN溶液中逐滴加入0.01 mol·L-1的盐酸,其pH变化曲线如下图乙所示[其中a点的坐标为(9.5,0.5)]。
甲 乙 下列溶液中的关系中一定正确的是( )
A . 图甲中pH=7的溶液:c(Cl-)=c(HCN)
B . 常温下,NaCN的水解平衡常数: K(NaCN)=10-4.5mol/L
C . 图乙中b点的溶液:c(CN-)>c(Cl-)>c(HCN)>c(OH-)>c(H+)
D . 图乙中c点的溶液:c(Na+)+c(H+)=c(HCN)+c(OH-)+c(CN-)
|
|
| 3. 多选题 | 详细信息 |
|
人体血液的pH通常在7.35-7.45之间的原因是血液中存在NaH2PO4-Na2HPO4等缓冲体系。常温下:Ka1(H3PO4)=7.6×10-3、Ka2(H3PO4)=6.3×10-8。下列指定溶液中微粒物质的量浓度关系正确的是( )
A . 0.1mol/L NaH2PO4溶液:2c(HPO42-)+3c(PO43-)>c(Na+)-c(H2PO4-)
B . 常温下,pH=7的NaH2PO4和Na2HPO4的混合溶液:c(Na+)>c(HPO42-)>c(H2PO4-)
C . 向10 mL0.1mol/L NaH2PO4溶液中加入5mL 0.4 mol/L NaOH溶液:c(H+)+3c(H3PO4)+2c(H2PO4-)+c(HPO42-)=c(OH-)
D . 物质的量浓度相等NaH2PO4和Na2HPO4溶液等体积混合:3[c(H2PO4-)+c(HPO42-)+c(PO43-)]=2c(Na+)
|
|
| 4. 多选题 | 详细信息 |
|
室温下用
 分别滴定 分别滴定  的盐酸和醋酸的曲线如图所示,下列说法正确的是( ) 的盐酸和醋酸的曲线如图所示,下列说法正确的是( )
A . Ⅰ表示的是滴定盐酸的曲线
B .
 时,两份溶液中: 时,两份溶液中:  C .
C .  时,两份溶液中: 时,两份溶液中:  D .
D .  时,醋酸溶液中: 时,醋酸溶液中: 
|
|
| 5. 综合题 | 详细信息 |
|
硒(Se)元素位于元素周期表第四周期第VIA族。请回答下列问题:
I.工业上用精炼铜的阳极泥(硒主要以CuSe形式存在,还含有少量Ag、Au)为原料与浓硫酸混合焙烧,将产生的SO2、SeO2混合气体用水吸收即可得Se固体。
|
|
| 6. 综合题 | 详细信息 |
|
烟气中SO2的大量排放给人类的生存环境造成了严重破坏,工业上通常采用以下三种方法实现烟气中硫的回收。
|
|
| 7. 综合题 | 详细信息 |
|
硫酸是最重要的化工产品之一,工业上若以硫黄为原料来制取硫酸,其反应原理如下:
S+O2 2SO2+O2 SO3+H2O=H2SO4 ③
|
|
| 8. 综合题 | 详细信息 |
|
甲醇可用于制造甲醛和农药,工业上可由碳的氧化物和氢气反应制得反应制得。
|
|
| 9. 综合题 | 详细信息 |
|
锑(Sb)广泛用于生产各种阻燃剂、陶瓷、半导体元件等领域,金属锑一般条
件下不与酸反应。以辉锑矿(主要成分为 Sb2S3 , 还含有 As2S5、PbS、CuO 和 SiO2等)为原料制备金属锑,其中一种工艺流程如下: 已知:①浸出液主要含 HCl 和 SbCl3 , 还含 SbCl5、CuCl2、AsCl3和 PbCl2等杂质。 ②25℃时,Ksp (CuS)=1.0×10 -36 , Ksp (PbS)=9.0×10 -29。 回答下列问题:
|
|
| 10. 综合题 | 详细信息 |
|
以软锰矿粉(主要含有MnO2 , 还含有少量的Fe2O3、Al2O3等杂质)为原料制备高纯MnO2的流程如下图所示:
已知:①常温下,Ksp[Fe(OH)3]=8.0×10-38 , Ksp[Al(OH)3]=4.0×10-34。 ②常温下,氢氧化物沉淀的条件:Al3+、Fe3+完全沉淀的pH分别为4.6、3.4;Mn2+开始沉淀的pH为8.1。 ③常温下,当溶液中金属离子的物质的量浓度小于或等于1×10-5 mol·L-1时,可视为该金属离子已被沉淀完全。
|
|
- 黑龙江省齐齐哈尔市2018-2019学年高考理综-化学一模考试试卷
- 福建省南平市2019-2020学年高一下学期化学期末考试试卷
- 2015-2016学年辽宁省营口市大石桥二中高二下学期期中化学试卷
- 2015-2016学年福建省南平市浦城县高一下学期期中化学试卷
- 2015-2016学年广西崇左市大新县民族高中高一上学期第一次月考化学试卷
- 2015-2016学年江苏省盐城市时杨中学高二下学期期中化学试卷
- 人教版化学高二选修6第四单元实验4-1纯净物与混合物性质的比较同步练习
- 广西南宁市“4N”高中联合体2018-2019学年高二下学期化学期末考试试卷
- 专题27:有机高分子材料
- 2016年江西省宜春市宜丰二中高考化学五模试卷
- 四川省绵阳市2019-2020学年高一下学期化学期末考试试卷
- 备考2018年高考化学二轮专题复习 专题十二:有机化合物
- 如图所示的是酶、激素、蛋白质、抗体四者关系。下列有关叙述,正确的是 ( ) A. 1 2 3 分别表示激素、酶、蛋白
- 如图所示,在空间四边形ABCD中,AD=BC=2,E,F分别是AB,CD的中点.若EF=,求AD,BC所成的角.
- 下列对组成细胞的分子的描述,不正确的是 ()。 A.激素、抗体、酶、载体蛋白发挥作用后均将失去生物活性 B.酪氨
- 分解因式: = .
- 某车间有技术工人 85 人,平均每天每人可加工甲种部件 16 个或乙种部件 10 个.两个甲种部件 和三个乙种部件配成一
- 等质量的两份锌粉a和b,分别加入过量的稀硫酸中,a中同时加入少量CuSO4,下列图中表示其产生H2总体积(V)与时间(t
- 每年五四青年节,青年们激情飞扬,用青春的活力、蓬勃的朝气来纪念五四运动,那么关于这一运动的说法正确的是() A.它是中国
- — You _____ stop me. — Even if you _____ it, I won’t allow
- 一只小昆虫从仰放的半球面形小碗内的最低点出发,沿碗壁向上缓慢爬行,在其滑落之前的爬行过程中的受力情况是( ) A.
- 在电场强度为E的匀强电场中,有一条与电场线平行的几何线,如图中虚线所示.几何线上有两个静止的小球A和B(均可视为质点),
- 下列哪些不是水对于人体的生理作用()A. 调节体温 B. 抵抗疾病 C. 运输营养物质 D. 运输代谢产物
- 关于平抛运动,下列说法正确的是( )A.是匀变速曲线运动 B.是非匀变速曲线运动
- 学习化学知识后,观察物质世界就要从化学视角看。下列对打火机主要燃料丁烷(C4H10)的看法不正确的是( ) A.从组
- 语言文字运用(24分) 下列各句中划线的熟语,使用恰当的一句是( )(3分) A.产业要发展,测试需先行,数字
- 近代以来,先进的中国人站在时代前列,探求救国救民的真理,推动了中国的近代化(现代化)进程。读图回答问题 ⑴请分别概述前
- 为庆祝新中国成立60周年,某导演筹拍一部电视政论片《建国初期的政治建设》。下列题材可以入选该片的有( )A.区域自
- 一个25 kg的小孩从高度为3.0 m的滑梯顶端由静止开始滑下,滑到底端时的速度2.0 m/s.取g=10 m/s2,关
- . --- Has your daughter finished writing the composition?
- 现有1200个氢原子被激发到量子数为4的能级上,若这些受激氢原子最后都回到基态,则在此过程中发出的光子总数是多少?假定处
- ⑴图中给出的是用螺旋测微器测量一小钢球的直径时的示数,此读数应是 毫米.⑵有一游标卡尺,主尺的最小分度是1




 CuSO4+SeO2↑+3SO2↑+4H2O
CuSO4+SeO2↑+3SO2↑+4H2O (aq)⇌Ag2SeO4(s)+SO
(aq)⇌Ag2SeO4(s)+SO 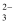 的还原过程。已知SeO
的还原过程。已知SeO  S(1)+2CO2(g)
S(1)+2CO2(g)
 S(1)+2CO2(g),平衡时SO2的转化率α(SO2)与投料比的比值[
S(1)+2CO2(g),平衡时SO2的转化率α(SO2)与投料比的比值[  =y]、温度T的关系如图所示。则平衡时,CO的转化率:NM(填“>”、“<”或“=”,下同),逆反应速率:NP。
=y]、温度T的关系如图所示。则平衡时,CO的转化率:NM(填“>”、“<”或“=”,下同),逆反应速率:NP。


 =
=
 SO2 ①
SO2 ①  2SO3 ②
2SO3 ② 



 )+c(OH-)
)+c(OH-)






