高考二轮复习知识点:常用仪器及其使用4
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
某兴趣小组用铬铁矿[Fe(CrO2)2]制备K2Cr2O7晶体,流程如下:
已知:4Fe (CrO2)2 + 10Na2CO3+7O2 2H++2CrO 相关物质的溶解度随温度变化如下图。 请回答:
|
|
| 2. 综合题 | 详细信息 |
|
氧化石墨烯具有稳定的网状结构,在能源、材料等领域有着重要的应用前景,通过氧化剥离石墨制备氧化石墨烯的一种方法如下(装置如图所示):
I.将浓H2SO4、NaNO3、石墨粉末在c中混合,置于冰水浴中。剧烈搅拌下,分批缓慢加入KMnO4粉末,塞好瓶口。 II.转至油浴中,35℃搅拌1小时,缓慢滴加一定量的蒸馏水。升温至98℃并保持1小时。 III.转移至大烧杯中,静置冷却至室温。加入大量蒸馏水,而后滴加H2O2至悬浊液由紫色变为土黄色。 IV.离心分离,稀盐酸洗涤沉淀。 V.蒸馏水洗涤沉淀。 VI.冷冻干燥,得到土黄色的氧化石墨烯。 回答下列问题:
|
|
| 3. 实验探究题 | 详细信息 |
|
化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献,某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备NaHCO3 , 进一步处理得到产品Na2CO3和NH4Cl,实验流程如图:
回答下列问题:
|
|
| 4. 综合题 | 详细信息 | ||||||||||||||||||||||||||||||||||||||||
|
碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原料制备碳酸钠,并测定产品中少量碳酸氢钠的含量,过程如下:
步骤I. ①称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中; ②移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用 ③在上述锥形瓶中再加入2滴指示剂N,继续用 ④平行测定三次, 已知:(i)当温度超过35℃时, (ii)相关盐在不同温度下的溶解度表
回答下列问题:
|
|||||||||||||||||||||||||||||||||||||||||
| 5. 实验探究题 | 详细信息 |
|
胆矾(
 )易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的 )易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的  (杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题: (杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:
|
|
| 6. 实验探究题 | 详细信息 | ||||||
 是很好的氯化剂,实验室用如图装置(夹持仪器已省略)制备高纯 是很好的氯化剂,实验室用如图装置(夹持仪器已省略)制备高纯  。已知: 。已知: ① ②常压下, ③ 请回答:
|
|||||||
| 7. 单选题 | 详细信息 | |||||||||||||||
|
下列实验对应的结论正确的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 8. 单选题 | 详细信息 |
|
X为含Cu2+的配合物。实验室制备X的一种方法如图。
下列说法不正确的是( )
A . ①中发生反应:Cu2++2NH3·H2O=Cu(OH)2↓+2NH
 B . 在①和②中,氨水参与反应的微粒相同
C . X中所含阴离子是SO
B . 在①和②中,氨水参与反应的微粒相同
C . X中所含阴离子是SO D . X的析出利用了其在乙醇中的溶解度小于在水中的溶解度
D . X的析出利用了其在乙醇中的溶解度小于在水中的溶解度
|
|
| 9. 单选题 | 详细信息 | |||||||||||||||
|
完成下列实验所选择的装置正确的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 10. 单选题 | 详细信息 | ||||||||||||||||||||
|
为完成下列各组实验,所选玻璃仪器和试剂均准确、完整的是(不考虑存放试剂的容器)( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
- 2015年四川省自贡市荣县高考化学模拟试卷(6月份)
- 内蒙古自治区呼伦贝尔市阿荣旗第一中学2019-2020学年高二下学期化学期末考试试卷
- 2016-2017学年北京市昌平区临川育人学校高二上学期期末化学试卷
- 人教版化学高二选修5第三章第四节有机合成同步练习
- 广东省华附、省实、广雅、深中2018-2019学年高三上学期理综-化学期末考试试卷
- 专题19:原子结构与性质
- 2016-2017学年广东省清远市清城区高三上学期期末化学试卷(A卷)
- 2016-2017学年江苏省宿迁市沭阳县高一上学期期中化学试卷
- 湖南省益阳市桃江县2019-2020学年高二下学期化学期末考试试卷
- 山东省德州市2020年高考化学一模试卷
- 2020高考化学常考知识点专练 09:物质结构与性质
- 河北省2020年高考理综-化学一模试卷(全国Ⅰ卷)
- 1861年开始的一场内战和一次改革极大地推动了世界历史的发展,它们是( ) A.美国内战和戊戌变法
- 小明、志刚在观看电影《哈利、波特》时,高谈阔论,无所顾忌,受到周围人的指责。这说明( )①尊重他人才能赢得他人的尊
- 小明同学在做实验室里用加热高锰酸钾的方法制氧气,实验结束后,发现试管炸裂,试帮她分析一下造成此后果的原因可能有(至少答三
- 已知X、Y、Z、M、W、R是前四周期中的六种元素。X元素原子形成的离子是一个质子,Y原子的价电子构型为2s22p2,Z的
- 阅读材料,结合所学知识回答。请回答: (1)据表中甲、乙内容,概述“欧洲旧思想”与“中国旧思想”的异同点。 (2)据表中
- 我国南海底蕴藏着丰富的锰结核﹣﹣含有锰,铁,铜等金属的矿物.已知锰原子的核内质子数为25,相对原子质量为55,则锰原子的
- 在日常生活中,为保持良好情绪,可以采用( )A.找知心朋友大吵一场B.如果有车,可以到高速公路上开快车宣泄自己的情绪
- 阅读下列材料,回答问题。 温家宝总理在2010年的政府工作报告中指出:“我们所做的一切都是要让人民生活得更加幸福、更有尊
- 我国20世纪90年代改革开放的重点和标志( ) A、设立深圳为经济特区
- (8分)透明光学材料制成的棱镜的正截面为等腰直角三角形,其折射率为n=。一束波长为564 nm的单色光与底面平行射入棱镜
- 生物技术已成为解决人口、资源、能源、食物和环境等全球性问题的重要技术。下列说法错误的是 A.制作酸奶的主要步骤:①器具原
- It was 1961 and was in the fifth grade. My marks in school w
- 历史学爱汤因比认为,英国是近代代议制民主的先驱。这是英国“光荣革命”后产生了对后世影响巨大的 A.第一部成文宪法
- 如图,在矩形ABCD中,AB=,BC=2,点E为BC的中点,点F在边CD上,若·=,则·=.
- 分子运动的速度与温度有关,所以水在0 ℃时,它的 A.分子的运动速度为零 B.内能为零 C.分子的运动速度不为零,但内能
- —I’m going to play soccer now. —________. It’s raining heavi
- ---_______ do you write toyour e-friends? --- Almost twice
- 图19-2-9中互相垂直的两条虚线MN及M′N′表示两种介质的分界面及其法线;实线表示一条入射光线及其反射光线和折射光线
- You can use your Business Telecard International at any card
- 作文(50分)题目:“总有一种记忆值得珍藏”人生是一次远航。起锚时的林林总总,那岸上的斑驳,那港湾的纷杂,深深烙进你的心

 8Na2CrO4 +4NaFeO2+10CO2
8Na2CrO4 +4NaFeO2+10CO2
 Cr2O
Cr2O  +H2O
+H2O


 B.
B.  C.
C.  D.
D.  E.
E. 

 的制备
的制备 步骤Ⅱ.产品中
步骤Ⅱ.产品中  含量测定
含量测定 盐酸标准溶液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸
盐酸标准溶液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸  ;
; ;
; 平均值为22.45,
平均值为22.45,  平均值为23.51。
平均值为23.51。 开始分解。
开始分解。





 ,冷却后用
,冷却后用  调
调  为3.5~4,再煮沸
为3.5~4,再煮沸  ,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、、乙醇洗涤、,得到胆矾。其中,控制溶液
,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、、乙醇洗涤、,得到胆矾。其中,控制溶液  ,加入胆矾后总质量为
,加入胆矾后总质量为  ,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为
,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为  。根据实验数据,胆矾分子中结晶水的个数为(写表达式)。
。根据实验数据,胆矾分子中结晶水的个数为(写表达式)。
 ,合适反应温度为
,合适反应温度为  ;副反应:
;副反应:  。
。 沸点
沸点  ,熔点
,熔点  ;
;  。
。 ,
,  在
在  中的溶解度远大于其在水中的溶解度。
中的溶解度远大于其在水中的溶解度。

 的比例
的比例 。反应停止后,温度保持不变,为减少产品中的
。反应停止后,温度保持不变,为减少产品中的  萃取分液,经气化重新得到。
萃取分液,经气化重新得到。  溶液及一定量的稀
溶液及一定量的稀 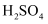 ,充分反应。用标准
,充分反应。用标准  溶液滴定(滴定Ⅰ);再以酚酞为指示剂,用标准
溶液滴定(滴定Ⅰ);再以酚酞为指示剂,用标准  溶液滴定(滴定Ⅱ)。已知产生
溶液滴定(滴定Ⅱ)。已知产生  的反应(不考虑
的反应(不考虑 







 (
(  均以
均以  N2O4(g)(无色)
N2O4(g)(无色)




 标准溶液
标准溶液 溶液制取无水
溶液制取无水


 含量
含量 溶液、
溶液、 溶液、浓NaOH溶液
溶液、浓NaOH溶液 和
和 对
对 分解的催化效果
分解的催化效果 溶液、
溶液、


