【备考2024年】从巩固到提高 高考化学二轮微专题08 铜及其化合物
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
将铜加入一定量稀硫酸和过氧化氢混合溶液中,充分反应后,溶液呈蓝色,有无色气体产生;若还发现容器底部有少量固体,则该固体可能是( )
A . Cu
B . S
C . CuS
D . Cu2S
|
|
| 2. 单选题 | 详细信息 |
|
某化学兴趣小组进行有关Cu、硝酸、硫酸化学性质的实验,实验过程如图所示.下列有关说法正确的是
( )
A . ①中溶液呈蓝色,试管口有红棕色气体产生,稀硝酸被还原为NO2
B . ③中反应的化学方程式:3Cu+Cu(NO3)2+4H2SO4=4CuSO4+2NO↑+4H2O
C . ③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸强
D . 由上述实验可知:Cu在常温下既可与稀硝酸反应,也可与稀硫酸反应
|
|
| 3. 单选题 | 详细信息 |
|
铜与浓硫酸反应的装置如图所示。下列描述合理的是( )
A . 反应过程中,试管Ⅰ中出现灰黑色固体是Cu2O
B . 反应结束后,为观察溶液颜色需向试管Ⅰ中加入水
C . 若试管Ⅱ盛放紫色石蕊溶液,可观察到溶液由紫色褪为无色
D . 为验证气体产物具有还原性,试管Ⅱ盛放酸性KMnO4溶液
|
|
| 4. 单选题 | 详细信息 | ||||||||||||||
|
用下图装置探究铜与硝酸的反应,实验记录如下:
下列说法错误的是( )
A . ①中反应的化学方程式是Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
B . ②中注射器内剩余的水被“吸入”试管的原因可能是NO2与H2O反应导致压强减小
C . ③中的实验现象能证明②中Cu与硝酸反应生成了NO
D . 待②中反应停止后,向试管内滴加少量稀硫酸,有气体产生
|
|||||||||||||||
| 5. 单选题 | 详细信息 | ||||||||||||||||||||
|
10℃时,分别向4支小试管中滴加8滴1mol/LCuSO4溶液,再分别向其中滴加2mol/LNaOH溶液,边滴加边振荡,实验数据及现象如下表:
取浅绿色沉淀用蒸馏水反复洗涤,加入稀盐酸完全溶解,再加入适量BaCl2溶液,产生大量白色沉淀。取蓝色沉淀重复上述实验,无白色沉淀。经检验,试管3、4中黑色沉淀中含有CuO。 下列说法错误的是( )
A . 由实验现象可知浅绿色沉淀中可能含有碱式硫酸铜
B . CuSO4溶液与NaOH溶液反应时,其相对量不同可以得到不同的产物
C . 试管3、4中的固体在加热过程中发生了反应:Cu(OH)2
 CuO+H2O
D . 取浅绿色沉淀再滴加适量NaOH溶液后加热仍不会变黑 CuO+H2O
D . 取浅绿色沉淀再滴加适量NaOH溶液后加热仍不会变黑
|
|||||||||||||||||||||
| 6. 单选题 | 详细信息 |
 的结构式如下图, 的结构式如下图, 时 时 会发生分解.下列推测合理的是( ) 会发生分解.下列推测合理的是( )
A .
 是离子晶体,熔点高,硬度大
B . 是离子晶体,熔点高,硬度大
B .  加热可能生成 加热可能生成 C .
C .  分解的产物可能为 分解的产物可能为 和 和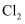 , 同类化合物 , 同类化合物 分解温度更高
D . 分解温度更高
D .  溶于浓盐酸呈绿色,加水稀释溶液变蓝色,是因为 溶于浓盐酸呈绿色,加水稀释溶液变蓝色,是因为 浓度减小 浓度减小
|
|
| 7. 单选题 | 详细信息 |
|
碱式氯化铜[CuaClb(OH)c·xH2O]是一种重要的无机杀虫剂,它的制备流程如下,下列有关说法正确的是( )
A . FeCl3的作用是增强盐酸的氧化性
B . 加入少量CuO目的是为了除去Fe3+
C . 石灰乳可用纯碱代替
D . 若制备1mol的CuCl2 , 理论上消耗11.2L空气
|
|
| 8. 单选题 | 详细信息 |
|
青铜器在古时被称为“金”或“吉金”,是红铜与锡、铅等的合金。铜锈大多呈青绿色,主要含有Cu2(OH)3Cl和Cu2(OH)2CO3。下列说法错误的是( )
A . 青铜器中锡、铅对铜有保护作用
B . 青铜的熔点低于纯铜
C . 可用FeCl3溶液清除青铜器的铜锈
D . 古时冶炼铸造青铜器涉及化学变化
|
|
| 9. 实验探究题 | 详细信息 |
|
氯化亚铜(CuCl)是一种非常重要的化工原料。查阅资料可知:CuCl为白色固体,微溶于水,不溶于乙醇,在空气中能被迅速氧化。回答下列问题:
|
|
| 10. 实验探究题 | 详细信息 | |||||||||||||||||||||||||||||||
某小组探究 |
||||||||||||||||||||||||||||||||
预测 | 反应的离子方程式 | 实验现象 |
1 |
| 生成绿色沉淀 |
2 |
| ____ |
3 |
| 生成红色沉淀 |
4 | ____ | 生成白色沉淀( |
-
(1) 预测2中的实验现象为。
-
(2) 预测4中反应的离子方程式为。
-
(3) 【实验探究】
实验1
 溶液
溶液
立即生成橙黄色沉淀,
 后沉淀颜色变浅并伴有少量白色沉淀产生,振荡
后沉淀颜色变浅并伴有少量白色沉淀产生,振荡 沉淀全部变为白色
沉淀全部变为白色 溶液
溶液为证明实验1中白色沉淀为
 , 设计实验如下。
, 设计实验如下。
①已知
 在水中呈无色。实验2总反应的离子方程式为。
在水中呈无色。实验2总反应的离子方程式为。②为证明深蓝色溶液中含有
 , 进一步实验所需的试剂为(填化学式)。
, 进一步实验所需的试剂为(填化学式)。 -
(4) 【进一步探究】查阅资料获知橙黄色沉淀可能为
 。在实验1获得橙黄色沉淀后,立即离心分离并洗涤。为探究其组成进行如下实验。
。在实验1获得橙黄色沉淀后,立即离心分离并洗涤。为探究其组成进行如下实验。
离心分离的目的是加快过滤速度,防止。
-
(5) 已知
 。实验3能否证明橙黄色沉淀中含有
。实验3能否证明橙黄色沉淀中含有 和
和 , 结合实验现象做出判断并说明理由。
, 结合实验现象做出判断并说明理由。
-
(6) 橙黄色沉淀转化为
 的原因可能是
的原因可能是 提高了
提高了 的氧化性,进行如下实验(已知装置中物质氧化性与还原性强弱差异越大,电压越大)。
的氧化性,进行如下实验(已知装置中物质氧化性与还原性强弱差异越大,电压越大)。实验4
装置
试剂a
试剂b
电压表读数

 溶液
溶液 溶液
溶液
 溶液
溶液X

①表中X为。
②能证实实验结论的实验现象为。
【解释和结论】综上,
 与
与 发生复分解反应速率较快,发生氧化还原反应趋势更大。
发生复分解反应速率较快,发生氧化还原反应趋势更大。
- 2016-2017学年山东省临沂市蒙阴一中高二上学期期中化学试卷
- 广东省潮州市潮安区2019-2020学年高一下学期化学期末考试试卷
- 2017年山西省重点中学协作体高考化学模拟试卷(一)
- 2016-2017学年河南省河南大学荆紫关附中 高二上学期开学化学试卷
- 陕西省渭南市三贤中学2019-2020学年高一下学期化学期中考试试卷
- 第3讲:氧化还原反应
- 2015-2016学年山东省德州市跃华学校高二下学期期中化学试卷
- 安徽省合肥市庐江县2019-2020学年高一下学期化学期末考试试卷
- 2015-2016学年安徽省淮南市示范高中五校高一上学期第一次月考化学试卷
- 2015-2016学年湖北省襄阳市枣阳市育才学校高一下学期期中化学试卷
- 河北省保定市2020年高考化学一模试卷(全国I卷)
- 安徽省宣城市2018-2019学年高考化学二模考试试卷
- 向装有等量水的A、B、C烧杯中加入10g、20g、25g的NaNO3固体,充分溶解后,现象如图一所示:(1)A、B、C烧
- 为了探究受到空气阻力时,物体运动速度随时间的变化规律,某同学采用了“加速度与物体质量、物体受力关系”的实验装置(如图所示
- 下列地区属于人口稀疏地区的是 ①南美洲东部 ②我国东南部沿海 ③加拿大 ④阿拉伯半岛 ⑤西欧 ⑥亚马孙平原
- ___exceptions, the rule may stand. A. Allow for
- WelcomeDaming _______ our city. A. to B.fo
- At last, we found ourselves in a pleasant park with trees pr
- 公元一世纪时,罗马博物学家普林尼在其著名《自然史》中说:“虽然铁的种类很多,但没有一种能和中国来的钢相媲美。”中国炼钢业
- 下列各种材料中,不能用来作为观察叶绿体的实验材料的是( ) A葫芦藓叶片 B。胡萝卜根的横切
- 春天来了,带着无限的娇美。小草已露出嫩芽,花朵也含苞待放,我们怎么能错过这大好的时光,不去旅游?假定你是学校学生会主席李
- (2013·安徽)“鞍山轧钢开红花,解放汽车跑中华”。新中国自主生产出第一批解放牌汽车是在() A.土地革命时期
- 书面表达 假如你是Simon, 想推荐Mary获今年的优秀学生奖 (Good Student Award), 根据下面的
- (泉州中考)小勇利用如图所示的装置探究“平面镜成像时像与物的关系”的实验:(1)用玻璃板代替平面镜,主要是利用玻璃板透明
- 5.下列各句中,没有语病的一句是(3分) A.由于自贸区致力于营造国际化、法治化、市场化的营商环境,使更多金融、物流和I
- 将镁粉和铝粉的混合物7.2g与足量的氧气充分反应,得到的氧化物质量可能为() A.10.6g B.12.0g
- Nothing is more pleasing and romantic as flowers in the bedr
- 关于转基因技术的应用,不正确的是( )A.可以将抗病虫害、抗除草剂等基因转入农作物使其具有相应的抗性B. 可以使
- 泰安市某校初二(1)班同学准备举行“1919—l949 年历史图片展”。小军找到一幅《中国军队血战卢沟桥》的图片,你认为
- The sun was shining brightly, _____ everything there _____ m
- 指出含有通假字的一组 A 年二十已下 B 民每十丁遣一兵 C 结拜羽林郎 D 良家子至者三万余骑
- 根尖结构中吸收水分的主要部位是( ) A、根冠 B、分生区 C、伸长区 D、成熟区








 溶液和
溶液和 溶液的反应物,开展如下活动。
溶液的反应物,开展如下活动。





