山东省济宁市兖州区2022-2023学年高二上学期期中考试化学试题
山东省济宁市兖州区2022-2023学年高二上学期期中考试化学试题
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
向某密闭容器中加入0.3 mol A、0.1 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图甲所示[
 阶段c(B)未画出]。图乙为改变条件平衡体系中化学反应速率随时间变化的情况, 阶段c(B)未画出]。图乙为改变条件平衡体系中化学反应速率随时间变化的情况, 、 、 、 、 、 、 时刻均改变一种条件,且改变的条件均不同。已知 时刻均改变一种条件,且改变的条件均不同。已知 时刻为使用催化剂。下列说法正确的是( ) 时刻为使用催化剂。下列说法正确的是( )
A . B的起始物质的量为0.02 mol
B . 若
 s,生成物C在 s,生成物C在 段的化学反应速率为 段的化学反应速率为 C .
C .  时刻改变的条件可能为降温
D . 时刻改变的条件可能为降温
D .  时刻改变的条件可能为充入0.1 mol B 时刻改变的条件可能为充入0.1 mol B
|
|
| 2. 实验探究题 | 详细信息 | ||||||||||||||||||||||||||||||||
|
某小组利用
 溶液与用硫酸酸化的 溶液与用硫酸酸化的 溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀并开始计时。该小组设计了如下方案: 溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀并开始计时。该小组设计了如下方案:
|
|||||||||||||||||||||||||||||||||
| 3. 单选题 | 详细信息 |
|
向纯水中加入少量下列物质或改变下列条件,能促进水的电离,并能使溶液中c(OH-)>c(H+)的是( )
A . NaHSO4固体
B . 将水加热煮沸
C . NaClO固体
D . 氨气
|
|
| 4. 单选题 | 详细信息 |
从科技前沿到日常生活,化学无处不在。下列说法错误的是( )
A . 我国首次在实验室实现了二氧化碳到淀粉的合成,生物酶催化剂的使用改变了反应历程
B . 神舟十三号升空时,火箭尾部喷射的气体呈红棕色是因为部分助燃剂N2O4转化为NO2
C . 明矾与高铁酸钾均可作水处理剂,两者处理水的原理相同
D . NH4Cl溶液可作焊接金属的除锈剂
|
|
| 5. 单选题 | 详细信息 |
已知某容器中存在反应,
|
|
| 6. 单选题 | 详细信息 |
下列说法正确的是( )
A . 若反应
 在常温下能自发进行,则该反应的 在常温下能自发进行,则该反应的 B . 强电解质溶液的导电能力一定比弱电解质溶液强
C . 其他条件不变,升高温度,一定增大活化分子百分数,但不一定加快反应速率
D . 配置
B . 强电解质溶液的导电能力一定比弱电解质溶液强
C . 其他条件不变,升高温度,一定增大活化分子百分数,但不一定加快反应速率
D . 配置 溶液时,为了加快溶解,可在热水中溶解再冷却 溶液时,为了加快溶解,可在热水中溶解再冷却
|
|
| 7. 单选题 | 详细信息 |
将一定量纯净的氨基甲酸铵置于密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:H2NCOONH4(s) |
|
| 8. 单选题 | 详细信息 | ||||||||
25℃时部分电解质的电离平衡常数数据如下。
已知H2R=H++HR- , HR-
A . NaHR溶液中既存在HR-的电离也存在HR-的水解
B . 等浓度溶液的pH:Na2CO3>NaClO>CH3COONa
C . 向NaClO溶液中通入少量CO2 , 漂白性增强的原因是ClO-+CO2+H2O=HClO+HCO
 D . 等浓度的NaClO和NaHCO3混合溶液中存在c(HClO)+c(ClO-)=c(HCO
D . 等浓度的NaClO和NaHCO3混合溶液中存在c(HClO)+c(ClO-)=c(HCO )+c(CO )+c(CO )+c(H2CO3) )+c(H2CO3)
|
|||||||||
| 9. 单选题 | 详细信息 |
液氨与水相似,存在着微弱的电离:2NH3
|
|
| 10. 单选题 | 详细信息 |
已知:①CH3OH的燃烧热为 |
|
高中化学 试卷推荐
- 人教版高中化学选修五 第四章 第一节 油 脂 同步练习
- 2016-2017学年福建省泉州市惠南中学高一上学期期中化学试卷
- 新疆维吾尔自治区生产建设兵团第一师高级中学2018-2019学年高一上学期化学期末考试试卷
- 2015-2016学年陕西省宝鸡市金台区高一下学期期中化学试卷
- 2020高考化学常考知识点专练 06:电池
- 2016-2017学年江西省宜春三中高二上学期期中化学试卷
- 人教高中化学一轮复习:专题5常见的金属元素
- 2015-2016学年山东省枣庄市滕州十一中高三上学期期末化学模拟试卷(四)
- 备考2018年高考化学一轮基础复习:专题32 定量实验和化学实验的设计与评价
- 2015-2016学年江苏省徐州市高二上学期期末化学试卷
- 广东省惠州市2018-2019学年高考化学4月模拟考试试卷
- 2016-2017学年福建省龙岩市四校联考高二上学期期中化学试卷
最近更新
- 科学研究需要进行实验,得到事实,并在此基础上进行必要的推理。因此,在学习科学过程中我们需要区分事实与推论。则关于表述:①
- _____he _______ a round face ? Sorry , Idon’t know him .
- 根据现代生物进化理论,下列说法正确的是 A.自然选择决定了生物变异和进化的方向 B.生物进化的实质是种群基因
- 一块完整的骨属于组织。( )
- 下表是某同学在做几个实验时所列举的实验材料和实验条件等相关内容,请据表回答下列问题: 组别 材料 实验条件 观察内容 A
- B London: It's well known that Charles Darwin's fam
- 有下列各数,0.01,10,-6.67,,0,-(-3),,,其中属于非负整数的共有A.1个 B.2个 C.3个D.4个
- 新中国成立前,中国内曾多次出现右倾错误,给中国革命造成巨大损失。所谓右倾是指政治思想上,认识落后于实际,不能随变化了的客
- 根据对宁波市相关的市场物价调研,预计进入夏季后的某一段时间,某批发市场内的甲种蔬菜的销售利润y1(千元)与进货量x(吨)
- 下列说法中正确的是 A、凡是放热反应都是自发的,吸热反应都是非自发的 B、自发反应一定是熵增大,非自发反应一定是熵减小
- 下图是表示某种生物个体内的三个正在进行分裂的细胞,请据图回答下列问题(1)判断三图各属于时期:甲图表示_________
- 下列实验操作正确的是
- 数列{an}的前n项和为Sn,已知an=5Sn-3(n∈N+),求an的通项公式.
- 下列词语中,没有错别字的一组是 ()A.隐秘黯然失色独当一面化干戈为玉帛B.涵养合盘托出惺惺相惜反其道而行之C.鼓噪出神
- “雨霁天晴,万紫千红增特色;凤鸣莺啭,三通两制促和平。”这副对联最早可能出现于20世纪 A.50
- 下列除垢或除污过程中利用乳化作用的是( ) A.自来水洗手 B.食醋除水垢 C.汽油除油污 D.洗洁精除油污
- 有的花并不结果,如黄瓜,南瓜,丝瓜的花多半都不会结果,解释这种现象。
- 有关旅游可持续发展的目标的叙述,正确的有() ①全面实现生态旅游 ②促进旅游的公平发展 ③改善旅游接待地的生活质量 ④
- 一个平行板电容器,使它每板电荷量从Q1=30×10-6 C增加到Q2=36×10-6 C时,两板间的电势差从U1=10
- 2010年9月5日,新华网载文指出,药品定价,不仅关系到药品生产企业的生存和发展,也是近年来社会关注的热点问题。科学、合



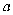
 , 忽略混合前后溶液体积的微小变化,这段时间内平均反应速率
, 忽略混合前后溶液体积的微小变化,这段时间内平均反应速率 。
。
 氧化为
氧化为 逸出,该反应的离子方程式为,为了观察到实验现象从而判断反应的快慢,
逸出,该反应的离子方程式为,为了观察到实验现象从而判断反应的快慢, 。
。
 时间内速率变快除反应放热温度升高外还有其他原因,若想验证这一原因,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择最合理的试剂是____(填字母)。
时间内速率变快除反应放热温度升高外还有其他原因,若想验证这一原因,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择最合理的试剂是____(填字母)。

 ,
, 
 。下列说法错误的是( )
。下列说法错误的是( )
 , 各种物质的物质的量浓度均增大
, 各种物质的物质的量浓度均增大 2NH3(g)+CO2(g)。能判断该反应已经达到化学平衡的是( )
2NH3(g)+CO2(g)。能判断该反应已经达到化学平衡的是( ) H++R2-。下列说法错误的是( )
H++R2-。下列说法错误的是( ) +
+ 。-50℃时,两种离子的平衡浓度均为1×10-15mol/L,下列有关液氨的离子积及其电离平衡的叙述中错误的是( )
。-50℃时,两种离子的平衡浓度均为1×10-15mol/L,下列有关液氨的离子积及其电离平衡的叙述中错误的是( )
 ;
; ;
;







