2015-2016学年广西桂林市逸仙中学高二下学期期中化学试卷
2015-2016学年广西桂林市逸仙中学高二下学期期中化学试卷
教材科目:化学
试卷分类:高二下学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高二下学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
在一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g)⇌H2(g)+I2(g),2s时生成0.1mol H2 , 则以HI表示该时段的化学反应速率是( )
A . 0.05 mol•Lˉ1•sˉ1
B . 0.1 mol•Lˉ1•sˉ1
C . 0.2 mol•Lˉ1•sˉ1
D . 0.8 mol•Lˉ1•sˉ1
|
|
| 2. 单选题 | 详细信息 |
|
下列物质的水溶液因水解呈碱性的是( )
A . Na2CO3
B . NaOH
C . HCl
D . AlCl3
|
|
| 3. 单选题 | 详细信息 |
|
关于常温下pH=11的氨水和氢氧化钠溶液,下列说法正确的是( )
A . 氨水溶液的浓度大于氢氧化钠溶液
B . NH3•H2O的电离方程式:NH3•H2O=NH4++OH﹣
C . c(NH3•H2O)+c(NH4+)=0.001 mol•Lˉ1
D . 往两溶液中加入盐酸恰好中和,则反应后溶液的pH值相同
|
|
| 4. 单选题 | 详细信息 |
|
COCl2(g)⇌CO(g)+Cl2(g);△H>0.当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A . ①②④
B . ①④⑥
C . ②③⑤
D . ③⑤⑥
|
|
| 5. 单选题 | 详细信息 |
|
用3g块状大理石与30mL 3mol/L盐酸反应制取CO2气体,若要增大反应速率,可采取的措施是( )
①再加入30mL 3mol/L盐酸 ②改用30mL 6mol/L盐酸 ③改用3g粉末状大理石 ④适当升高温度.
A . ①②④
B . ②③④
C . ①③④
D . ①②③
|
|
| 6. 单选题 | 详细信息 |
|
25℃、101kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( )
A . 2H2(g)+O2(g)═2H2O(1)△H=﹣285.8kJ/mol
B . 2H2(g)+O2(g)═2H2O(1)△H=+571.6kJ/mol
C . 2H2(g)+O2(g)═2H2O(g)△H=﹣571.6kJ/mol
D . H2(g)+
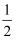 O2(g)═H2O(1)△H=﹣285.8kJ/mol O2(g)═H2O(1)△H=﹣285.8kJ/mol
|
|
| 7. 单选题 | 详细信息 |
|
关于NaHCO3溶液,下列表述不正确的是( )
A . c(Na+)=c(HCO3﹣)+c(CO32﹣)+c(H2CO3)
B . c(Na+)+c(H+)=c(HCO3﹣)+c(CO32﹣)+c(OH﹣)
C . HCO3﹣的水解程度大于HCO3﹣的电离程度
D . c(H+)+c(H2CO3)=c(OH﹣)+c(CO32﹣)
|
|
| 8. 单选题 | 详细信息 |
|
高温下,某反应达平衡,平衡常数
 .恒容时,温度升高,H2浓度减小.下列说法正确的是( ) .恒容时,温度升高,H2浓度减小.下列说法正确的是( )
A . 该反应的焓变为正值
B . 恒温恒容下,增大压强,H2浓度一定减小
C . 升高温度,逆反应速率减小
D . 该反应的化学方程式为CO+H2O⇌CO2+H2
|
|
| 9. 单选题 | 详细信息 |
|
在一个不传热的固定容积的密闭容器中发生可逆反应:mA(g)+nB(g)⇌pC(g)+qD(g),当m、n、p、q为任意整数(不为零)时,不能说明达到平衡状态的标志是( )
A . A的百分含量不再改变
B . 各组分的浓度不再改变
C . 反应速率υA:υB:υC:υD=m:n:p:q
D . 单位时间内m mol A断键发生反应,同时p mol C也断键发生反应
|
|
| 10. 单选题 | 详细信息 |
|
25℃时,由水电离出c(OH﹣)=1×10﹣11mol/L 的溶液中,一定能大量共存的离子组是( )
A . Al3+、NH4+、Cl﹣、CO32﹣
B . Na+、CH3COO﹣、K+、HCO3﹣
C . Fe2+、Cl﹣、Na+、NO3﹣
D . K+、I﹣、Cl﹣、Rb+
|
|
高中化学 试卷推荐
- 四川省遂宁市高中2016-2017学年高一下学期化学期末考试试卷
- 高中化学鲁科版(2019)选择性必修2 第1章第2节 原子结构与元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.1金属矿物的开发利用课时作业
- 2015-2016学年河北省邢台市高一上学期期末化学试卷
- 内蒙古呼和浩特市2017-2018学年高考理综-化学二模考试试卷
- 山东省菏泽市2016-2017学年高一上学期化学期末考试试卷(B卷)
- 北京市西城区2017-2018学年高考理综-化学二模考试试卷
- 2015年河南河北山西三省高考化学考前模拟试卷
- 浙江省嘉兴市2018-2019学年高一下学期化学期末考试试卷
- 2015-2016学年吉林省延边州汪清六中高二下学期期中化学试卷
- 河南省郑州市2016-2017学年高一下学期化学期末考试试卷
- 江西省上饶市横峰中学2020年高考化学模拟试卷
最近更新
- 将函数的图象先向左平移个单位长度,再把横坐标伸长到原来的倍,纵坐标不变。所得到的曲线对应的函数解析式是
- 镓元素的相关信息如图.下列有关镓的说法不正确的是()A.元素符号是Ga B.相对原子质量为69.72g C.属于金属元素
- 雁南飞,燕归来属于( ) A.迁徙行为 B.取食行为 C.繁殖行为 D.防御行为
- 国际工人运动推动了马克思主义理论的诞生,马克思主义理论经历了产生—实践—实现—发展的过程,这个过程的史实论证不相符的是A
- 有BaCl2和NaCl的混合溶液a L,将它均分成两份。一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使
- .如图是实验室常用的仪器,请用图中仪器的名称按要求填空:(1)用于夹持试管的仪器是 ; (2)取用粉末状药品时一般选
- 世界上的事物千差万别,纷繁复杂,其原因在于 ( ) A.矛盾的普遍性 B.矛盾的特殊性 C. 矛盾的
- 甲、乙两个实心球质量相等,放入水中后,它们露出水面的体积分别为各自体积的1/3和1/2,那么() A.甲、乙两物体的密度
- — Have you called Mr. Johnson’s office? — Yes, he _____ b
- 某地以东是东半球,以西是西半球,以北是北温带,以南是热带,该点的经纬度是( ) A、20°E,23.5°N
- 过点B(0,-a)作双曲线x2-y2=a2右支的割线BCD,又过右焦点F作平行于BD的直线,交双曲线于G、H两点.(1
- 2008年12月3日召开的国务院常务会议要求各地要认真落实适度宽松的货币政策。下列符合这一政策措施的有①提高个人所得税起
- 下列有关染色体和基因的叙述,错误的是( ) A.基因位于染色体上 B.
- 关于现象、本质 ,感性认识和理性认识之间的关系,以下表述正确的是:( )A.本质总是表现为一定的现象,理性认识总要
- 下列化学方程式的书写完全正确的是( ) A.C+O2====CO2 B.4Fe+3O22Fe2O3 C.KMnO4K
- 某种群中年轻的个体非常多,年老的个体却很少,其种群密度将会 A.绝对不变 B.相对稳定
- 下列地区人口稠密的是( ) A.热带雨林地区 B.地势高峻的高原山地 C.高纬度严寒地区 D.中低纬度
- 已知定义在上的函数满足:且,,则方程在区间上的所有实根之和为( ) A. B.
- 淀粉溶液遇碘变蓝色。实验表明,无论是固体碘还是碘蒸气,均能使淀粉溶液变蓝色。这一现象说明
- 下列分子中,所有原子最外层均为8电子结构的是 A. BeCl2 B. H2O C. CO2



