黑龙江省牡丹江市2020-2021学年高一上学期期末考试化学试题
黑龙江省牡丹江市2020-2021学年高一上学期期末考试化学试题
教材科目:化学
试卷分类:高一上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高一上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
下列推理正确的是( )
A . 铝粉在氧气中燃烧生成Al2O3 , 故钠在氧气中燃烧生成Na2O
B . 铁能从硫酸铜溶液中置换出铜,故钠也能从硫酸铜溶液中置换出铜
C . 活泼金属钠保存在煤油中,故活泼金属铝也保存在煤油中
D . 钠与氧气、水等反应时钠均作还原剂,故金属单质参与反应时金属单质均作还原剂
|
|
| 2. 单选题 | 详细信息 |
|
在CuO和Fe粉的混合物中,加入一定量的稀硫酸,并微热,当反应停止后,滤出不溶物,并向滤液中插入一枚铁钉,发现铁钉并无任何变化。根据上述现象,确定下面结论正确的是( )
A . 不溶物一定是Cu
B . 不溶物一定含铜,但不一定含铁
C . 不溶物一定是Fe
D . 溶液中一定含有Fe2+ , 但不一定含有Cu2+
|
|
| 3. 单选题 | 详细信息 |
|
下列关于合金的叙述中正确的是( )
A . 合金一定是由两种或多种金属熔合而成的
B . 日常生活中用到的五角硬币属于铜合金
C . 铝合金的硬度比铝的大,熔点比铝的高
D . 商代的司母戊鼎是由纯铜打造而成的
|
|
| 4. 单选题 | 详细信息 |
|
向含有1 mol KAl(SO4)2的溶液中逐滴加入氢氧化钡溶液,充分反应。下列说法错误的是( )
A . 当Al3+恰好完全沉淀时,消耗氢氧化钡1.5 mol
B . 当SO42-恰好完全沉淀时,铝元素全部以偏铝酸根的形式存在
C . 当向溶液中加入1.5 mol氢氧化钡时,反应可用下列离子方程式表示:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
D . 随加入的氢氧化钡的物质的量不断增大,沉淀的物质的量不断增大
|
|
| 5. 单选题 | 详细信息 |
|
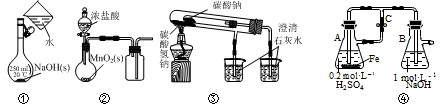
下列图示方法能完成相应实验的是( )
A . 用图①配制一定物质的量浓度的NaOH溶液
B . 用图②在实验室制取Cl2
C . 用图③探究碳酸氢钠和碳酸钠的热稳定性
D . 用图④制备少量Fe(OH)2并能较长时间看到其白色
|
|
| 6. 单选题 | 详细信息 |
|
36.5gHCl溶解在1L水中(水的密度近似为1 g×mL-1),所得溶液的密度为ρ g×mL-1 , 质量分数为w,物质的量浓度为c g×mL-1 , NA表示阿伏加德罗常数,下列说法正确的是( )
A . 所得溶液的物质的量浓度:c=1 g×mL-1
B . 所得溶液中含有NA个HCl分子
C . 36.5 gHCl气体占有的体积为22.4L
D . 所得溶液的质量分数: w=

|
|
| 7. 单选题 | 详细信息 |
|
用NA表示阿伏加德罗常数的值。下列叙述中正确的是( )
A . 足量Na2O2和11.2LCO2反应,转移电子数目为0.5NA
B . 1molSO2和O2的混合气体中含有的氧原子数为2NA
C . 常温常压下,17gOH—所含电子数为9NA
D . 5.6g铁与7.1g氯气充分反应,转移电子数为0.3NA
|
|
| 8. 单选题 | 详细信息 |
|
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA
B . 标准状况下,11.2 L CCl4中含有分子的数目为0.5NA
C . 2 L 0.5 mol· L-1硫酸钾溶液中阴离子所带电荷数为NA
D . 标准状况下,22.4 L氨水含有NA个NH3分子
|
|
| 9. 单选题 | 详细信息 |
|
将5mol·L-1盐酸10mL稀释到100mL,再取出5mL,这5mL溶液的物质的量浓度是( )
A . 0.05mol·L-1
B . 0.5mol·L-1
C . 0.1mol·L-1
D . 0.25mol·L-1
|
|
| 10. 单选题 | 详细信息 |
|
相同温度下,下列选项中前者一定大于后者的是( )
A . 所含分子数:6.72LCH4与4.48LNH3
B . 所含原子总数:18.0gH2O与36.5gHCl
C . 所含离子总数:0.5mol·L-1Fe2(SO4)3溶液与0.5mol·L-1FeCl3溶液
D . 密闭容器中的压强:2L容器中盛有2molO2与1L容器中盛有1.5molH2
|
|
高中化学 试卷推荐
- 2015-2016学年广东省清远市阳山县南阳中学高一上学期月考化学试卷(9月份)
- 2017年高考理综真题试卷(化学部分)(新课标Ⅰ卷)
- 2016-2017学年河南省洛阳市白马中学高二上学期开学化学试卷
- 2015年四川省成都市崇州市崇庆中学高考化学“一诊”模拟试卷(六)
- 山东省潍坊市临朐县2019-2020学年高三下学期化学模拟考试试卷(二)
- 吉林省五地六市联盟2018-2019学年高二下学期化学期末考试试卷B卷
- 人教版高中化学选修五 第五章 第一节 合成高分子化合物的基本方法 同步练习
- 河北省邯郸市2020年高考化学一模试卷
- 2016-2017学年江西省赣州市厚德外国语学校高二上学期开学化学试卷
- 四川省绵阳市丰谷中学2016-2017学年高二上学期化学期中考试试卷
- 广东省潮州市潮安区颜锡祺中学2019-2020学年高二上学期化学期中考试试卷
- 第24讲:烃
最近更新
- 动物细胞表面有一种物质,就好比是细胞与细胞之间或者细胞与其他大分子之间互相联络用的文字或语言,这种物质是()
- 1mol某烃A完全燃烧生成5molCO2和5molH2O。A在一定条件下发生加聚反应,生成高聚物B。(1)烃A分子中的碳
- 已知圆C在x轴上的截距为和3,在y轴上的一个截距为1. (1)求圆C的标准方程; (2)若过点的直线l被圆C截得的弦AB
- 有这样一位大学毕业生,上学期间并不是学新闻专业,却被某报社聘用。当谈及成功原因时说:“从大二起,我就在这家报社实习。要想
- 许多照相机镜头到胶片的距离是可调的。某次拍摄前摄影师已经“调好焦”,使被摄者在胶片上形成了清晰的像。如果在拍摄前被摄者和
- (陕西卷文14)的展开式中的系数为 .(用数字作答)
- 在社会公众的强烈呼吁下,国务院下属98个部门中的绝大部分已向社会公开三公经费 (公车购置费、公务招待费、出国经费)及财政
- 喜马拉雅山脉地区的发展演变说明了 A.内力作用进行得极其缓慢,不易被人们
- 如图所示表示生物体内核酸的基本单位--核苷酸的模式图,下列说法正确的是()A.DNA与RNA在核苷酸上的不同点只体现在②
- 英国革命和法国大革命“不仅反映了它们本身发生的地区即英法两国的要求,而且在更大得多程度上反映了当时整个世界要求”。这表明
- I’m_____ taller than he.A.moreB.a littleC.mostD.many
- 为了解释地球的磁性,19世纪安培假设:地球的磁场是由绕过地心的轴的环形电流I引起的。在下列四个图中,正确表示安培假设中环
- 探究与实践(14分)材料一:2011年3月21日,涿州市青少年科技服务中心组织学生开展“3·23”世界气象日科普活动。2
- We'd better wait more minutes. I think Jeff will come so
- 如图,已知四边形ABCD和BCEG均为直角梯形,AD//BC,CE//BG,且,平面平面BCEG,BC=CD=CE=.
- (本小题满分13分)如图,在直角坐标系中,有一组底边长为的等腰直角三角形,底边依次放置在轴上(相邻顶点重合),点的坐标为
- 质量为1t的汽车沿半径为49m的水平公路面转弯,若路面对车的动摩擦因数为μ=0.4,且假定最大静摩擦力等于滑动摩擦力。则
- 随着中国国际地位提高和国际交往日增,世界范围内的汉语热在不断升温。你认为今天世界“汉语热”出现的主要原因是( )。①中
- 下面对古诗句的品析,不恰当的一项是 A.海日生残夜,江春入旧年:“生”、“入”两字,形象地表现了时序的变迁、新旧的交替。
- Now you live in an important year _____, harder than ever be