人教(新课标)高中化学一轮复习:专题3离子反应
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 多选题 | 详细信息 | ||||||||||||||||||||||||||
|
利用如图所示装置进行实验,能达到相应实验目的的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||||||||
| 2. 多选题 | 详细信息 |
|
除去电石渣浆(CaO)清液中的S2- , 并制取石膏(CaSO4·2H2O)的流程如图所示:
下列说法错误的是( )
A . 过程I、II中起催化剂作用的物质是Mn(OH)2
B . 17.2g石膏失水后质量变为14.5g,所得固体中CaSO4与结晶水物质的量之比为1:1
C . 10L上清液(S2-浓度为320mg·L-1)中的S2-转化为
 时,理论上共需要4.48LO2
D . 过程II反应的离子方程式为4MnO 时,理论上共需要4.48LO2
D . 过程II反应的离子方程式为4MnO  +2S2-+9H2O= +2S2-+9H2O=  +4Mn(OH)2↓+10OH- +4Mn(OH)2↓+10OH-
|
|
| 3. 多选题 | 详细信息 |
|
常温下,向
 某一元碱 某一元碱  溶液中逐滴加入 溶液中逐滴加入  的 的  溶液,溶液中 溶液,溶液中  中和率的变化如图所示。 中和率的变化如图所示。  为 为  的电离常数, 的电离常数,  下列说法正确的是( ) 下列说法正确的是( )
A . 溶液中水的电离程度从a点到d点逐渐增大
B . a点时,
 C . b点时,
C . b点时,  D . c点时,
D . c点时, 
|
|
| 4. 多选题 | 详细信息 |
|
某溶液中只可能含有
 中的几种离子,各离子浓度均为 中的几种离子,各离子浓度均为  。某同学进行了如图实验: 。某同学进行了如图实验:
A . 无法确定原溶液中是否含有
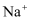 B . 原溶液中肯定存在的离子为
B . 原溶液中肯定存在的离子为  C . 沉淀A为
C . 沉淀A为  ,沉淀C为 ,沉淀C为  D . 滤液X中大量存在的阳离子有
D . 滤液X中大量存在的阳离子有  和 和 
|
|
| 5. 填空题 | 详细信息 |
|
某化学兴趣小组设计了如图装置,该装置能制取 Cl2 , 并进行相关性质实验,且可利用装置A 储存多余的氯气。
|
|
| 6. 填空题 | 详细信息 |
|
|
| 7. 实验探究题 | 详细信息 |
|
长期缺碘和碘摄入过量都会对健康造成危害,目前加碘食盐中碘元素绝大部分以IO3-存在,少量以I-存在。现使用Na2S2O3对某碘盐样品中碘元素的含量进行测定。
|
|
| 8. 实验探究题 | 详细信息 | |
|
实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:
|
||
| 9. 单选题 | 详细信息 |
|
分类法是化学学习的重要方法,下列说法正确的是( )
①冰水混合物属于纯净物,高分子化合物属于混合物 ②CaCl2、NaOH、HCl、HT四种物质都是化合物 ③0℃,101kPa,含有1mol硫原子的SO2与SO3的混合物,其体积小于22.4L ④既能与酸反应又能与碱反应的氧化物属于两性氧化物 ⑤AlCl3属于共价化合物,故AlCl3是非电解质;胆矾、苛性钠、冰醋酸、氧化钾均是电解质 ⑥向新制氯水中加入碳酸钙粉末,能提高溶液中HClO的浓度 ⑦1molBrCl与H2O完全反应生成氯化氢和次溴酸,转移的电子的物质的量为1mol ⑧碘的升华、NaOH潮解、胶体渗析、氯化钠溶液导电、煤的干馏均属于物理变化
A . ①④⑦⑧
B . ③④⑤⑥⑧
C . ②⑤⑥⑦.
D . ①③⑥
|
|
| 10. 单选题 | 详细信息 |
|
常温下pH=1的某溶液A中含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、Cl-、I-、SO42-中的4种,且溶液中各离子的物质的量浓度均为0.1mol/L,现取该溶液进行有关实验,实验结果如图所示:下列有关说法正确的是( )

A . 该溶液中一定有上述离子中的NO3-、Al3+、SO42-、Cl
|
|
- 河南省洛阳市2017-2018学年高二下学期化学期末考试试卷
- 内蒙古赤峰市2015-2016学年高三上学期化学期末考试试卷
- 2015-2016学年陕西省榆林市府谷县麻镇中学高三上学期期中化学试卷
- 第6讲:镁、铝及其化合物
- 2016-2017学年江西省赣州市十四县(市)联考高二下学期期中化学试卷
- 2016-2017学年山东省德州市武城二中高一下学期期中化学试卷(普通班)
- 2016-2017学年福建省宁德市部分一级达标中学高一上学期期中化学试卷
- 重庆市江津巴县长寿等七校联盟2017-2018学年高考理综-化学三模考试试卷
- 山西省孝义市2017-2018学年高考理综-化学一模考试试卷
- 2015-2016学年四川省雅安市天全中学高一下学期期中化学试卷
- 福建省厦门市2020年高考理综-化学4月模拟试卷
- 贵州省安顺市2017-2018学年高考理综-化学三模考试试卷
- The rich_____ not always happy. A. is B. are
- She is very good at playing ___ piano and now she is teachin
- 如图6所示,轻质杠杆OA可绕O点转动,杠杆长0.2m,在它的A端挂一重20N的物体G,若在杠杆上的中点B处施加最小的力F
- 关于x的方程的解是x1=-2,x2=1(a,m,b均为常数,a≠0),则方程的解是 ▲ .
- Win a week in England! You still don’t know what to do thiss
- 2010年,冰岛火山多次喷发,曾迫使欧洲的民航飞机停飞,火山灰里含有大量的硅酸钙(CaSiO3),硅酸钙中Si元素的化合
- 讨论函数f(x)=x+(a>0)的单调性.
- —Who can reach the book onthe top of the shelf? —Xiaoqiang
- 菜刀在下列五种情况下发生锈斑轻重程度顺序是( ) ①切湿咸菜后放置 ②切酸菜后放置 ③切完菜后洗净擦干
- 健康人、流感、流感病人、流感病人的飞沫、流感病毒分别属于 ①传染源 ②病原体 ③传播途径 ④传染病 ⑤易感人群
- 函数f(x)=sin xcos x+cos 2x的最小正周期和振幅分别是 ( ) A.2π,1
- 我们经常能在电视上看到这样的情景:站在悬崖下的人仰头望着生长在崖间的树,把手中的长绳抛向树干,由于绳端系着一块石头,所以
- 下图中的“誓死力争,还我青岛”是哪一运动的口号A.戊戌变法 B.新文化运动
- 我们读过《伊索寓言》的很多寓言,请写出几个读过的篇目(至少三个),并写出一则寓言的寓意。篇名:_________,___
- 小夏同学向上提静止在桌面上的金属板,并用传感器测量拉力和桌面受到的压强,收集到以下数据,请根据表中数据归纳出压强p和拉力
- 解决城市交通拥挤最有效、最科学的办法是 () A.在市中心区建立大量停车场B.学校、工厂和机关安排不同的上下班
- 下列对应关系不正确的是() A.积贫——富国 B.积弱——强兵之法 C.“
- (6分)某化工厂排放的污水中含有Mg2+、Fe3+、Cu2+四种离子,甲、乙、丙三位同学设计从污水中回收铜的方案如下:(
- 下列化学肥料中,属于复合肥的是 A.CO(NH2)2 B.K2SO4 C.NH4H2
- 在学到《机械振动与机械波》时,四位同学就自己看到的现象,发表自己的观点,让你从物理学的角度来看,你认为他们谁说的对:(

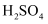
 生成
生成 或
或 

 溶液
溶液 悬浊液
悬浊液 与
与 


 下列说法错误的是( )
下列说法错误的是( )
 晶体 ②
晶体 ②  ③液态醋酸 ④铜 ⑤固体
③液态醋酸 ④铜 ⑤固体  ⑥纯蔗糖
⑥纯蔗糖  ⑦酒精
⑦酒精  ⑧熔融的
⑧熔融的  ⑨氨水 ⑩液氮.
⑨氨水 ⑩液氮. 
 最小的是.
最小的是. B.
B.  分子数 D.
分子数 D. 
 时,
时,  的电离平衡常数
的电离平衡常数  的电离平衡常数
的电离平衡常数  ,试写出下列情况下发生的离子反应方程式:
,试写出下列情况下发生的离子反应方程式:  溶液中通入少量
溶液中通入少量 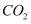 :
: 溶液中滴入少量新制氯水:
溶液中滴入少量新制氯水: ,某化学兴趣小组用上述原理实验室制备硫代硫酸钠如图:
,某化学兴趣小组用上述原理实验室制备硫代硫酸钠如图:
 ,
,  ,
, 




