人教高中化学一轮复习:专题14物质的分离、提纯与检验
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
豆浆营养丰富,是大众喜爱的传统饮品。下列制作豆浆的主要步骤中,属于过滤的是( )
A . 泡豆
 B . 磨豆
B . 磨豆 C . 沥浆
C . 沥浆 D . 煮浆
D . 煮浆
|
|
| 2. 单选题 | 详细信息 | |||||||||||||||
|
分离提纯是化学学科的基本实验操作。下列为达到实验目的所使用的分离提纯方法不正确的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 3. 单选题 | 详细信息 | ||||||||
|
下列基本实验操作正确的是( )
A . A
B . B
C . C
D . D
|
|||||||||
| 4. 综合题 | 详细信息 |
|
钛合金是一种重要的航空材料,以下是以钛铁矿(主要成分为FeTiO3 , 含FeO和Fe2O3等杂质)为原料制备金属钛及副产品铁红的工艺流程:
已知:①TiO2+易水解为TiO2·nH2O;高温下钛易与N2、H2等反应。 ②常温下,Ksp [Fe(OH)2]=8.0×10-16 , Ksp[FeCO3]=3.2×10-11。 回答下列问题:
|
|
| 5. 综合题 | 详细信息 | ||||||||||||||||||||
|
从印刷电路板的腐蚀废液(主要含CuCl2、FeCl3、FeCl2等)中回收FeCl3、制备CuSO4·5H2O的流程如下。
|
|||||||||||||||||||||
| 6. 综合题 | 详细信息 | |||||||||||||||
|
废镍催化剂主要含Ni,还有少量Cu、Fe、Al及其氧化物、
 。某研究性学习小组设计如下工艺流程回收镍,制备硫酸镍晶体 。某研究性学习小组设计如下工艺流程回收镍,制备硫酸镍晶体 。 。
该小组同学查阅资料知: ①镍的化学性质与铁相似,能与酸缓慢反应。 ②溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
|
||||||||||||||||
| 7. 综合题 | 详细信息 |
|
山西运城实施“盐湖‘全科’修复,生态蝶变‘提速’”工程,“五步制盐”古老工艺将传承再现。模拟“五步制盐法”制备粗盐(主要成分
 , 还含有 , 还含有 以及泥沙等杂质),并进一步在实验室中制备精盐的流程如下。 以及泥沙等杂质),并进一步在实验室中制备精盐的流程如下。
|
|
| 8. 单选题 | 详细信息 | ||||||||||||||||||||
|
为了提纯表中所列物质(括号内为杂质),有关除杂试剂和分离方法的选择错误的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
| 9. 综合题 | 详细信息 |
|
金属镓拥有电子工业脊梁的美誉,镓与铝同族,化学性质相似。一种从高铝粉煤灰(主要成分是Al2O3 , 还含有少量Ga2O3和Fe2O3等)中回收镓的工艺如下:
回答下列问题:
|
|
| 10. 综合题 | 详细信息 |
|
菜之魂在味,在“七味八滋”中,盐应是百味之首。粗盐常含有少量
 、 、  、 、  以及泥沙等杂质,实验室中提纯 以及泥沙等杂质,实验室中提纯  的流程如图所示。 的流程如图所示。 回答下列问题:
|
|
- 江苏省宿迁市2017-2018学年高一上学期化学期末考试试卷
- 高中化学人教版(2019)必修第一册 第一章单元测试
- 湖南省张家界市2018-2019学年高一上学期化学期末考试试卷
- 湖北省十堰市2019-2020学年高二下学期化学期末考试试卷
- 2015-2016学年江苏省南通市如皋市高一下学期期中化学试卷
- 人教版高中化学选修五 第一章第三节:有机化合物的命名
- 2016-2017学年四川省绵阳市丰谷中学高二上学期开学化学试卷
- 2019年初中化学中考难点专练 16 无机化工流程
- 福建省三明市2019-2020学年高一下学期化学期末考试试卷
- 2019年高考化学真题分类汇编专题07:化学平衡
- 江苏省南京师范大学附属中学2020年高考化学6月模拟试卷
- 浙江省嘉兴市2019-2020学年高二下学期化学期末考试试卷
- 聚乙烯、聚氯乙烯、有机玻璃都是常见的塑料。塑料属于 A.金属材料 B.合成材料 C.复合材
- 下列关于农业的叙述,正确的是: A、饲养奶牛不属于农业 B、农业生产的基本条件是土地资源 C、农业生产就是生产
- 焰色反应属于( ) A.元素的性质
- 从集合{,,,}中任意取出两个不同的数记作,则方程表示焦点在轴上的双曲线的概率是 .
- With the economic situation worsening _______, shopkeepers h
- 如图所示的是甲、乙两种质量相等的非燃料液体吸收的热量与温度变化情况的图像,请根据图像中提供的信息判断,_________
- 下列说法中正确的是( )A.100 mL pH=3的盐酸和醋酸溶液,与足量锌反应,起始时二者产生氢气的速率基本相等
- 在青海玉树地地震救灾中因舍己救人不幸牺牲的香港义工黄福荣受到人们的广泛赞誉,香港市民称他为“香港之子”,内地同胞赞他为“
- 下列肯定不含核糖的一组结构或物质是( ) A.质粒和T2噬菌体的遗传物质 B.酶和
- 法国政府曾向各国递交一份备忘录,为将要到来的议和定调子。其中写道:“由于各国使馆希望前往沿海或各国部队想要从沿海前往首都
- 张若虚的《春江花月夜》“人生代代无穷己.江月年年望相似.不知江月待何人,但见长江送流水”。刘希夷的《代悲白头翁》“年年岁
- 如图,∠AOB=∠COD=90°,OC平分∠AOB,∠BOD=3∠DOE.试求∠COE的度数.
- 我国现阶段,在收入分配上实行以按劳分配为主体、多种分配方式并存的分配制度.其直接原因是 A.我国现阶段生产力总体水平低、
- 文中共有10处语言错误,每句中最多两处。错误涉及一个单词的增加、删除或修改。 增加:在此处加一个漏词符号(∧),并在其下
- 已知复数|z|=2,求复数1++z的模的最大值、最小值.
- 下列有关Fe2(SO4)3溶液的叙述正确的是 A、该溶液中K+、Fe2+、C6H5OH、Br-可以大量共存 B、和KI溶
- 下列各句中,没有语病,句意明确的一句是() A.美国国务卿希拉里20日抵京,开始为期三天的访华行程,中美双方希望通过此次
- 完成句子 按所给的汉语,用英语完成下列句子。 1. 尽管他是我遇见的最有钱的人,但他从不炫耀他的财富。 Although
- 某学习小组在实验室制取CO2气体的过程中,不慎用到了浓盐酸,导致制得的CO2气体中混有HCl气体,他们设计了如下除去HC
- 许多俗语或广告词包含着丰富的经济生活道理。下列体现的经济生活道理对应正确的是( ) ①“保险不会改变你的生活,但是会





 , 计算该反应的平衡常数K=。
, 计算该反应的平衡常数K=。

 浓度过小,原因是(用离子方程式表示),不能得到硝酸铜晶体。
浓度过小,原因是(用离子方程式表示),不能得到硝酸铜晶体。 中铁(含
中铁(含 、
、 )的含量,评定纯度等级。
)的含量,评定纯度等级。 和
和 溶液,加热。
溶液,加热。 。过滤、洗涤,得到红褐色沉淀。
。过滤、洗涤,得到红褐色沉淀。 溶解红褐色沉淀,滴入
溶解红褐色沉淀,滴入 溶液,稀释至一定体积。将溶液红色的深浅与标准色阶对照,确定含量。
溶液,稀释至一定体积。将溶液红色的深浅与标准色阶对照,确定含量。 完全沉淀的pH为6.7,
完全沉淀的pH为6.7, 溶液,研究
溶液,研究 溶液的再生条件。
溶液的再生条件。

 , 有
, 有
 ,
,  )
) 、。
、。


 的pH
的pH 的pH
的pH 目的是(用离子方程式表示)。有同学认为可用NaClO代替
目的是(用离子方程式表示)。有同学认为可用NaClO代替 c.
c. d.
d.
 ,
,  , 则“调pH”需控制溶液pH的范围为。
, 则“调pH”需控制溶液pH的范围为。 的溶解度随温度变化关系,据图分析操作B是。
的溶解度随温度变化关系,据图分析操作B是。

 溶液时发生反应的离子方程式为。
溶液时发生反应的离子方程式为。



 精盐,配制成
精盐,配制成 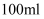 溶液;量取
溶液;量取  与
与  的
的 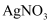 溶液反应,消耗
溶液反应,消耗  ,则该精盐样品中
,则该精盐样品中 


