高中化学人教版(2019)选择性必修1 第二章第四节 化学反应的调控
高中化学人教版(2019)选择性必修1 第二章第四节 化学反应的调控
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
氨是重要的化工产品之一,研究合成氨反应具有重要意义.σ
(1)已知断裂下列化学键需要吸收的能量分别为:N≡N 946.0kJ•mol﹣1、H﹣H 436kJ•mol﹣1、N﹣H 390.8kJ•mol﹣1 , 写出以N2(g)和H2(g)为原料合成NH3(g)的热化学方程式 (2)某小组研究了其他条件不变时,改变某一条件对上述反应的影响,实验结果如图1所示: ①t1时刻改变的条件为 ②t2时刻,恒压充入氦气,t3时刻达到平衡.在图中画出t2时刻后的速率变化图象. (3)相同温度下,A、B、C三个密闭容器,A、B恒容,C带有可自由移动的活塞K,各向其中充入如图2所示反应物,初始时控制活塞K,使三者体积相等,一段时间后均达到平衡. ①达到平衡时,A、C两个容器中NH3的浓度分别为c1、c2 , 则c1 c2(填“>”、“<”或“=”). ②达到平衡时,若A、B两容器中反应物的转化率分别为α(A)、α(B),则 α(A)+α(B) 1(填“>”、“<”或“=”). ③达到平衡时,若容器C的体积是起始时的 (4)直接供氨式碱性燃料电池(DAFC),以KOH溶液为电解质溶液,其电池反应为 4NH3+3O2═2N2+6H2O,则负极的电极反应式为 |
|
| 2. 单选题 | 详细信息 |
|
从化学反应速率和化学平衡两个角度考虑,合成氨应采用的条件是( )
A . 低温、高压、催化剂
B . 低温、低压、催化剂
C . 适当温度、高压、催化剂
D . 高温、高压、催化剂
|
|
| 3. 单选题 | 详细信息 |
|
合成氨工业采用下列措施是为了使平衡正向移动而提高反应物转化率的是( )
A . 采用高温
B . 采用高压
C . 使用催化剂
D . 以上均不对
|
|
| 4. 综合题 | 详细信息 |
|
氨是最重要的氮肥,是产量最大的化工产品之一.德国人哈伯在1905年发明了合成氨的方法,其合成原理为:N2(g)+3H2(g)
|
|
| 5. 综合题 | 详细信息 |
|
氨是重要的无机化工产品,合成氨工业对国民经济和社会发展具有重要的意义。其原理如下:N2(g)+3H2(g)
 2NH3 (g) ΔH< 0。在恒温恒容密闭容器中进行合成氨反应,各组分浓度与时间的关系如图所示。 2NH3 (g) ΔH< 0。在恒温恒容密闭容器中进行合成氨反应,各组分浓度与时间的关系如图所示。
|
|
| 6. 单选题 | 详细信息 |
|
合成氨生产中,说法正确的是( )
A . 使用催化剂,提高原料的利用率
B . 采用高温、高压工艺提高氨的产率
C . 产物用水吸收,剩余气体循环利用
D . 增大反应物浓度,对v正影响更大
|
|
| 7. 综合题 | 详细信息 |
|
工业上合成氨反应为:N2+3H2
 2NH3 , 回答下列问题: 2NH3 , 回答下列问题:
|
|
| 8. 单选题 | 详细信息 |
|
比较合成氨工业与制硫酸中SO2催化氧化的生产过程,正确的是( )
A . 都按化学方程式中的系数比投料
B . 都选择了较大的压强
C . 使用不同的催化剂加快反应速率
D . 都采用吸收剂分离产物
|
|
| 9. 综合题 | 详细信息 |
|
|
| 10. 单选题 | 详细信息 |
|
合成氨反应难以发生的根本原因是( )
A . 该反应是可逆反应
B . 氮分子中存在氮氮叁键
C . 该反应需要催化剂
D . 氨气容易液化
|
|
高中化学 试卷推荐
- 湖南省郴州市2021年高考化学3月模拟试卷
- 2022年新高考山东化学高考真题
- 广东省揭阳市2021年高考化学2月模拟试卷
- 天津市河北区2022届高三下学期质量检测(二)化学试题
- 山西省晋中市2021年高考化学二模试卷
- 江西省景德镇市2021-2022学年高三第一次模拟化学试题
- 广东省湛江市第四中学2020-2021学年高一上学期化学期中考试试卷
- 贵州省贵阳市2022届高三一模理综化学试卷
- 备考2021年高考化学二轮专题 第5讲 物质结构 元素周期律
- 陕西省榆林市2022届高三下学期四模理科综合化学试题
- 黑龙江省哈师大青冈实验中学2020-2021学年高二上学期化学开学考试试卷
- 黑龙江省齐齐哈尔市2021-2022学年高二上学期期末考试化学试题
最近更新
- 下列各组有机物,不管它们以何种比例混合,只要总物质的量一定,则完全燃烧时消耗O2为一恒量的是( ) ①C2H4和C
- 如图所示是一个几体体的三视图,其侧视图是一个边长为的等边三角形,俯视图是由两个等边三角形拼成的菱形,则该几何体的体积为(
- 右图中N、S为南北极点,P、Q是晨昏线与某一经线圈的两个交点,K、L位于晨线与昏线的中点,P、K两地经度差
- 阅读下面的文言文,完成1—4题。 黄歇受约归楚,楚使歇与太子完入质于秦,秦留之数年。楚顷襄王病,太子不得归。而楚
- The Bunsen Burner is so named because it is thought ________
- The fact __________she hasn’t know the result of the examin
- 5、下面是摘自柳斌《中国近代粮食生产衰落原因分析》的中国古代粮食相关情况统计表。这表明 时期粮食亩产(公斤/亩年)人均占
- 下图是某小组同学配制100 mL 0.100 mol·L-1Na2CO3溶液的一些关键步骤和操作图。(1)配制过程所需的
- It is difficult to ________ for yourself on the concert stag
- 为了保护鱼类资源不受破坏,并能持续地获得最大捕鱼量,根据种群增长的S型曲线,应使被捕鱼群的种群数量保持在K/2水平。这是
- 为训练宇航员适应失重状态,需要创造失重的环境,在地球表面附近,可以在飞行器的座舱内短时间地进行失重实验。设想某一飞行器可
- 消防队员手持水枪灭火,水枪跟水平面有一仰角.关于水枪射出水流的射高和射程下列说法中错误的是( )
- —Happy birthday to you,Gina!—. A.All right B.Thank you
- I’m afraid your parents won’t ________ of your joining the c
- 现有浓盐酸、浓硫酸、氢氧化钠、石灰水四种溶液,将其长期露放在空气中,溶液质量因发生物理变化而减少的是,而增大的是.因发生
- 假定英语课上老师要求同桌之间交换修改作文, 请修改你同桌写的以下作文。文中 共有10处语言错误,每句中最多有两处。每
- 经过原点和(4,0)的两条抛物线,,顶点分别为,且都在第1象限,连结交轴于,且.1.分别求出抛物线和的解析式;2.点C是
- 下列对阿司匹林的描述错误的是() A.化学名为乙酰水杨酸 B.是一种有机碱
- We are allsurprised to see him drive a Benz. Who knows ____
- 有关专家建议,在未来几年,中国的通货膨胀率保持在3%左右将对中国经济的稳定有利无害.所谓通货膨胀率为3%,指的是每年消费

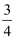 , 则平衡时容器C中H2的体积分数为
, 则平衡时容器C中H2的体积分数为 






