福建省三明市教研联盟2021-2022学年高二下学期期中联考化学试题
福建省三明市教研联盟2021-2022学年高二下学期期中联考化学试题
教材科目:化学
试卷分类:高二下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高二下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
已知
 呈粉红色, 呈粉红色,  呈蓝色, 呈蓝色,  为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: 为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:  ,用该溶液做实验,溶液的颜色变化如下: ,用该溶液做实验,溶液的颜色变化如下: 以下结论和解释正确的是( )
A . 等物质的量的
 和 和  中σ键数之比为3:2
B . 由实验①可推知△H<0
C . 实验②是由于c(H2O)增大,导致平衡逆向移动
D . 由实验③可知配离子的稳定性: 中σ键数之比为3:2
B . 由实验①可推知△H<0
C . 实验②是由于c(H2O)增大,导致平衡逆向移动
D . 由实验③可知配离子的稳定性: 
|
|
| 2. 单选题 | 详细信息 |
|
三种元素基态原子的电子排布式如下:①
 ② ② ③ ③ 。下列有关比较中正确的是( ) 。下列有关比较中正确的是( )
A . 第一电离能:③>①>②
B . 原子半径:①>②>③
C . 电负性:③>①>②
D . 最高正化合价:③>①>②
|
|
| 3. 单选题 | 详细信息 |
|
下列关于晶体的叙述正确的是( )
A . 晶体中只要有阳离子就一定有阴离子
B . 区分晶体和非晶体最可靠的方法是对固体进行X射线衍射实验
C . 分子晶体中共价键键能越大熔点和沸点越高
D . 金属晶体发生形变时,内部金属离子与“自由电子”的相互作用消失
|
|
| 4. 单选题 | 详细信息 |
|
实验室可用
 检验 检验 , 离子方程式为 , 离子方程式为 。下列有关说法正确的是( ) 。下列有关说法正确的是( )
A .
 中铁离子的配位数为9
B . 中铁离子的配位数为9
B .  元素在周期表中位于第4周期ⅧB族,属 元素在周期表中位于第4周期ⅧB族,属 区
C . 区
C .  中含 中含 键数目为 键数目为 D .
D .  比 比 更难再失去1个电子 更难再失去1个电子
|
|
| 5. 单选题 | 详细信息 |
|
下列叙述中正确的个数有( )
①氧原子的轨道表示式(电子排布图): ②处于最低能量状态原子叫基态原子, ③1~36号元素中,基态原子的价电子层有3个未成对电子的元素有5种 ④非极性分子中一定有非极性键,极性分子中一定有极性键 ⑤金属键和氢键都有方向性和饱和性 ⑥在有机化合物中,碳原子和碳原子之间形成的σ键比π键更牢固
A . 0个
B . 1个
C . 2个
D . 3个
|
|
| 6. 单选题 | 详细信息 |
|
有关结构如下图所示,下列说法中错误的是( )
A . 在
 晶胞中,与 晶胞中,与 最邻近等距离的 最邻近等距离的 有6个
B . 在干冰晶体中,每个晶胞拥有6个 有6个
B . 在干冰晶体中,每个晶胞拥有6个 分子
C . 在金刚石晶体中,碳原子与碳碳键个数比为 分子
C . 在金刚石晶体中,碳原子与碳碳键个数比为 D . 该气态团簇分子的化学式为
D . 该气态团簇分子的化学式为
|
|
| 7. 单选题 | 详细信息 |
|
如图所示,
 为乙二胺四乙酸( 为乙二胺四乙酸( ),易与金属离子形成螯合物, ),易与金属离子形成螯合物,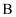 为 为 与 与 形成的螯合物。下列叙述正确的是( ) 形成的螯合物。下列叙述正确的是( )
A .
 结构中 结构中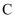 原子均采取 原子均采取 杂化
B . 杂化
B . 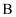 结构中 结构中 的配位数为6
C . 的配位数为6
C .  和 和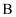 结构中均含有分子内氢键
D . 结构中均含有分子内氢键
D .  和 和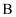 结构中均含有手性碳原子 结构中均含有手性碳原子
|
|
| 8. 单选题 | 详细信息 |
|
向
 溶液中逐滴滴加氨水,先生成蓝色沉淀,后蓝色沉淀逐渐溶解,溶液变为深蓝色。接着向深蓝色溶液中加入 溶液中逐滴滴加氨水,先生成蓝色沉淀,后蓝色沉淀逐渐溶解,溶液变为深蓝色。接着向深蓝色溶液中加入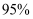 乙醇,静置后有深蓝色硫酸四氨合铜晶体析出,上层溶液颜色变浅。下列有关说法正确的是( ) 乙醇,静置后有深蓝色硫酸四氨合铜晶体析出,上层溶液颜色变浅。下列有关说法正确的是( )
A . 生成蓝色沉淀反应的离子方程式为
 B .
B .  溶液转化为深蓝色溶液过程中,溶液中 溶液转化为深蓝色溶液过程中,溶液中 的浓度相等
C . 硫酸四氨合铜在乙醇中的溶解度小于在水中的溶解度
D . 在 的浓度相等
C . 硫酸四氨合铜在乙醇中的溶解度小于在水中的溶解度
D . 在 配离子中, 配离子中, 给出孤电子对, 给出孤电子对, 提供空轨道 提供空轨道
|
|
| 9. 单选题 | 详细信息 |
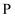 原子在形成 原子在形成 分子时, 分子时, 、 、 轨道和1个 轨道和1个 轨道参与形成 轨道参与形成 杂化, 杂化, 的空间构型为三角双锥形(如下图所示)。下列关于 的空间构型为三角双锥形(如下图所示)。下列关于 分子的说法错误的是( ) 分子的说法错误的是( )
A .
 分子中价电子对数为5
B . 分子中价电子对数为5
B .  分子中没有形成 分子中没有形成 键
C . 键
C .  分子中所有的 分子中所有的 键角都相等
D . 键角都相等
D .  分子中 分子中 原子也采用 原子也采用 杂化 杂化
|
|
| 10. 单选题 | 详细信息 |
|
前4周期元素
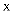 、 、 、 、 、 、 的原子序数依次增大。 的原子序数依次增大。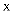 和 和 的基态原子的 的基态原子的 能级上各有两个未成对电子, 能级上各有两个未成对电子, 与 与 同族, 同族, 原子核内有29个质子。下列说法正确的是( ) 原子核内有29个质子。下列说法正确的是( )
A .
 与 与 形成的化合物晶胞如图所示,该化合物的化学式为 形成的化合物晶胞如图所示,该化合物的化学式为 B .
B . 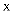 与 与 形成的简单化合物分子的空间构型均为直线形
C . 简单氢化物的沸点: 形成的简单化合物分子的空间构型均为直线形
C . 简单氢化物的沸点: D .
D .  的含氧化合物都能用于漂白 的含氧化合物都能用于漂白
|
|
高中化学 试卷推荐
- 2015-2016学年内蒙古包头市北重五中高二上学期期末化学试卷(理科)
- 2015-2016学年河南省信阳市高级中学高三下学期开学化学试卷
- 2015-2016学年河南省许昌市三校高一上学期第一次联考化学试卷
- 2016-2017学年广东省惠州市永汉中学高一下学期期中化学试卷
- 宁夏吴忠市2017-2018学年高考理综-化学模拟考试试卷
- 广东省揭阳市2018-2019学年高三上学期理综-化学期末考试试卷
- 高中化学人教版 选修四 第一章 化学反应与能量 第一节 化学反应与能量的变化 化学反应与能量第一课时(焓变 反应热)
- 2020年高考理综化学真题试卷(新课标Ⅰ)
- 内蒙古自治区呼和浩特市开来中学2019-2020学年高一下学期化学期末考试试卷
- 山东省德州市2019-2020学年高一下学期化学期末考试试卷
- 广东、河南、湖南、湖北四省2020年高三联考模拟试卷
- 2016-2017学年北京市怀柔区高二上学期期末化学试卷
最近更新
- 在一定温度下,有盐酸、硫酸、醋酸三种溶液,请按要求回答下列问题:(1) 当三种酸的物质的量浓度相同时,电离出来的c(H+
- 在下列运动状态下,物体处于平衡状态的有 A.蹦床运动员上升到最高点时 B.秋千摆到最低点时 C.相对静止于水平匀速运动的
- 有两棵树,一棵树高8米,另一棵树高2米,两棵树相距8米,一只小鸟从一棵树梢飞到另一棵树梢,至少要飞_____米.
- 海尔集团将电冰箱等产品打入欧美市场,并不是依靠( ) A.企业的全球战略 B.对欧美
- 2013年世界环境日中国主题为“同呼吸,共奋斗”。下列做法不符合这一主题的是 A.植树造林,绿化家园
- 随着科技水平的提高,人类对地球形状的认识经历了“天圆地方”、“圆球体”、“扁球体,,和“不规则扁球体”的漫长过程。人类对
- 若|x|=4,则x=
- 关于“中心法则”含义的叙述不正确的选项是( ) A.DNA只能来自DNA的复制 B.表示基因
- 计算:.
- Jimoften ______ to the library on weekends. He likes reading
- 如图导轨竖直放置,电源电动势,内阻,竖直导轨电阻可忽略,金属棒的质量,电阻,它与导轨间的摩擦因数,有效长度为,靠在导轨外
- 过点且与直线平行的直线方程为 ( ) A. B. C. D.
- 长江、黄河发源于是( ) A、青海省 B、四川省 C、西藏自治区 D、
- 如图3所示,质量为m、电荷量为-q的小球悬挂于O点,O点处于水平放置的相距为d、电势差为U的平行金属板正中,给小球一个水
- 函数随自变量的增大而增大,图象与轴交于(-4,0),则 >0时,的取值范围是( ). A.>-4
- 右边漫画《另辟蹊径》给我们的就业启示是( ) A.要树立自主择业观 B.要树立竞争就业观 C.要树立职业平等观
- X、Y、Z和R为原子序数依次递增的四种元素。其中X、Y同周期,X的最高正价是最低负价绝对值的3倍,Y、Z、R同主族,R为
- 阅读下文,完成12~14题。(9分) 绿色之恋 葛道吉 ①那是一片浩瀚的绿色林海。 ②进入绿林。便迷了眼睛,便绿
- 随着社会发展,人们越来越关注健康、养生。据此回答下题。 “养生专家”张悟本说:“喝绿豆汤可以包治百病。”一时间,绿豆价格
- 20.限制酶可识别并切割DNA分子上特定的核苷酸序列。下图为四种限制酶BamHI、EcoRI、HindIII及BgIII

 过程中形成的是发射光谱
过程中形成的是发射光谱







