广东省梅州市水寨中学2019-2020学年高二上学期化学期中考试试卷
广东省梅州市水寨中学2019-2020学年高二上学期化学期中考试试卷
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
|
|
| 2. 单选题 | 详细信息 |
|
用Na2FeO4溶液氧化废水中的还原性污染物M,为研究降解效果.设计如下对比实验探究温度、浓度、 pH、催化剂对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示,
下列说法正确的是( )
A . 实验①在15 min内M的降解速率为1.33×10-2mol/(L·min)
B . 若其他条件相同,实验①②说明升高温度,M降解速率增大
C . 若其他条件相同,实验①③证明pH越高,越有利于M的降解
D . 实验②④说明M的浓度越小,降解的速率越慢
|
|
| 3. 单选题 | 详细信息 |
|
我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程,该历程示意图如下所示。
下列说法错误的是( )
A . 生成CH3COOH总反应的原子利用率为100%
B . CH4→CH3COOH过程中,有C—H键发生断裂
C . ①→②放出能量并形成了C—C键
D . 该催化剂可有效提高反应物的平衡转化率
|
|
| 4. 单选题 | 详细信息 |
|
根据如下能量关系示意图,下列说法正确的是( )
A . 1molC(g)与1molO2(g)的能量之和为393.5kJ
B . 反应2CO(g)+O2(g)=2CO2(g)中,生成物的总能量大于反应物的总能量
C . 由C→CO的热化学方程式为:2C(s)+O2(g)=2CO(g) ΔH=-221.2kJ·mol-1
D . 热值指一定条件下单位质量的物质完全燃烧所放出热量,则CO热值ΔH=-10.1 kJ·mol-1
|
|
| 5. 单选题 | 详细信息 |
|
下列说法正确的是( )
A . CaO+H2O=Ca(OH)2可放出大量热,可利用该反应设计成原电池,把化学能转化为电能
B . 任何化学反应中的能量变化都表现为热量变化
C . 有化学键断裂一定发生化学反应
D . 灼热的铂丝与NH3、O2混合气接触,铂丝继续保持红热,说明氨的氧化反应是放热反应
|
|
| 6. 单选题 | 详细信息 |
|
固态或气态碘分别与氢气反应的热化学方程式如下:
①H2(g)+I2(?)⇌2HI(g)△H=-9.48kJ•mol-1 ②H2(g)+I2(?)⇌2HI(g)△H=+26.48kJ•mol-1 下列判断错误的是( )
A .
|
|
| 7. 单选题 | 详细信息 |
|
一定温度下,把2.5molA和2.5molB混合盛入容积为2L的密闭容器里,发生如下反应:3A(g)+B(g)
A . x=4
B . 达到平衡状态时A的物质的量浓度为c(A)=1.0mol·L-1
C . 5s内B的反应速率 v(B)=0.05mol·(L·s)-1
D . 达到平衡状态时容器内气体的压强与起始时压强比为6:5
|
|
| 8. 单选题 | 详细信息 |
|
向某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体,一定条件下发生如下反应:3A(g)
A . 若t1=15 s,则用A的浓度变化表示t0~t1阶段的平均反应速率为0.004mol·L-1·s-1
B . t1时该反应达到平衡,A的转化率为60%
C . 该容器的容积为2L,B的起始的物质的量为0.02mol
D . t0~t1阶段,此过程中容器与外界的热交换总量为akJ,该反应的热化学方程式为3A(g)
|
|
| 9. 单选题 | 详细信息 |
|
2SO2(g)+O2(g)
A . 该反应的逆反应为吸热反应,升高温度可提高活化分子的百分数
B . 500℃、101kPa下,将1molSO2(g)和0.5molO2(g)置于密闭容器中充分反应生成SO3(g)放热akJ,其热化学方程式为2SO2(g)+O2(g)
|
|
| 10. 单选题 | 详细信息 |
|
在3个体积均为1 L的恒容密闭容器中发生反应:SO2(g)+2NO(g)
A . 该反应的ΔH>0
B . T1时,该反应的平衡常数为
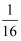 C . 容器Ⅰ与容器Ⅱ均在T1时达到平衡,总压强之比大于1:2
D . 若T2<T1 , 达到平衡时,容器Ⅲ中NO的体积分数大于40%
C . 容器Ⅰ与容器Ⅱ均在T1时达到平衡,总压强之比大于1:2
D . 若T2<T1 , 达到平衡时,容器Ⅲ中NO的体积分数大于40%
|
|
高中化学 试卷推荐
- 备考2018年高考化学一轮基础复习:专题6 钠、镁及其化合物
- 山东省烟台市2017-2018学年高考理综-化学二模考试试卷
- 吉林省博文中学2018-2019学年高一下学期化学3月月考试卷
- 2016-2017学年湖南省衡阳市高二上学期期末化学试卷
- 陕西省宝鸡市岐山县2016-2017学年高二上学期化学期末考试试卷(文科)
- 专题11:氮及其化合物
- 2016-2017学年河北省邯郸市四县联考高一下学期期中化学试卷
- 2015-2016学年四川省南充市营山二中高一下学期期末化学模拟试卷
- 广东省广州市2020年高考理综-化学3月模拟试卷(全国I卷)
- 2017_2018学年高中化学新人教版必修二 第一章 第一节 元素周期表
- 人教版高中化学选修五 第四章 第一节 油 脂 同步练习
- 2016-2017学年福建省泉州市惠南中学高一上学期期中化学试卷
最近更新
- 下列中国古代科学家中,对甘薯种植做过研究和介绍的是
- 一个袋中装有2个红球和2个白球,现从袋中取出1个球,然后放回袋中再取出1个球,则取出的2个球同色的概率为() A.
- 已知等差数列的前n项和为,,则使得取最大值时n的值 为( ) A.11或12 B.12
- 2009年7月5日,由境内外“三股势力”精心策划和组织的乌鲁木齐“7·5”严重暴力犯罪事件给当地人民群众生命财产造成重大
- 蛋白质工程中直接需要进行操作的对象是( ) A.氨基酸结构 B.蛋白质空间结构 C.肽链
- 比较大小, ▲ .
- To all the famousartists’ surprise, the unknown woman’s two
- 儿子长得和父亲很像,这种遗传现象是下列哪项的作用( ) A、DNA B、细胞膜 C、细胞质 D
- 有人在谈到国企改革的问题时讲道,“办好企业,光靠一个厂长不行;但搞垮一个企业,一个厂长足矣”。这告诉我们 …( )
- Pirates from Somalia who hijacked _____European carrier in
- 请回答下列有关金属的问题。 (1)铝是活泼金属,为什么通常铝锅却很耐腐蚀?
- 根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量么 (近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完
- 右图示意我国东部主要石化基地和企业的分布,读图完成47~48题。 47.图中主要石化基地共同区位优势在于 A.资源丰
- 已知抛物线C的方程为x2=2py(p>0),过抛物线上点M(-2,p)作△MAB,A、B均在抛物线上.过M作x轴的平行线
- 生物体内的蛋白质千差万别,即使像催产素、牛加压素、血管舒张素等由相同数量的氨基酸构成的蛋白质,生理功能也差异很大。其原因
- 下列说法正确的是A.两种烃相对分子质量相同,但结构不同,则它们一定是同分异构体B.有机物和无机物之间不可能出现同分异构体
- 下列变化不属于物理变化的是( )A.灯泡用久了灯丝变细 B.用石灰浆抹墙,经过一段时间后变硬C.用压缩体积的办法,使丁烷
- 2009年2月1日,“家电下乡”在全国推广,农民购买彩电、冰箱、洗衣机、手机四大类产品将可获得产品销售价格13%的财政补
- 固知一死生为虚诞, 。(王羲之《兰亭集序》)
- 下列各大河中,汛期最长的是 A.珠江 B.长江 C.黄河












