化学方程式的有关计算 知识点题库
将某元素形成的单质0.1mol与氯气充分反应,生成物的质量比原单质的质量增加了7.1g,这种元素可能是( )
A . Na
B . Fe
C . Cu
D . Al
标准状况下,某同学向 100mL H2S 饱和溶液中通入SO2 , 所得溶液 pH 变化如图所示.下列分析中,正确的是( )
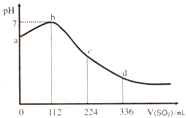
A . ab 段反应是:SO2+2 H2S=3S↓+2 H2O
B . 亚硫酸是比氢硫酸更弱的酸
C . 原H2S溶液的物质的量浓度为0.05 mol•L﹣1
D . b 点对应的溶液导电性最强
在1.00L 1mol/L氢氧化钠溶液中通入16.8L标准状况下的CO2气体,所得的溶液中含有的溶质是( )
A . Na2CO3
B . NaHCO3
C . Na2CO3和NaHCO3
D . NaOH、Na2CO3和NaHCO3
等质量的下列有机物充分燃烧时,消耗氧气最多的是( )
A . 甲烷
B . 乙烯
C . 苯
D . 乙醇
有FeO、Fe2O3的混合物若干克,在足量H2气流中加热充分反应,冷却后称得剩余固体比原混合物减轻0.8g;将等质量的原混合物与盐酸反应,欲使之完全溶解,至少需要1mol/L盐酸的体积为( )
A . 0.1L
B . 0.2L
C . 0.5L
D . 1.0L
25℃ 和101kpa时,乙烷、乙炔和丙烯组成的混合烃32mL与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体的总体积缩小了72mL,原混合烃中乙炔的体积分数为( )
A . 12.5%
B . 25%
C . 50%
D . 75%
某厂排放的废水中含有碳酸钠,未经处理,会造成污染.化学兴趣小组的同学对废水处理设计了如图所示的实验方案.试计算:

-
(1) 反应生成CO2气体的质量是 g.
-
(2) 反应后所得溶液中溶质的质量分数?
2.1g镁铝合金完全溶于足量盐酸,生成氢气2.24L(标准状况下),再向溶液中加入氢氧化钠溶液,生成沉淀的质量最大是( )
A . 2.9 g
B . 4.6 g
C . 5.5 g
D . 6.9 g
向100mL18mol•L﹣1浓硫酸中加入20g铜粉,加热一段时间后,冷却,过滤,得剩余固体7.2g.
-
(1) 标准状况下,产生气体的体积是多少?(假设产生的气体全部放出)
-
(2) 将最终所得溶液稀释至1L,滴加2mol•L﹣1的氢氧化钠溶液,若要使溶液中的Cu2+全部沉淀,需加入该氢氧化钠溶液的体积为L.
将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L.请回答:
-
(1) NO的物质的量为mol,NO2的物质的量为mol.
-
(2) 待产生的气体全部释放后,向溶液中加入VmL、amol•L﹣1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为mol•L﹣1 .
-
(3) 欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3 , 至少需要30%的双氧水g.
120mL含有0.20mol碳酸钠的溶液和200mL盐酸,不管将前者滴入后者,还是将后者滴入前者,都有气体产生,但最终生成的气体体积不同,且比值为5:2,则盐酸的浓度是( )
A . 2.0mol/L
B . 1.0mol/L
C . 0.18mol/L
D . 1.25mol/L
在标准状况下把4.48 L CO2通过足量的Na2O2固体后,固体增加的质量是( )
A . 8.8 g
B . 5.6 g
C . 3.2 g
D . 2.4 g
将0.3 molMnO2和100mL 12 mol/L的浓盐酸混合后缓慢加热,充分反应后向留下的溶液中加入足量的AgNO3溶液,生成AgCl沉淀的物质的量为(不考虑HCl的挥发)( )
A . 等于0.6mol
B . 小于0.6mol
C . 大于0.6mol,小于1.2mol
D . 以上结论都不符合题意
铜和镁的合金4.6g完全溶于浓硝酸,若反应后硝酸被还原只产生标准状况下4480mLNO2气体和336mL的N2O4气体,在反应后的溶液中,加入1mol/L的NaOH溶液,当金属离子全部沉淀时,生成沉淀的质量为8.51g。下列说法错误的是( )
A . 该合金中铜与镁的物质的量之比是2:3
B . 得到8.51g沉淀时,加入NaOH溶液的体积为230mL
C . NO2和N2O4的混合气体中NO2的体积分数是93%
D . 该反应消耗HNO3的物质的量为0.23mol
38.4gCu跟适量的浓HNO3反应,Cu全部反应后共收集到气体22.4L(标准状况),反应中作氧化剂的硝酸与总消耗的HNO3的物质的量比( )
A . 5∶11
B . 6∶11
C . 5∶6
D . 6∶5
等体积、等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5:6,则甲、乙两烧杯中的反应情况可能分别是( )
A . 甲、乙中都是铝过量
B . 甲中铝过量,乙中碱过量
C . 甲中酸过量,乙中铝过量
D . 甲中酸过量,乙中碱过量
在一密封的容器中,将一定量的NH3加热使其发生分解反应:2NH3(g) 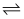 N2(g)+3H2(g),当达到平衡时,测得50%的NH3分解,此时容器内的压强是原来的( )
N2(g)+3H2(g),当达到平衡时,测得50%的NH3分解,此时容器内的压强是原来的( )
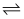 N2(g)+3H2(g),当达到平衡时,测得50%的NH3分解,此时容器内的压强是原来的( )
N2(g)+3H2(g),当达到平衡时,测得50%的NH3分解,此时容器内的压强是原来的( )
A . 1.125倍
B . 1.25倍
C . 1.375倍
D . 1.50倍
-
(1) 某烃经测定其蒸气密度为2.589g/L(已换算为标准状况),则其分子式为。
-
(2) 等物质的量下列物质 ①CH2=CH2 ②C2H5OH ③HOCH2CH2COOH分别完全燃烧,耗氧量大小关系是 (填序号)。
-
(3)
 用系统命名法命名其名称为。
用系统命名法命名其名称为。
-
(4) 有机物分子式为C4H10O,能与金属钠反应放出H2且能够氧化生成醛的物质有种。
将适量铁粉放入三氯化铁溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等。则已反应的Fe3+和未反应的Fe3+的物质的量之比是( )
A . 2∶3
B . 3∶2
C . 1∶2
D . 1∶1
NO是大气污染物之一,目前有一种治理方法是在400℃左右、催化剂存在的条件下,使NH3与NO发生反应:NO+NH3→N2+H2O(没有配平)。NA是阿伏加德罗常数的值,下列说法正确的是( )
A . 常温常压下,3.0gNO中含质子数为3NA
B . 1.8gH2O中含有共用电子对数目为0.4NA
C . NH3与NO混合气体1mol,所含氮原子数为2NA
D . 生成11.2L(标准状况下)N2时,转移电子数目为1.2NA
最近更新
- 实验测得某氯元素的氧化物中,氯元素与氧元素的质量比为71:64,该氧化物中氯元素化合价() A.
- 腹有诗书气自华 (12分)(1)是她那对世界无私的爱丰富了我,
- 2009年4月,《中共中央、国务院关于深化医药卫生体制改革的意见》(也称新医改方案)正式发布。新医改提出,到2011年基
- 当神州六号飞船往太空发射时,我们马上欢呼起来。(cheer up)
- 如图,圆:内的正弦曲线与轴围成的区域记为(图中阴影部分),随机往圆内投一个点,则点落在区域内的概率是( ) A、
- 微山湖是我国北方最大的淡水湖,湖内有鱼类78种,鸟类205种,湖中还有维管束植物239种,这些数字主要体现了()A. 生
- 科学研究过程一般包括发现问题、提出假设、实验验证、数据分析、得出结论等。在孟德尔探究遗传规律的过程中,导致孟德尔发现问题
- 随着经济的快速发展,我国能源消费总量由2003年的1204.2百万吨油当量上升到2012年的2735.2百万吨油当量;能
- 已知f(x)是定义在区间[-1,1]上的增函数,且f(x-2)<f(1-x),求x的取值范围.
- 明清时期商帮的崛起,为中国的历史画卷平添了一抹亮丽的色彩。阅读材料,回答问题。 材料一 古代徽州地处皖南崇山峻岭之中
- 锰(Mn)和镍(Ni)都是金属,将镍丝插入硫酸锰溶液中,无变化;将镍丝插入硫酸铜溶液中,镍丝上有铜析出。则Mn 、Ni
- Ⅰ.选择下列实验方法分离物质,将分离方法的序号填在横线上。 A、萃取分液法 B、渗析 C、结晶法 D、分液法
- 在平面直角坐标系中,把与轴交点相同的二次函数图像称为“共根抛物线”.如图,抛物线的顶点为,交轴于点、(点在点左侧),交轴
- 等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变成原体积的8/9(同温同压),这时混合气体中N2、O2、C
- 中共中央7月26日在中南海召开党外人士座谈会,就当前经济形势和下半年经济工作听取各民主党派中央、全国工商联领导人和无党
- “金砖四国”是指巴西、俄罗斯、印度及中国等发展中大国的发展模式。这一名称来自这四国国名开头英文字母BRIC的谐音英文单词
- 近年来,科学家们发现,除金刚石、石墨外,还有一些新的以单质形式存在的碳。其中,发现较早并在研究中取得重要进展的是C60分
- 广州市斥巨资复原南越王宫博物馆这一举动,遭到了51名专家学者的质疑。现在考古人员自己都说不清楚,它的“全貌谁都没见过,现
- 以下能说明细胞全能性的实验是 A.紫色糯性玉米种子培育出植株 B.胡萝卜韧皮部细胞培育出
- 北京是我们国家的政治中心,向世界展示着中华文化的悠久与灿烂。回答题。【小题1】保护世界文化遗产的说法,正确的是(



