粗盐提纯 知识点题库
-
(1) 实验室进行NaCl溶液蒸发时,一般有以下操作过程:
①放置酒精灯;②固定铁圈位置;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌;⑤停止加热。其正确的操作顺序为。
-
(2) 如何运用最简单的方法检验溶液中有SO
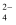 :。
:。如果有,应该如何除去SO
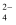 :。
:。 -
(3) 在粗盐经过溶解、过滤、除SO
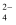 后的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止。请问这步操作的目的是
后的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止。请问这步操作的目的是。
实验室里需要纯净的氯化钠溶液,但手边只有混有硫酸钠、碳酸氢铵的氯化钠.某学生设计了如下方案:
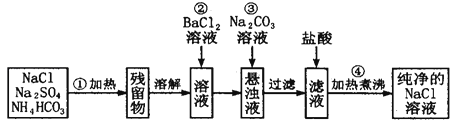
如果此方案正确,那么:
-
(1) 操作①可选择的仪器是
-
(2) 操作②是否可改为加硝酸钡溶液?为什么? ;理由
-
(3) 进行操作②后,如何判断SO42-已除尽,方法是
-
(4) 操作③的目的是 .为什么不先过滤后加碳酸钠溶液?理由是
-
(5) 操作④的目的是
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO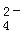 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):

-
(1) 判断BaCl2已过量的方法是
-
(2) 第④步中,相关的化学方程式是
-
(3) 配制NaCl溶液时,若出现下列操作,其结果偏高还是偏低?
A.称量时NaCl已潮解 B.天平的砝码已锈蚀
C.定容摇匀时,液面下降又加水 D.定容时俯视刻度线
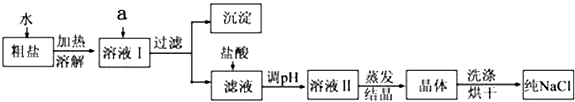
提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液、稀盐酸.
-
(1) 欲除去溶液I中的MgCl2、CaCl2、Na2SO4 , 从提供的试剂中选出a所代表的试剂,试剂的选择和滴加顺序均正确的是: ;A . Na2CO3溶液、BaCl2溶液、NaOH溶液 B . 溶液、NaOH溶液、K2CO3溶液 C . NaOH溶液、BaCl2溶液、Na2CO3溶液 D . Ba(NO3)2、NaOH溶液、Na2CO3溶液 E . BaCl2溶液、Na2CO3溶液、NaOH溶液
-
(2) 过量碳酸盐溶液的作用是.
-
(3) 洗涤晶体操作使用的玻璃仪器有.
-
(4) 蒸发结晶的操作方法是.
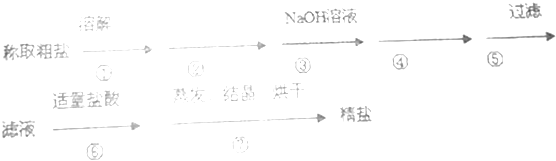
称取粗盐 
 滤液
滤液 
 粗盐 第①步的操作是,第⑤步的操作是.
粗盐 第①步的操作是,第⑤步的操作是.
-
(1) 实验室进行NaCl溶液蒸发时,一般有以下操作过程 ①放置酒精灯;②固定铁圈位置;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌; ⑤停止加热.其正确的操作顺序为.
-
(2) 如何运用最简方法检验溶液中有无SO42﹣离子?.如果有,应该如何除去SO42﹣离子?.
-
(3) 在粗盐经过溶解→过滤后的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止.请问这步操作的目的是.
-
(4) 将经过操作(3)后的溶液过滤.请问这一操作能除掉哪些杂质?.
-
(5) 实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的;
溶解时:.
过滤时:.
蒸发时:.
-
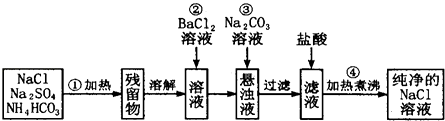
(1) 步骤②中应加入的试剂是溶液,判断此试剂已加过量的方法是.
-
(2) 步骤④中应加入的试剂是溶液,第④步中相关的化学方程式是.
-
(3) 若将第⑤步和第⑥步颠倒,会对实验结果产生影响,其原因是.
-
(4) ②③④中所加试剂的顺序也可以调整为 .A . ③②④ B . ④③② C . ②④③ D . ④②③
-
(5) 为检验粗盐溶液中Cl﹣、SO42﹣ , 请根据内容填空:
①首先检验离子,应先加入过量的.
②将所得混合物过滤,然后在溶液中加入试剂检验另一离子.
如果此方案正确,那么:
-
(1) 操作①可选择的仪器是.
-
(2) 操作②是否可改为加硝酸钡溶液?为什么?;理由.
-
(3) 进行操作②后,如何判断SO
 已除尽,方法是.
已除尽,方法是.
-
(4) 操作③的目的是.为什么不先过滤后加碳酸钠溶液?理由是.
-
(5) 操作④的目的是.
①过滤
②加过量的NaOH溶液
③加适量的盐酸
④加过量的碳酸钠溶液
⑤加过量的氯化钡溶液.
-
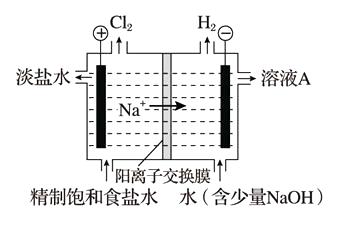
(1) 溶液A的溶质是。
-
(2) 电解饱和食盐水的离子方程式是。
-
(3) 电解时用盐酸控制阳极区溶液的pH在2~3。用化学平衡移动原理解释盐酸的作用:。
-
(4) 电解所用的盐水需精制,去除有影响的Ca2+、Mg2+、NH4+、SO42- [c(SO42-)>c(Ca2+)]。精制流程如下(淡盐水和溶液A来自电解池):
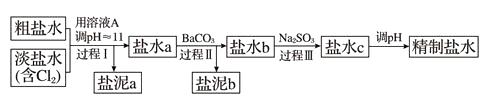
①盐泥a除泥沙外,还含有的物质是。
②过程Ⅰ中将NH4+转化为N2的离子方程式是。
③BaSO4的溶解度比BaCO3的小,过程Ⅱ中除去的离子有。
①加入稍过量的碳酸钠溶液;②加入稍过量的氢氧化钠溶液;③加入稍过量的氯化钡溶液;④滴入稀盐酸至无气泡产生;⑤过滤。正确的操作顺序是( )
 、
、  、
、  等杂质离子,现用下列操作除去,正确的顺序是( )
等杂质离子,现用下列操作除去,正确的顺序是( ) ①加NaOH②加Na2CO3③加BaCl2④加稀盐酸⑤过滤
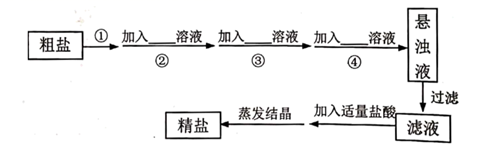
请回答下列问题:
-
(1) 操作①为。
-
(2) 操作②~④加入的试剂依次是、、。
-
(3) 写出过滤操作中所使用的玻璃仪器除了烧杯外,还需要、。
-
(4) 简述判断SO
 已除尽的方法。
已除尽的方法。
-
(5) 工业上用电解精制的饱和食盐水的方法制取氯气,方程式为,理论上每产生标准状况下5.6LCl2 , 转移电子的物质的量为。

下列说法正确的是( )
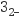
-
(1) 从海水中可提取多种化工原料,下图是工业上对海水资源进行综合利用的流程图。试回答下列问题:
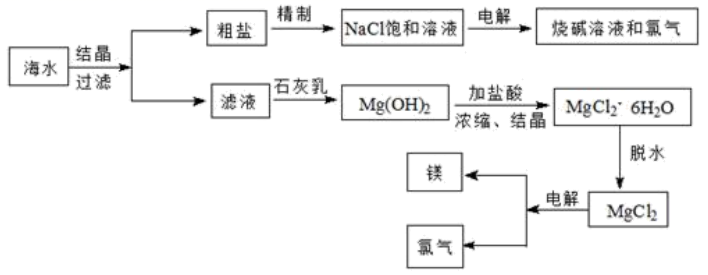
①若粗盐中含有杂质离子
 、
、 、
、 , 精制时所用试剂为:A.盐酸;B.
, 精制时所用试剂为:A.盐酸;B.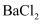 溶液;C.NaOH溶液;D.
溶液;C.NaOH溶液;D. 溶液。则加入试剂的顺序是(填序号)。
溶液。则加入试剂的顺序是(填序号)。②电解NaCl饱和溶液产生的NaOH和
 可用于制备对新冠病毒有效消杀的“84”消毒液,写出该反应的离子方程式:。
可用于制备对新冠病毒有效消杀的“84”消毒液,写出该反应的离子方程式:。③电解熔融
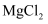 可制取镁和
可制取镁和 , 化学方程式为。其中
, 化学方程式为。其中 和
和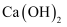 反应可制得漂白粉。漂白粉的有效成分是。
反应可制得漂白粉。漂白粉的有效成分是。 -
(2)
 (主要指NO和
(主要指NO和 )是大气主要污染物之一、有效去除大气中的
)是大气主要污染物之一、有效去除大气中的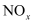 是环境保护的重要课题。在催化剂作用下,
是环境保护的重要课题。在催化剂作用下, 可与
可与 发生如下反应:
发生如下反应: 。
。
①该反应的氧化剂是,还原产物是。
②标准状况下生成
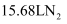 , 转移电子为mol。
, 转移电子为mol。
 , 下列有关粗盐提纯正确的是( )
, 下列有关粗盐提纯正确的是( )
- 已知P是圆M:x2+y2+4x+4-4m2=0(m>0且m≠2)上任意一点,点N的坐标为(2,0),线段NP的垂直
- 至少存在一点
- Don’t forget_________ the television when you go to bed.
- 下列句子没有语病的一项是( )(3分) A、老头子浑身没有多少肉,干瘦得像老了的鱼鹰。 B、通过初一、初二的锻
- 工业分散现象主要表现在A.电子元件供应厂家与电子装配工厂之间 B.简单产品的原料和零部件生产C.钢铁工业区和
- 为了检测“苏丹红”对人体细胞的毒害作用,研究人员以哺乳动物组织块为实验材料开展有关研究,得到下表结果。下列相关叙述,不正
- 有对夫妇筹资开了个小饭馆,夫妻俩既当老板又当服务员,后来生意越来越红火,他俩开起了连锁店,取名为“小南瓜”,雇工经营,自
- 下列关于化学反应限度的叙述中错误的是() A. 不同的化学反应,限度可能不同 B. 可以通过改变温度来控制化学反应的限度
- America has been experiencing the longest economic increase
- 常温下,在下列给定条件的各溶液中,一定能大量共存的离子组是() A.使酚酞变红色的溶液:Na+、Ba2+、I﹣、Cl﹣
- 阅读《轻放》 轻 放 ①走廊里的声控灯,很早以前就坏了。每次走到门口,同租三室一厅的几个人,都会习惯性地叹口气,在黑暗
- 张岱年说:“一个民族自立于世界民族之林,必须具有民族的自信心与自尊心。而民族的自信心和自尊心有其思想基础,即对于民族文化
- 有人这样形容罗斯福新政前后企业与政府的关系的变化:新政之前,企业主是老板,政府是“守夜人”;新政以来,企业主是大老板,政
- 直线上的点到圆上的点的最近距离是 ▲ .
- “I haven’t heard from Henry for a long time.” “What do you
- 将一瓶接近饱和的澄清石灰水变成饱和溶液,可采用的方法是 (任写一种)。
- 已知抛物线的相同的焦点,点是两曲线的 一个交点,且轴,若为双曲线的一条渐近线,则的倾斜角所在的区间可能是( )
- 1921年,苏俄实施的新经济政策
- 罗马帝国皇帝高度重视法律制定,许多法学家纷纷前来献策。下列四人的主张不可能被 采纳的是 A.丙建议政府保护一切自由民的
- 根据对话的上下文,在横线上写出所缺少的内容。 A: Hello! B: Hello? 1 Mrs. Green?



