镁的化学性质 知识点题库
取等物质的量的镁粉和铝粉混合,再将混合物平均分为四份,分别加入足量的下列溶液中,充分反应后放出氢气最多的是( )
A . 3mol/L的HCl
B . 4mol/L的HNO3
C . 8mol/L的NaOH
D . 18mol/L的H2SO4
将1.8g某金属与足量盐酸充分反应,产生2.24LH2(标准状况下),则该金属是( )
A . Al
B . Mg
C . Fe
D . Zn
某化学兴趣小组用回收的镁铝合金制取氢气。现有10.8g镁铝合金,下列说法正确的是( )
A . 常温下与足量18mol/LH2SO4溶液反应,最多可放出0.6molH2
B . 常温下与足量2mol/LHNO3溶液反应,最少可放出0.45molH2
C . 常温下与足量2mol/LH2SO4溶液反应,放出H2的物质的量在0.45~0.6mol之间
D . 常温下与足量2mol/LNaOH溶液反应,放出H2的物质的量在0.45~0.6mol之间
镁和铝都是较活泼金属,下列叙述正确的是()
①镁易溶于冷水,而铝难溶于冷水②镁溶于碱溶液,而铝难溶于碱溶液③常温下镁难溶于浓硫酸,而铝易溶于浓硫酸④镁易溶于氯化铵溶液,而铝难溶于氯化氨溶液
A . ①②
B . ③
C . ④
D . 全部
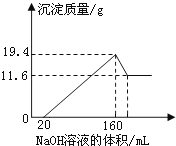
将一定质量的镁铝合金样品全部溶于100mL某浓度的盐酸中.向所得溶液中滴加5.0mol/L的NaOH溶液,生成沉淀质量与加入的NaOH溶液体积关系如图所示.
(1)19.4g沉淀中含有Al(OH)3的质量为 ;
(2)盐酸的物质的量浓度为 .
在CO2中,Mg燃烧生成MgO和C,下列说法不正确( )
A . 在该反应条件下,Mg的还原性强于C的还原性
B . Mg、MgO中镁元素微粒的半径:r(Mg2+)<r(Mg)
C . 元素C 在自然界中既有游离态又有化合态
D . 该反应中化学能全部转化为热能
下列关于镁和钠的比较,结论正确的是( )
A . 铝镁合金的硬度较大,钠钾合金的硬度较小
B . 因为钠的金属性比镁要强,所以钠的熔点比镁要高
C . 镁能置换硫酸铜溶液中的铜,钠也能置换硫酸铜溶液中的铜
D . 在空气中都能被点燃,生成的产物都是氧化物,氧在产物中的化合价都是﹣2
下列叙述正确的是( )
A . Mg、Al、Cu在空气中长时间放置,在其表面均生成氧化物
B . 把SO2气体分别通入到BaCl2、Ba(NO3)2溶液中均有白色沉淀生成
C . 工业上通常用电解钠、镁、铝对应的熔融氯化物制得该三种金属单质
D . 将水蒸气通过灼热的铁粉,反应后固体质量增加
在自然界存在游离态的元素是( )
A . 硫
B . 氯
C . 铝
D . 镁
某同学将镁条放在水中煮沸,趁热取出部分溶液,滴加酚酞试液,溶液变为红色,放置在空气中一段时间后,发现溶液的红色褪去了.
-
(1) 据你推测,溶液红色褪去的原因可能是
① ;
②.
-
(2) 请设计一个实验来证明你的其中一个推测,简要说明操作、现象及结论:
下列推断不正确的是( )
A . 工业上可以用碳还原二氧化硅得到硅和二氧化碳
B . 制普通玻璃的主要原料是纯碱、石灰石、石英
C . Mg失火不能用CO2灭火;Na失火也不能用CO2灭火
D . Fe与S直接化合生成FeS;Al与S也可以直接化合得到Al2S3
有一块镁铝合金,其中镁与铝的质量比是8:9。加入足量稀H2SO4使其完全溶解后,再加入NaOH溶液,生成沉淀的质量随NaOH溶液体积变化的曲线如下图,其中正确的是( )
A . 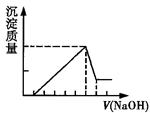 B .
B . 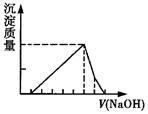 C .
C . 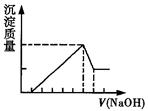 D .
D . 
 B .
B .  C .
C .  D .
D . 
下列有关金属性质的描述,符合事实的是( )
A . 金属钠暴露在空气中,表面变暗,生成白色的过氧化钠固体
B . 用坩埚钳夹住打磨过的镁带,在酒精灯上点燃,发出耀眼白光,放出大量热,生成白色固体
C . 用坩埚钳夹住一小块铝箔,在酒精灯上加热至熔化,轻轻晃动,有液态的铝滴落
D . 金属铝比铁活泼,因此在空气中,铁制品比铝制品耐腐蚀
镁粉在焰火、闪光粉、鞭炮中是不可少的原料,工业上制造镁粉是将镁蒸气在某种气体中冷却。现有下列气体:①空气②CO2③Ar④H2⑤N2 , 其中可作为冷却气体的是( )
A . ①和②
B . ②和③
C . ③和④
D . ④和⑤
一定量的镁铝合金与500mL 1mol•L-1 HNO3完全反应生成2.24LNO(标况),再向反应后的溶液中加入2mol•L-1 NaOH溶液,使镁、铝元素完全沉淀,则所加NaOH溶液体积是( )
A . 50mL
B . 100mL
C . 150mL
D . 200mL
-
(1) 有相同物质的量的 H2O 和 H2SO4 , 其质量之比为,氢原子个数比 为,氧原子个数比为。
-
(2) 把 3.06 g 铝和镁的混合物粉末放入 100 mL 盐酸中,恰好完全反应,并得到标准状况下 3.36 L H2。
计算:①该合金中铝的物质的量为。
②该合金中镁的质量为。
③反应后溶液中 Cl﹣的物质的量浓度为(假定反应体积仍为 100 mL)。
-
(3) 由 CO2 与 CO 组成的混和气体对 H2 的相对密度为 20,则混和气体中 CO2 的体积分数为; CO 的质量分数为。
下列物质中,不能与金属镁反应的是( )
A . Ar
B . N2
C . O2
D . CO2
将一定质量的镁铝合金投入一定体积10 mol·L-1的盐酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的质量与加入NaOH溶液的体积关系如图所示。若不考虑金属和盐酸反应时HCl的挥发,则下列说法错误的是( )
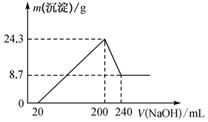
A . 该镁铝合金中铝的质量为5.4 g
B . 所用NaOH物质的量浓度为4.5 mol·L-1
C . 反应中沉淀的物质的量最多时为0.35 mol
D . 溶解合金所用盐酸的体积为100 mL
下列实验事实能得出相应结论的是( )
| 选项 | 实验事实 | 实验结论 |
| A | 将打磨后的镁条放入盛有稀盐酸的试管中,用手触摸试管外壁感觉变热 | 镁条与稀盐酸反应是放热反应 |
| B | 向某酸雨样品中加入Ba(OH)2溶液,有白色沉淀生成 | 酸雨试样中一定含SO |
| C | 将浓硫酸滴到蔗糖表面,固体变黑膨胀,有刺激性气味的气体产生 | 浓硫酸只有脱水性 |
| D | 将某气体通入酸性高锰酸钾溶液,溶液褪色 | 该气体一定是乙烯 |
A . A
B . B
C . C
D . D
下列有关金属的工业制法中,正确的是( )
A . 制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液
B . 制镁:用海水为原料,经一系列过程制得氧化镁固体, 还原得镁
C . 制铁:以铁矿石、焦炭为原料,用焦炭经一系列反应产生的CO还原得铁
D . 制铝:从铝土矿中获得氧化铝再得到氯化铝固体,电解熔融氯化铝得到铝
还原得镁
C . 制铁:以铁矿石、焦炭为原料,用焦炭经一系列反应产生的CO还原得铁
D . 制铝:从铝土矿中获得氧化铝再得到氯化铝固体,电解熔融氯化铝得到铝
 还原得镁
C . 制铁:以铁矿石、焦炭为原料,用焦炭经一系列反应产生的CO还原得铁
D . 制铝:从铝土矿中获得氧化铝再得到氯化铝固体,电解熔融氯化铝得到铝
还原得镁
C . 制铁:以铁矿石、焦炭为原料,用焦炭经一系列反应产生的CO还原得铁
D . 制铝:从铝土矿中获得氧化铝再得到氯化铝固体,电解熔融氯化铝得到铝
最近更新
- 右图所显示的书名为中国古代儒家经典的合称,它最早应该出现于 A.春秋时期 B.西
- 读“甲、乙两区域图”,完成3~4题。3.图中M、N是世界著名的湖泊,关于两湖泊的描述正确的是
- 已知椭圆,动直线 (1)若动直线与椭圆C相交,求实数的取值范围; (2)当动直线与椭圆C相交时,证明:这些直线被椭圆截得
- 罗荣渠在《现代化新论》一书中说:“在此以后,外国渗透的方式从外贸领域扩大到投资、生产、销售、金融各个领域,直接改变了原有
- 下列说法正确的是A.一定质量的气体,保持温度不变,压强随体积减小而增大的微观原因是:每个分子撞击器壁的作用力增大B.一定
- 分析处理图表中的信息是学习化学的一种重要方法。 (1)表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答: 温度/℃
- 短周期元素X和Y,可组成化合物XY3。当X的原子序数为a时,Y的原子序数可能是:①a+2,②a+4,③a+8,④a+12
- 一战后成立的国际联盟,其实质是 A、英法维护凡尔赛体系的工具 B、美国称霸世界的工具 C、促
- 在棱长为a的正方体ABCD—A1B1C1D1中,M是AA1的中点,则点A1到平面MBD的距离是()A.a
- I have told you the truth. ________ I keep repeating it? A.
- 一批早期改良派的思想家批评洋务派只知“师夷长技”,徒袭西艺之皮毛,未得西艺之要领。于是,他们在光绪皇帝的支持下,发动戊戌
- 右图1表示细胞分裂的不同时期与每条染色体DNA含量变化的关系,图2表示处于细胞有丝分裂某个时期的细胞图像。下列说法中正确
- ......
- ______ the growing number of patients, the clinic had to ext
- 民族工业自产生之日起,就具有顽强的生命力,一有机会就发展。为中国化学工业作出巨大贡献的人物是( ) A.范旭东
- 现有H、O、S、K四种元素,请选用其中两种或几种元素组成符合下列要求的物质,写出化学式各一个: (1)酸 (2)碱 (3
- 函数的值域是
- 读中东地区图,完成下列各题(6分)(1)本地区作为东、西方交通走廊的地位非常重要,其中的咽喉要道____________
- 依次填入下列各句横线处的词语,最恰当的一组是 ( )①加入世贸组织后,我国在享受 _____ 的同时,也要切实 ____
- 我国20世纪60年代社会主义建设时期在尖端科学技术方面取得的重大成就是() ①第一颗原子弹爆炸成功 ②籼型杂交水稻育成




