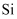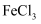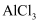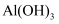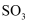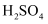含硫物质的性质及综合应用 知识点题库
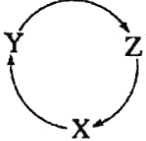
选项 | X | Y | Z |
A | | | |
B | | | |
C | | | |
D | | | |
选项 | X | Y | Z |
|
A | HCl | Cl2 | HClO | |
B | Fe | FeCl2 | FeCl3 | |
C | S | H2S | SO2 | |
D | NO | N2 | NH3 |
-
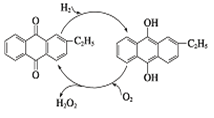
(1) I.双氧水(主要成分H2O2)是常见的氧化剂、还原剂。
如下图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式。
-
(2) H2O2可看作二元弱酸,写出它在水中第一步电离的方程式。
-
(3) II.A、B、C、D、E、X是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。
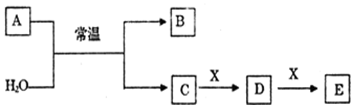
若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式: 。
-
(4) 若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则X可能为(填代号)。
a.NaHCO3 b.Na2CO3 c.Fe(OH)3 d.Na[Al(OH)4]
-
(5) 若A为淡黄色粉末,则A的电子式为。若X为一种最常见的造成温室效应的气体。则鉴别等浓度的D、E两种溶液,可选择的试剂为(填代号)。
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
-
(6) 若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为,E是(填化学式)。
 Si+CO2↑
B . 向铜粉中滴加稀硝酸产生气体:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
C . 浓硝酸通常显黄色:4HNO3
Si+CO2↑
B . 向铜粉中滴加稀硝酸产生气体:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
C . 浓硝酸通常显黄色:4HNO3  4NO2↑+O2↑+2H2O
D . 硫在纯氧中点燃发出蓝紫色火焰:2S+3O2
4NO2↑+O2↑+2H2O
D . 硫在纯氧中点燃发出蓝紫色火焰:2S+3O2  2SO3
2SO3
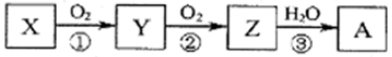
下列有关上述转化关系中物质及其反应的叙述错误的是( )
-
(1) 甲组采用如图装置脱硫(部分装置略)。
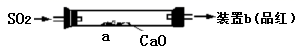
① CaO脱硫后的产物是。
② b中品红很快褪色,说明脱硫效果不好。下列措施能提高脱硫效果的是。
ⅰ.加快SO2气体流速
ⅱ.将堆集在一起的CaO平铺在整个玻璃管
ⅲ.加热a,脱硫效果可能会更好
③ 小组拟通过CaO的增重评价其脱硫能力。需要测量的数据是。
-
(2) 乙组选用AgNO3溶液脱除SO2 , 如图所示:
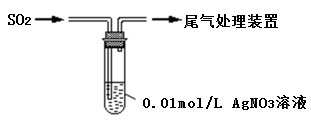
现象:通入SO2 , 立即生成大量白色沉淀A。对白色沉淀A的成分进行探究,提出假设:
假设1:发生了氧化还原反应,依据是AgNO3溶液中含有O2、NO
 等具有氧化性的粒子,沉淀A主要是Ag2SO4(微溶)。
等具有氧化性的粒子,沉淀A主要是Ag2SO4(微溶)。假设2:发生了复分解反应,依据是SO2与水生成酸,能与AgNO3溶液发生复分解反应。
实验探究:
①取沉淀A,加入蒸馏水,静置。取上层清液滴加Ba(NO3)2溶液,无明显变化。
②取,加入蒸馏水,静置。取上层清液滴加Ba(NO3)2溶液,产生沉淀。
实验证明"假设1"不成立。
③ 为进一步确认"假设2",向A中加入浓HNO3 , 立即产生红棕色气体。加入浓硝酸的目的是;经确认,反应后混合液中存在SO
 。
。实验证明"假设2"成立。
④产生沉淀A的化学方程式是,。AgNO3溶液具有良好的脱硫能力,但因其价格高,未能大规模使用。
-
(3) 丙组用NaClO脱除SO2 , 用1 L 0.1 mol/L的NaClO溶液最多可以吸收标准状况下的SO2L。
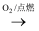 SO3
SO3  H2SO4
B . Si
H2SO4
B . Si  SiO2
SiO2  H2SiO3
C . NH3
H2SiO3
C . NH3 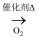 NO2
NO2  HNO3
D . Cl2
HNO3
D . Cl2 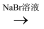 Br2
Br2  I2
I2
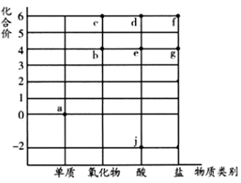
请回答下列问题:
-
(1) 硫元素在周期表中的位置。
-
(2) 氧元素比硫元素的非金属性(填“强"或“弱"”)。请用化学方程式证明该结论:。
-
(3) 写出b与j混合,发生反应的化学方程式。
-
(4) 已知硒(Se)与硫是相邻周期同主族元素。
①画出硒原子结构示意图。
②判断硒元素的主要化合价有。
③硒最高价氧化物的水化物与d相比较,酸性强弱关系为>(填化学式)。
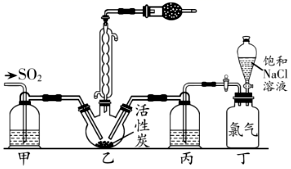
已知:①SO2(g)+Cl2(g)=SO2Cl2(l)ΔH<0
②硫酰氯熔点为-54.1℃,沸点为69.1℃,易水解,100℃以上分解生成二氧化硫和氯气。
下列说法错误的是( )
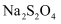 , 也称为保险粉)是一种白色砂状结晶或淡黄色粉末状化学用品,隔绝空气条件下加热至300℃时发生分解,有亚硫酸盐生成,同时放出刺激性气味气体;在250℃时能被引燃;该物质不溶于乙醇,溶于氢氧化钠溶液,遇少量水或暴露在潮湿的空气中会发生剧烈反应并燃烧,同样有刺激性气味气体产生。下列关于
, 也称为保险粉)是一种白色砂状结晶或淡黄色粉末状化学用品,隔绝空气条件下加热至300℃时发生分解,有亚硫酸盐生成,同时放出刺激性气味气体;在250℃时能被引燃;该物质不溶于乙醇,溶于氢氧化钠溶液,遇少量水或暴露在潮湿的空气中会发生剧烈反应并燃烧,同样有刺激性气味气体产生。下列关于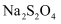 说法错误的是( )
说法错误的是( )
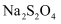 时应注意干燥并尽可能隔绝空气
B .
时应注意干燥并尽可能隔绝空气
B . 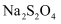 遇水所发生的是放热反应,燃烧时会有
遇水所发生的是放热反应,燃烧时会有 产生
C . 隔绝空气加热
产生
C . 隔绝空气加热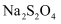 的反应为:
的反应为: D .
D . 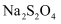 溶液可以和
溶液可以和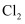 反应,但不能和酸性
反应,但不能和酸性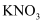 溶液反应
溶液反应
 能促进血管扩张,防止栓塞
能促进血管扩张,防止栓塞
 B .
B .  C .
C .  D .
D . 
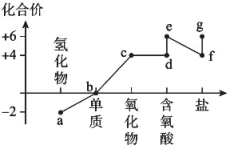
下列说法正确的是( )
 B . b只有一种分子,不存在同素异形体
C . d、e均属于二元强酸
D . a与c、d、e都有可能反应生成b
B . b只有一种分子,不存在同素异形体
C . d、e均属于二元强酸
D . a与c、d、e都有可能反应生成b

请回答下列问题:
-
(1) S在周期表中的位置是;Y的化学式为。
-
(2) 用电子式表示图中X的形成过程:;X的水溶液长期在空气中放置容易变浑浊,该变化可说明:S的非金属性比O(填“强或“弱”),用原子结构解释原因为:同主族元素原子的最外层电子数相同,从上到下,,得电子能力逐渐减弱。
-
(3) SO2是常见的大气污染物之一,同时也是重要的工业原料。实验室中常把SO2通入中,通过观察是否褪色检验SO2是否存在;SO2也可以使酸性高锰酸钾溶液褪色,二者褪色原理(填“相同”或“不同”)。
-
(4) 比较H2SO4和Na2SO4的熔点高低,并从微粒间相互作用(化学键、分子间作用力)的角度说出理由。情况下会生成(间二硝基苯)
 的质量分数为a%(假设杂质不含硫元素),其燃烧过程转化率为75%,
的质量分数为a%(假设杂质不含硫元素),其燃烧过程转化率为75%, 生成
生成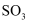 的转化率为80%,
的转化率为80%,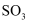 吸收率为98%,现有黄铁矿10t,能制备98%的硫酸( )
吸收率为98%,现有黄铁矿10t,能制备98%的硫酸( )
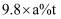 B .
B . 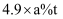 C .
C . 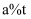 D .
D . 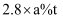
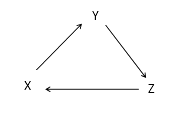
- 以下是一些常见物质间互相转化的关系图(有些反应条件已省略,各步反应均是恰好完全反应)。图中A、B均为无色气体,Y能使澄清
- 贾谊《过秦论》 贾谊,世称贾生。又称贾长沙,贾太傅。主要作品为《新书》58篇《过秦论》(上中下三篇)出于此书。另有《论积
- 2008年3月,台湾地区陈永扁当局推动的“入联公投”遭到失败,再次说明“台独”分裂势力搞“台独”是不得人心的。据此回答问
- 1.依次填入下列各句横线处的成语,最恰当的一组是 ①退休以后,老叶迷上了书法和篆刻,不仅到老年大学上课,还四出旅游,收集
- 如图,平面α⊥平面β,A∈α,B∈β,AB与两平面α、β所成的角分别为和,过A、B分别作两平面交线的垂线,垂足为A′、B
- 在某无色透明的酸性溶液中,能共存的离子组是
- 长江三峡水利枢纽工程2009年建成后,将避害趋利,按照人们的意志发挥巨大的综合效益。据此回答问题。 三峡工程按照人们的意
- 根据化学方程式不能获得的信息是() A.反应中的反应物和生成物 B.各反应物、生成物之间的质量比 C.化学反应速率的快慢
- Read the play and answer the questions.Place: A child’s room
- 某学生做匀速直线运动去给同学送一件东西,停留一会儿后又做匀速直线运动返回出发点.那么,如图2-11-1所示的位移—时间图
- 用丝绸摩擦过的玻璃棒去靠近甲、乙两个轻小物体,结果甲被排斥、乙被吸引。由此我们可以判定:A.甲带正电,乙带负电;
- 对于3Fe(s)+4H2O(g)Fe3O4(s)+4H2(g),若起始投入3mol铁、4mol水汽在体积为0.5L的密闭
- 某高校“统计初步”课程的教师随机调查了选该课的一些学生情况,具体数据如下表:为了判断主修统计专业是否与性别有关系,根据表
- 一What should we do first if we want to develop our village?
- 翻译下面文言文 颜渊喟然叹曰:“仰之弥高,钻之弥坚。瞻之在前,忽焉在后。夫子循循然善诱人,博我以文,约我以礼,欲罢不能。
- Instead of makingprogress, my work ______ seems to be going
- — What did the teacher say just now? — Sorry, I didn’t hear
- It is already home to whales, seals and polar bears, but soo
- 下列物质中既有离子键,又有共价键的是 ( )A.H2O B.CaCl2
- 正五棱柱中,不同在任何侧面且不同在任何底面的两顶点的连线称为它的对角线,那么一个正五棱柱对角线的条数共有( )