含硫物质的性质及综合应用 知识点
二氧化硫:物理性质,无色、有刺激性气味的有毒气体、密度比空气大。易液化。SO2的化学性质,是酸性氧化物与碱性氧化物反应,漂白性,通入品红溶液后变为无色,漂白纸浆、毛、 丝、草编制品等。具有氧化性,能与硫化氢发生反应, 具有还原性与强氧化剂反应。 用途:制硫酸、制漂白剂、消毒剂和防腐剂。
硫酸:纯硫酸是一种无色黏稠油状、难挥发的液体,密度比水大。易溶于水,能以任意比与水混溶、溶解时大量放热。质量分数为98%的浓硫酸,密度为1.84g/cm3,物质的量浓度为18.4mol/L。具有脱水性、强氧化性和酸性。用途 :工业上用做制过磷酸钙、磷酸、硫酸铵等化肥。金属材料表面除锈、金属矿石的处理。制取挥发性酸,制取硫酸盐。精炼石油、制炸药、农药、医药、染料等。实验室常用于制备氢气、氯化氢、二氧化硫、硫化氢等气体,做干燥剂、脱水剂、催化剂。
含硫物质的性质及综合应用 知识点题库
高温下,硫酸亚铁发生如下反应:2FeSO4 Fe2O3+SO2↑+SO3↑.若将生成的气体通入氯化钡溶液中,得到的沉淀物是( )
Fe2O3+SO2↑+SO3↑.若将生成的气体通入氯化钡溶液中,得到的沉淀物是( )
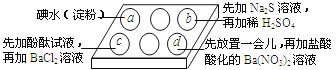
为探究Na2SO3溶液的性质,在白色点滴板的a、b、c、d四个凹槽中滴入Na2SO3 溶液,再分别滴加用如图所示的试剂对实验现象的“解释或结论”错误的是( )
选项 | 实验现象 | 解释或结论 |
A | a中溶液褪色 | 还原性:SO32﹣<I﹣ |
B | b中加硫酸后产生淡黄色沉淀 | SO32﹣和S2﹣在酸性条件下发生反应 |
C | c中滴入酚酞溶液变红,再加BaCl2溶液后产生白色沉淀且红色褪去 | SO32﹣+H2O⇌HSO3﹣+OH﹣ , 所以滴入酚酞变红; Ba2++SO32﹣→BaSO3↓(白),使水解平衡左移,红色褪去 |
D | d中产生白色沉淀 | Na2SO3溶液已被氧化变质 |
-
(1) Na2S溶液盛装在带橡胶塞的试剂瓶中,仔细闻有臭鸡蛋气味,请用离子方程式解释:,.
-
(2) 将Na2S溶液加入AlCl3溶液中,有白色沉淀和臭鸡蛋气味的气体生成,发生的离子反应为:.
-
(3) 将Na2S溶液加入AgCl的浊液中,生成的黑色沉淀是(写化学式).
-
(1) (实验探究)
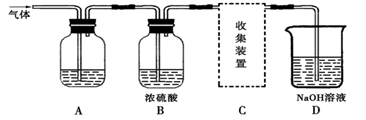
将12.6g的Na2SO3与足量的浓硫酸反应可制得SO2的体积为L(标准状况),该制取SO2的反应(选填“是”或“不是”)氧化还原反应。
-
(2) 若用A装置检验SO2具有漂白性,则A中的溶液是。
若用A装置检验SO2是一种酸性氧化物,则A中的溶液是。
-
(3) D装置中发生的反应是(写化学方程式):。
-
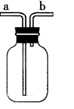
(4) (实验讨论)
对如图中的C处,甲、乙两同学都选用如图装置,但对连接方式持有不同意见。甲同学认为:SO2气体应从a处通入集气瓶中。乙同学认为:SO2气体应从b处通入集气瓶中。你认为(填“甲”或“乙”)同学的看法是正确。
-
(5) (联系实际)
SO2对环境的影响较大,为了减少SO2对空气的污染,请你从工业生产的角度提出一种有效可行的措施(用文字表述):。
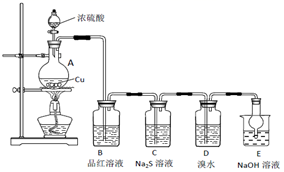
-
(1) A中发生反应的化学方程式为。
-
(2) B中的现象是。
-
(3) C中出现淡黄色沉淀,反应中Na2S做 (填“氧化剂”或“还原剂”)。
-
(4) D溴水褪色,该反应S元素的价态变化是由+4价变为价。
-
(5) 某同学认为D中换成H2O2溶液也可以实现上述硫元素的价态转化,并通过实验进一步证明了他的观点。实验方案和现象为:取D中反应后的溶液于试管中,。
-
(6) E的作用是,离子方程式为。
-
(7) 上述实验体现SO2 的性质有。
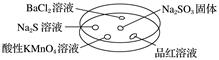
下表中对实验现象的描述或所做的解释错误的是( )
| 选项 | 实验现象 | 解释 |
| A | BaCl2溶液变浑浊 | SO2与BaCl2溶液反应产生了BaSO3沉淀 |
| B | Na2S溶液变浑浊 | SO2与Na2S溶液反应产生了S单质 |
| C | 酸性KMnO4溶液褪色 | SO2具有还原性 |
| D | 品红溶液褪色 | SO2具有漂白性 |
 SO3
SO3  H2SO4
B . Cu2(OH)2CO3
H2SO4
B . Cu2(OH)2CO3  CuSO4(aq)
CuSO4(aq) 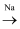 Cu
C . SiO2
Cu
C . SiO2  Si
Si  SiCl4
SiCl4  Si
D . Mg(OH)2
Si
D . Mg(OH)2  MgCl2(aq)
MgCl2(aq)  Mg
Mg
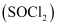 在农药、制药行业中用途广泛。某化学研究性学习小组通过查阅资料,设计了如下图所示装置来制备
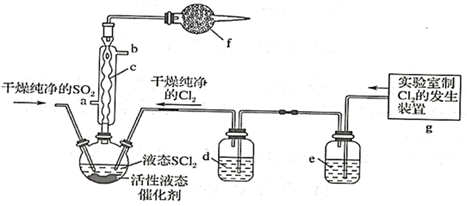
在农药、制药行业中用途广泛。某化学研究性学习小组通过查阅资料,设计了如下图所示装置来制备 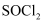 。
。 
已知:① 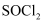 是一种液态化合物,沸点为77℃
是一种液态化合物,沸点为77℃
② 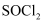 遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生
遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生
③实验室合成 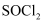 原理:
原理: 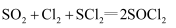
请回答以下问题:
-
(1) 仪器c的名称是,f中的最佳试剂是(填字母符号)。
A.碱石灰 B.浓硫酸 C.
 溶液 D.无水氯化钙
溶液 D.无水氯化钙 -
(2) 实验室用浓盐酸与
 粉末反应制
粉末反应制  的化学方程式为。
的化学方程式为。
-
(3)
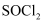 与水反应的化学方程式为。
与水反应的化学方程式为。
-
(4) 下列三种制备
 的方案中最佳选择是.
的方案中最佳选择是. 方案
甲
乙
丙
发生装置
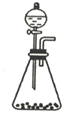
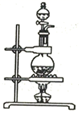
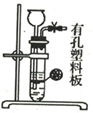
所选试剂
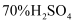 和
和  粉末
粉末 铜片
铜片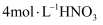 和
和  粉末
粉末 -
(5) 装置g中产生的
 经过e、d后进入三颈烧瓶,e中的试剂为。
经过e、d后进入三颈烧瓶,e中的试剂为。
-
(6) 实验结束后,将三颈烧瓶中混合物分离开的实验操作是(已知
 的沸点为50℃);若反应中消耗
的沸点为50℃);若反应中消耗  的体积为
的体积为 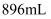 (已转化为标准状况,
(已转化为标准状况,  足量),最后得到
足量),最后得到 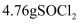 ,则
,则 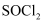 的产率为(已知产率=
的产率为(已知产率=  ×100%)。
×100%)。

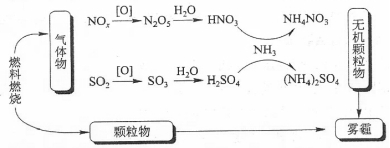
 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和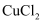 的混合溶液中回收
的混合溶液中回收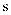 , 其转化如下图所示(
, 其转化如下图所示(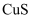 不溶于水)。下列说法中,错误的是( )
不溶于水)。下列说法中,错误的是( )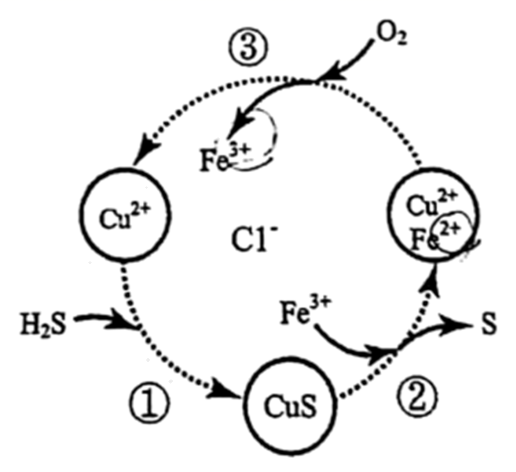
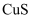 的反应为
的反应为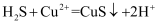 B . 过程②中,
B . 过程②中, 作氧化剂
C . 过程③中,各元素化合价均未改变
D . 回收S的总反应为
作氧化剂
C . 过程③中,各元素化合价均未改变
D . 回收S的总反应为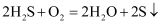
 通入品红溶液中,待溶液褪色后,加热,溶液恢复原色,说明
通入品红溶液中,待溶液褪色后,加热,溶液恢复原色,说明 的漂白是可逆的
的漂白是可逆的
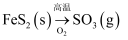 B .
B . 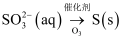 C . 稀
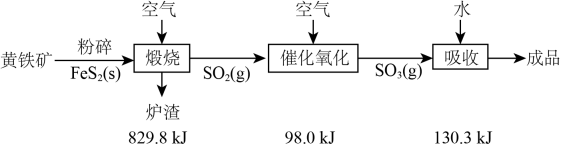
C . 稀 D .
D . 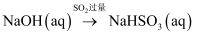
已知:催化氧化阶段的反应是可逆反应。下列说法错误的是( )
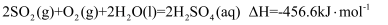 D . 生成
D . 生成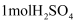 , 上述流程放出的总热量为
, 上述流程放出的总热量为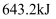
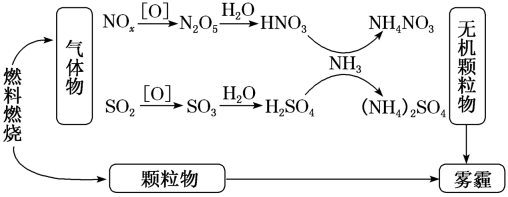
-
(1) 雾霾中含有多种物质,其中属于盐类是(填写名称);图中的电解质有种。
-
(2)
 在水中的电离方程式是:;把稀硫酸滴入氢氧化钡溶液中,反应的离子方程式是。
在水中的电离方程式是:;把稀硫酸滴入氢氧化钡溶液中,反应的离子方程式是。
-
(3) 下列物质属于电解质的是____(填字母)。A .
 B .
B .  C .
C .  D .
D . 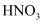
-
(4) 某白色固体中含有
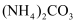 、
、 、
、 , 若只取用一次样品,在同一个容器中检验出3种阴离子,所用的试剂及顺序是。
, 若只取用一次样品,在同一个容器中检验出3种阴离子,所用的试剂及顺序是。
- 下列不属于仿生技术的是 ( ) A.
- 右图表示正常人肝组织细胞的结构示意图,其中①②③④分别表示人体内的液体成分。下列说法中正确的是
- 下列各句中,没有语病的一项是() A.著名学者李明关于切实加强舆论监督功能、依法保障公民权益的文章在社会上引起强烈反响,
- 1978年11月,安徽省凤阳县小岗村18位农民在契约中表示“坐牢杀头也甘心”;1979年,听取设立特区的汇报时指示“杀出
- 现在,越来越多的学生开始意识到学习英语的重要性,但是一些学生发现在日常生活中很少有说英语的机会。假设你校学生会决定举办一
- 将7.6 g氢氧化钠和氢氧化钾的固体混合物溶于水,配成250 mL溶液,从中取出20 mL,用0.5 mol·L-1的硫
- 在人的个体发育中,一个受精卵能形成一个复杂的人,主要是下列哪一生理过程在起作用?( ) A. 细胞分裂
- (05上海卷)B、下面是以小麦为材料所进行的实验,请回答有关问题。(1)将发芽的种子研磨液置于试管中,加入班氏试剂,并_
- Jane hopes to become a friend of _______ shares her interest
- 在国际单位制中,力学的三个基本单位是:( )A.N m s B.kg m s C.N k
- 2005年10月12日“神舟六号”载人飞船成功发射,是我国航天史上又一座新的里程碑,标志着我国在攀登世界科技高峰的征程上
- 人们面对人口、资源、环境之间日益加剧的矛盾而进行的思考不可回避地触及了具有哲学性质的问题。这说明 A.哲学的智慧源于生活
- 在苍茫的大海上,狂风卷集着乌云。在乌云和大海之间,海燕像黑色的闪电,在高傲的飞翔。 一会儿翅膀碰着波浪,一会儿箭
- (二)文学类文本阅读(本题共3小题,14分) 阅读下面的文字,完成4—6题。(14分) 双琴祭 梁晓声 ①那两棵树,最适
- 已知:SO32-+I2+H2O=SO42-+2I-+2H+。某溶液中可能含有Na+、NH4+、Fe2+、K+、I-、SO
- 若关于的不等式组的解集不是空集,则实数的取值范围是( ).A. B. C. D.
- 函数y=+的定义域是() A.(0,2] B.(0,2) C.(1,2) D.[1,2)
- 在探究共点力的合成法则实验中,为使橡皮筋沿竖直方向伸长,那么互成角度的两弹簧秤所施的力 F1和F2必须( ) A.
- 地球自转一周的时间是:( ) A.365天 B.30天 C
- 世界第三大宗教是( )。 A.基督教 B.伊斯兰教



