氯水、氯气的漂白作用 知识点题库
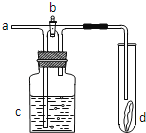
如图所示,从a处通入氯气.若打开活塞b,d处的有色布条不褪色;若关闭活塞b,d处的有色布条褪色.下列判断正确的是( )
-
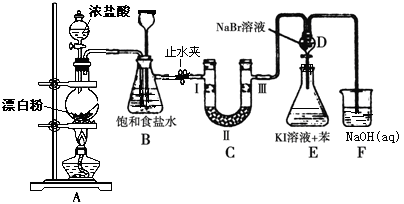
(1) 写出A装置生成氯气的化学反应方程式。
-
(2) 装置B除及吸收HCl外还有两个作用, 请写出: ,。
-
(3) 装置C的实验目的是验证氯气是否具有漂白性, 为此C中Ⅰ、Ⅱ、Ⅲ依次放入物质的组合是(填编号)。
编号
1
2
3
4
Ⅰ
干燥的有色布条
湿润的有色布条
干燥的有色布条
湿润的有色布条
Ⅱ
碱石灰
无水氯化钙
硅胶
浓硫酸
Ⅲ
湿润的有色布条
干燥的有色布条
湿润的有色布条
干燥的有色布条
-
(4) 设计装置D、E的目的是比较氯、溴、碘的非金属性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是该现象(填“能”或“不能”)说明溴的非金属性强于碘,原因是。
-
(5) 有人提出,装置F中可改用足量的Na2S2O3溶液吸收余氯,试写出相应的离子方程式:。
选项 | 现象或事实 | 解释 |
A | 用热的纯碱溶液洗去油污 | Na2CO3可直接和油污反应 |
B | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2 与空气中的CO2反应生成CaCO3 |
C | 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 | K2CO3与NH4Cl反应生成氨气会降低肥效 |
D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含有Cu2+的溶液中置换出铜 |
 、NO
、NO  ),得到NO、SO2脱除率如图,下列说法错误的是( )
),得到NO、SO2脱除率如图,下列说法错误的是( )

 +3Cl-
B . SO2脱除率高于NO的原因可能是SO2在水中的溶解度大于NO
C . 依据图中信息,在80 min时,吸收液中n(NO
+3Cl-
B . SO2脱除率高于NO的原因可能是SO2在水中的溶解度大于NO
C . 依据图中信息,在80 min时,吸收液中n(NO  )∶n(Cl-)=2∶3
D . 随着脱除反应的进行,吸收剂溶液的pH逐渐减小
)∶n(Cl-)=2∶3
D . 随着脱除反应的进行,吸收剂溶液的pH逐渐减小
-
(1) 写出下列物质的化学式:漂白粉的主要成分
-
(2) ①氯气与铁反应的化学方程式
-
(3) 氯气与水反应的化学方程式
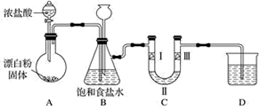
已知:装置 A 是氯气的发生装置,反应的化学方程式为 Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O。据此回答下列问题:
-
(1) 装置 B 中饱和食盐水的作用是。
-
(2) 装置 C 的作用是验证氯气是否具有漂白性,则装置 C 中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是:湿润的有色布条、无水氯化钙、干燥的有色布条,请你推测Ⅰ、Ⅲ处的现象依次为,。
-
(3) 装置 D 的作用是,则烧杯中的溶液是,写出所发生反应的化学方程式:。
|
消毒剂类型 |
成分 |
使用主要注意事项 |
|
含氯消毒剂 |
①84消毒液,有效成分NaClO ②漂白粉,有效成分Ca(ClO)2 |
对织物有漂白作用,不能与洁厕灵混用 |
|
醇类消毒剂 |
乙醇含量为70%-80% |
易燃,远离火源 |
|
过氧化物类消毒剂 |
①过氧化氢消毒剂 ②过氧乙酸消毒剂 |
有腐蚀性,对眼睛、粘膜和皮肤有刺激性,有灼伤危险,受热易分解 |
据信息回答问题:
-
(1) 下列说法错误的是____(填标号)。A . 明矾可用作自来水的消毒剂 B . 浓度为95%的酒精消毒效果比75%的医用酒精好 C . 漂白粉既可以漂白棉、麻、纸张,又可作游泳池及环境的消毒剂 D . 含氯消毒剂和过氧化物类消毒剂的消毒原理均是利用了它们的强氧化性 E . 过氧化物类消毒剂对眼睛、粘膜和皮肤有刺激性,配制和使用时建议佩戴口罩、防护镜和手套
-
(2) 84消毒液不能与洁厕灵(主要成分为盐酸)混用,若混用会产生氯气而使人中毒,请写出该反应的离子方程式。
-
(3) 双氧水消除采矿业废液中所含氰化物(KCN)的化学方程式为:KCN+H2O2+H2O=A+NH3↑,生成物A的化学式为。若标准状况下有44.8L氨气生成,则转移的电子数为,反应中被还原的元素是。
| 选项 | 加入物质 | 现象 | 解释或离子方程式 |
| A | AgNO3溶液 | 有白色沉淀生成 | Cl-+Ag+=AgCl↓ |
| B | 石蕊试液 | 显红色 | 氯水中有盐酸、次氯酸 |
| C | CaCO3 | 有气体放出 | CO |
| D | 有色布条 | 有色布条褪色 | Cl2有漂白性 |
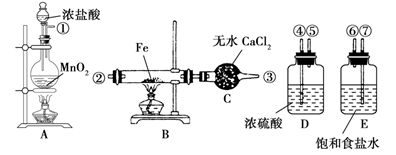
-
(1) 按照气体流向从左到右的顺序连接仪器(填仪器接口):
①接,接,接②。
-
(2) A装置的烧瓶中发生反应的离子方程式为,B装置中发生反应的化学方程式为。
-
(3) D装置的作用是;E装置的作用是。
-
(4) 实验开始时,应先点燃(填“A”或“B”)处的酒精灯。
-
(5) 工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学方程式为,已知浓盐酸和次氯酸钙能发生如下反应:Ca(ClO)2+4HCl(浓)= CaCl2+2Cl2↑+2H2O。用贮存很久的漂白粉与浓盐酸制得的氯气中,可能含有的杂质气体是 (填序号)。①CO2②HCl ③H2O ④H2
A.①②③ B.②③④ C.②③ D.①④
| 选项 | 实验操作及现象 | 实验结论 |
| A | 分别向碳酸钠和碳酸氢钠固体中加入稀盐酸 | 有气泡产生的是碳酸氢钠固体 |
| B | 向紫色石蕊溶液中加入新制氯水,溶液先变红,随后褪色 | 新制氯水中含有氯气分子 |
| C | 向淀粉﹣KI溶液中通入氯气,溶液变成蓝色 | 氧化性:Cl2>I2 |
| D | 向某溶液中加入AgNO3溶液,有白色沉淀生成 | 该溶液中一定含有Cl- |
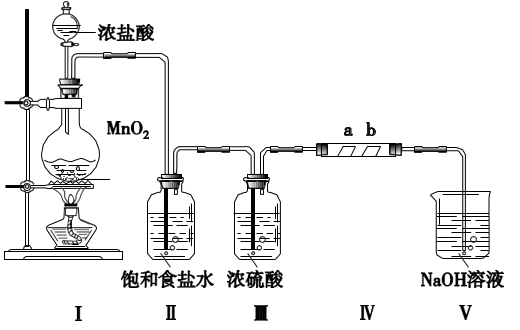
-
(1) 装置I可用于制取Cl2 , 写出该反应的化学方程式。
-
(2) 装置II的作用是。
-
(3) 装置IV中a处红色纸条无明显变化,b处红色纸条褪色,同学猜测使b处红色纸条褪色的物质是。
-
(4) 装置V中NaOH溶液可吸收Cl2并制得漂白液(有效成分:NaClO),写出该反应的离子方程式。
-
(5) 该小组同学查阅资料,发现:
①NaClO溶液具有氧化性,能使红色纸条褪色
②溶液的pH会影响NaClO溶液的漂白效果
该小组同学利用市售“84”消毒液(主要成分:NaClO)探究不同pH下红色纸条褪色的情况,实验如下:
实验方案
实验现象
1.将市售“84”消毒液稀释至溶液的pH=12.
2.取20mLpH=12的稀释液各3份,分别用H2SO4溶液将pH调至10、7和4(液体积变化忽略不计)。
3.分别放入大小相同的红色纸条。
pH=10
10min后,红色纸条基本不褪色;4h后红色褪去。
pH=7
10min后,红色纸条颜色变浅;4h后红色褪去。
pH=4
10min后,红色纸条颜色变得更浅;4h后红色褪去。
已知:溶液中HClO、ClO-物质的量分数(a)随溶液pH变化的关系如下图所示:
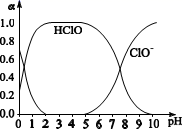
①由实验现象可知:溶液的pH在4~10范围内,pH越大,红纸褪色。
②结合图像分析pH=7和pH=4的溶液,现象差异的原因。
③结合实验现象和图像可知,氧化性:HClONaClO(填“>”或“<”)。“84”消毒液主要成分是NaClO而不是HClO,因为HClO不稳定,不易保存。写出HClO见光分解的化学方程式 。
综上所述,HClO能使红色纸条褪色,“84”消毒液在酸性环境下漂白效果更佳。
 此图为与实验有关的图标,表示实验时需要佩戴护目镜
B . 保存
此图为与实验有关的图标,表示实验时需要佩戴护目镜
B . 保存 溶液时需加入少量
溶液时需加入少量 粉
C . 新制氯水需要避光保存
D . 实验室中未用完的钠、钾、白磷等放回原试剂瓶
粉
C . 新制氯水需要避光保存
D . 实验室中未用完的钠、钾、白磷等放回原试剂瓶
①氯气 ②液氯 ③新制氯水 ④氯气溶解在四氯化碳溶液中 ⑤盐酸 ⑥盐酸与少量漂白粉的混合溶液
- 下面的实验仪器省去了固定装置,请根据要求回答问题:(1)甲图中仪器①的名称为______ ____。 (2)乙图中
- “花气袭人知骤暖,鹊声穿树喜新晴”描述了春天晴暖、鸟语花香的山村美景。下列从微观角度对“花气袭人知骤暖”的解释最合理的
- 1体积某烃的蒸气完全燃烧生成的水蒸气比CO2多1体积。0.2摩尔该烃完全燃烧,其生成物被碱石灰完全吸收增重78克,则该烃
- 四大洋中,跨经度最多、面积最小、深度最浅的是 A.太平洋 B.大西洋
- 人体血液内的血红蛋白(Hb)易与O2结合生成HbO2, 因此具有输氧能力,CO吸入肺中发生反应:CO+HbO2O2+Hb
- 如图8-1-5所示,AB是某个点电荷的一根电场线,在电场线上O点由静止释放一个负电荷,它仅在电场力作用下沿电场线向B运动
- 5.下列有关细胞学说的叙述,正确的是: A.英国科学家罗伯特·胡克是细胞的发现者,也是细胞学说的主要提出者 B.细胞是构
- 下列是芳香族化合物A、B、C、D、E的转化关系,其中A、E分子式分别是C9H8O和C9H8O2,E分子中除苯环外还含有一
- 下列哪项不是植物生长需要的最多的三种无机盐A.铁 B.磷
- 利用图2-13所示装置收集以下8种气体(图中烧瓶的位置不得变化)。 收集气体 图2-13①H2 ②Cl2
- 如图所示,①中多边形(边数为12)是由正三角形“扩展”而来的,②中多边形是由正方形“扩展”而来的,…,依此类推,则由正八
- 人类和环境是对立统一的关系,人类从环境中获取物质和能量,同时又通过消费活动把废弃物排放到环境中去,人类作用于环境,环境对
- 古希腊历史学家希罗多德曾记述一名希腊人对波斯王薛西斯的讲话:“希腊人虽然是 自由的,但他们并不是任何事情都是自由的,他们
- 如图,在小山的东侧A点有一个热气球,由于受西风的影响,以30米/分的速度沿与地面成75°角的方向飞行,25分钟后到达C处
- 下列几种动物行为,不属于学习行为的是 A.失去雏鸡的母鸡抚爱小猫 B.蚯蚓走“T”形迷宫
- 一个从地面竖直上抛的物体,它两次经过同一较低a点的时间间隔为Ta,两次经过另一较高的b点的时间间隔为Tb,则ab两点间的
- 在“碰撞中的动量守恒”实验中,已测得A、B两小球质量mA<mB,由实验所得结果如图8—7—7所示,图中M、P、N为
- 下图中,若甲代表水和二氧化碳,则( )A.Ⅱ是呼吸作用,乙是有机物和氧气,Ⅰ是光合作用 B.Ⅱ是光合作用,乙是二氧化
- 18.下列各句,没有语病、句意明确的一句是( )(3分)A.这次招聘,一半以上的应聘者曾多年担任外资企业的中高层管
- 右图为下丘脑中某细胞的部分膜结构示意图,下列叙述正确的是( ) A.若此图为突触后膜局部结构,则兴奋经过此处时的信
 +2H+=H2O+CO2↑
+2H+=H2O+CO2↑


