物质检验实验方案的设计 知识点题库
实验I:用砂纸擦去镁条表面氧化膜,将其放入盛适量滴有酚酞的饱和碳酸氢钠溶液的烧杯中,迅速反应,产生大量气泡和白色不溶物,溶液的浅红色加深。
-
(1) 该同学对反应中产生的白色不溶物做出如下猜测:
猜测1:白色不溶物可能为 。
猜测2:白色不溶物可能为MgCO3
猜测3:白色不溶物可能为碱式碳酸镁[xMg(OH)2•yMgCO3]
-
(2) 为了确定产物成分(包括产生的气体、白色不溶物及溶液中溶质),进行以下定性实验。请填写表中空白:
实验序号
实 验
实验现象
结 论
实验Ⅱ
将实验I中收集到的气体点燃
安静燃烧,火焰呈淡蓝色
气体成分为①
实验Ⅲ
将实验I中的白色不溶物滤出、洗涤,取少量加入足量②
③
白色不溶物中含有MgCO3
实验Ⅳ
取实验Ⅲ中的滤液,向其中加入适
量④稀溶液
产生白色沉淀,溶液红色变浅
溶液中存在CO32-离子
-
(3)
为进一步确定实验I中白色不溶物的成分,进行以下定量实验,装置如图所示:
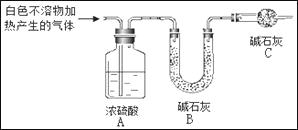
称取干燥、纯净的白色不溶物 4.52 g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验后装置A增重0.36 g,装置B增重1.76 g。
①装置C的作用是;
②白色不溶物的化学式为。
-
(4) 根据以上(2)及(3)的定性定量实验,写出镁与饱和碳酸氢钠溶液反应的化学方程式。
-
(1) 此瓶“84”消毒液的说明书上这样写道:“本品为无色液体,呈碱性……”,请你推测它的有效成分( )(填序号)。A . Cl2 B . H2O2 C . NaClO D . KMnO4
-
(2) 该化学兴趣小组的同学在瓷碗中盛放20 mL的“84”消毒液,露置在阳光充足的室内,他们对“84”消毒液的消毒效果和组成成分的变化进行了研究。得出数据如下:
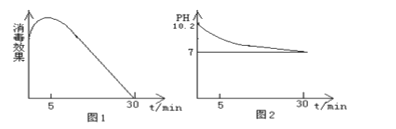
从数据图1和图2可得知“84”消毒液暴露在空气中半小时后,“84”消毒液中的主要溶质是,用化学方程式或离子方程式表示其中变化的主要原因
、、。
-
(3) 该化学兴趣小组的同学选了紫色石蕊试液对“84”消毒液的性质进行实验检验,请你帮助他们完成实验报告:
实验操作
预期现象
结论
-
(4) 该化学实验小组同学上网查询有关“84”消毒液的信息时,发现这样一则消息:有一家庭主妇把抗SARS用的“84”消毒液和清洁剂(呈酸性、含Cl-)都倒出一些混合在一起,进行刷洗。一会儿,她就晕倒在房间里。这几位同学感到迷惑不解。请你用离子方程式帮助他们解开这一悬念。
①向其中加入过量盐酸,有气体生成,并得到无色透明溶液;
②在①所得溶液中加入过量氢氧化钡溶液,产生白色沉淀,过滤;
③在②所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀.
根据上述实验回答下列问题:
(1)原溶液中一定不存在的离子是 ;
(2)原溶液中一定存在的离子是 ;
(3)原溶液中可能存在的离子是 ,
(4)请写出①和③中发生反应的离子方程式
I.NH4+含量的测定
采用蒸馏法,蒸馏装置如图所示.
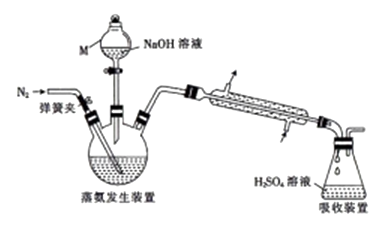
相关的实验步骤如下:
①准确称取58.80g晶体X,加水溶解后,将溶液注入圆底烧瓶中;
②准确量取50.00mL 3.0300mol•L-1H2SO4溶液于锥形瓶中;
③向三颈烧瓶中加入足量NaOH溶液,加热蒸馏;
④用0.120mo l•L-1 NaOH标准溶液滴定锥形瓶中过量的硫酸,滴定终点时消耗25.00mL NaOH标准溶.
-
(1) 仪器M的名称为。
-
(2) 步骤③中,发生的氧化还原反应的化学方程式为。蒸氨结束后,为了减少实验误差,还需要对直形冷凝管进行“处理”。“处理”的操作方法是。
-
(3) 步骤④中,若振荡时锥形瓶中有液体溅出,则所侧得的n(NH4+)的值将(填“偏大”、“偏小”或“不变”).
-
(4) Ⅱ.SO42-的测定
采用重量分析法,实验步骤如下:
①另准确称取58.80g晶体X于烧杯中,加水溶解,边搅拌边加入过量的 BaCl2溶液;
②将得到的溶液用无灰滤纸(灰分质量很小,可忽略)过滤,洗涤沉淀3~4次;
③用滤纸包裹好沉淀取出,灼烧滤纸包至滤纸完全灰化;
④继续灼烧沉淀至恒重.得沉淀质量69.90g.
步骤①中,判断 BaCl2溶液已过量的实验操作和现象是。
-
(5) 步骤②中,采用冷水洗涤沉淀,其主要目的是.
-
(6) 综合实验I、Ⅱ,通过计算得出晶体X的化学式为,实验Ⅰ的步骤①中,溶液中离子浓度由大到小的顺序为。
| 实验目的 | 实验操作 | |
| A | 配制1.0mol/LCuSO4溶液 | 把25g胆矾晶体溶于水配成100mL溶液 |
| B | 证明某溶液中含有SO42- | 向该溶液中滴入BaCl2溶液 |
| C | 实验室制大量CO2 | 向稀硫酸中加入大理石 |
| D | 制备Fe(OH)3胶体 | 将饱和的FeCl3溶液滴加到热NaOH溶液中 |
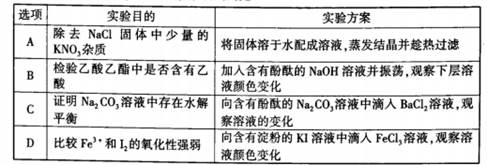
| 实验操作 | 现象 | 结论 | |
| A | 向AgNO3和AgCl的混合浊液中滴加0.1mol·L-1KI溶液 | 生成黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
| B | 向某溶液中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色沉淀 | 原溶液中一定含有SO42- |
| C | 向盛有某溶液的试管中滴加NaOH溶液并将湿润的红色石蕊试纸置于试管口 | 试纸颜色无明显变化 | 原溶液中不含NH4+ |
| D | 向某溶液中滴加KSCN溶液 | 溶液未变血红色 | 原溶液中不含Fe3+ |
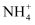 、Na+、Mg2+、Fe2+、
、Na+、Mg2+、Fe2+、  、Cl−、Br−、
、Cl−、Br−、  、SiO32-和HCO3-离子中的若干种。取100 mL该溶液进行如下实验:
、SiO32-和HCO3-离子中的若干种。取100 mL该溶液进行如下实验: 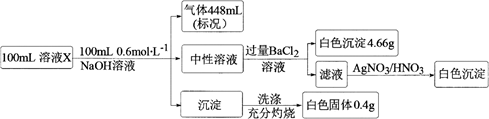
下列说法正确的是( )
 、SiO32- , 可能有Na+、Fe2+
B . 溶液X中加NaOH后,所得沉淀的成分可能有两种
C . 溶液X中c(Cl−)≤0.2 mol·L−1
D . 溶液X可能是由NH4HSO4、MgCl2按物质的量之比2∶1混合再溶于水配制而成
、SiO32- , 可能有Na+、Fe2+
B . 溶液X中加NaOH后,所得沉淀的成分可能有两种
C . 溶液X中c(Cl−)≤0.2 mol·L−1
D . 溶液X可能是由NH4HSO4、MgCl2按物质的量之比2∶1混合再溶于水配制而成
-
(1) I.NO能被灼热的铁粉还原为N2 , 同时生成FeO,利用下列装置模拟该反应。
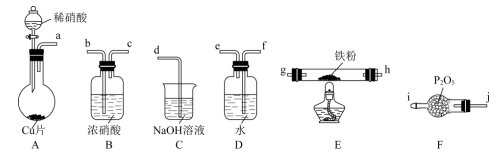
已知:①浓硝酸可将NO氧化为NO2;②NaOH溶液能与NO2反应,不与NO反应。
打开A装置分液漏斗活塞,烧瓶中观察到的实验现象有:铜片表面出现无色气泡,铜片逐渐变小、、烧瓶中溶液由无色变为蓝色。
-
(2) 上述装置接口的连接顺序为:a→→→→→g→h→b→c→d(按气流方向,用小写字母表示)。
-
(3) 装置B的作用是。
-
(4) 装置E中反应的化学方程式为。
-
(5) II.已知:(NOx)能与Na2O2反应;NO2和Na2O2都有较强氧化性。为探究NO2与Na2O2反应的产物,提出如下假设:
假设①NO2氧化Na2O2;假设②Na2O2氧化NO2
甲同学设计如图所示实验装置:
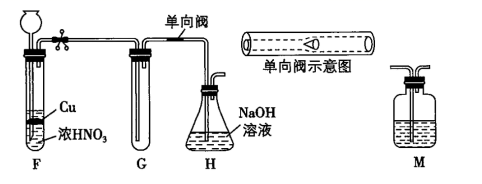
请回答下列问题:
甲乙两同学对假设分别进行了验证:
实验操作
现象
结论
甲同学
待试管G中收集满气体,向其中加入适量Na2O2粉末,塞紧塞子,轻轻振荡试管,观察现象;并将带火星的木条迅速伸进试管,观察。
红棕色气体迅速消失;木条复燃
假设①正确
乙同学
在F、G之间增加一个M洗气瓶,目的是,重复甲同学的实验操作。
红棕色气体迅速消失,带火星的木条未复燃
假设②正确
请做出正确判断,写出NO2和Na2O2反应的化学方程式。
-
(6) 图中单向阀在实现气体单向流通的同时,还有一个作用是。
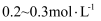 )、医用酒精(乙醇体积分数为
)、医用酒精(乙醇体积分数为 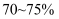 )
)
-
(1) Ⅰ:探究84 消毒液的成分
NaClO 溶液呈碱性的原因是(用离子方程式表示)。
-
(2) 常温下
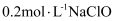 溶液的pH范围是_______(填标号)。
溶液的pH范围是_______(填标号)。 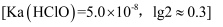 A . 7.0~8.0 B . 10.0~11.0 C . 13.0~14.0
A . 7.0~8.0 B . 10.0~11.0 C . 13.0~14.0 -
(3) 实测该84消毒液
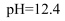 ,在瓶口能闻到刺激性气味。则该 84消毒液成分中,除了NaCl、NaClO,还含有(填化学式)。
,在瓶口能闻到刺激性气味。则该 84消毒液成分中,除了NaCl、NaClO,还含有(填化学式)。
-
(4) 84消毒液露置于空气中,消毒效果先增强后降低。消毒效果增强的原因是。
-
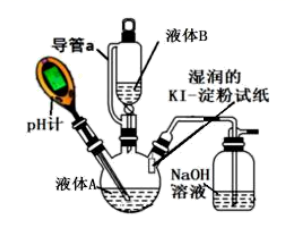
(5) Ⅱ:探究 84 消毒液能否与医用酒精混用 实验装置如图所示。
序号
液体A
液体B
现象
ⅰ
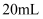 (
( 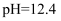 )的84消毒液
)的84消毒液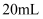 蒸馏水
蒸馏水溶液中无明显现象;溶液
 变为12.0;
变为12.0; 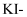 淀粉试纸在
淀粉试纸在 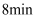 时变蓝,
时变蓝, 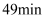 时蓝色完全褪去
时蓝色完全褪去ⅰ
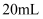 (
( 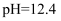 )的84消毒液
)的84消毒液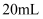 医用酒精
医用酒精产生气泡,颜色无明显变化;溶液
 升高到13.1,
升高到13.1, 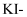 淀粉试纸在
淀粉试纸在 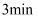 时变蓝,
时变蓝, 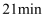 时蓝色完全褪去
时蓝色完全褪去导管 a 的作用是。
-
(6) ①实验ⅰ的目的是。
②判断实验ⅱ中生成了
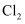 的依据是。
的依据是。 -
(7) 需补充以下实验ⅲ,才能说明反应中是否有 NaOH 生成。填写表中空白完成实验设计。
序号
液体A
液体B
现象
ⅲ
的NaOH溶液
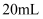 医用酒精
医用酒精溶液
 升高到12.6
升高到12.6结论:医用酒精可与84消毒液发生反应并有少量
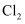 和NaOH 生成,二者不可混用。
和NaOH 生成,二者不可混用。
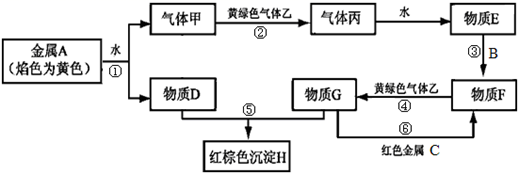
请根据以上信息回答下列问题:
-
(1) 写出气体乙的化学式。
-
(2) 写出反应①的化学方程式:。
-
(3) 写出反应⑥的离子方程式:。
-
(4) 检验物质F溶液中含有金属B元素的阳离子的方法为。

-
(1) 实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离。设计此步操作的目的是。
-
(2) 将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为。
-
(3) 用F向E中鼓入空气的现象是。
-
(4) 一段时间后,C中白色沉淀溶解,其原因是。
-
(5) 装置D的作用是。
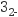 D . 石灰水敞口存放,出现白色固体:2OH- + CO2 =CO
D . 石灰水敞口存放,出现白色固体:2OH- + CO2 =CO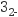 + H2O
+ H2O
资料:①锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3  +2H2O=2
+2H2O=2  +MnO2↓+4OH-
+MnO2↓+4OH-
②酸性条件下的氧化性:KMnO4>KIO3>I2
-
(1) I.KMnO4的制备
从A~D中选择合适的装置制备KMnO4 , 正确的连接顺序是a→(按气流方向,用小写字母表示);装置A中m的作用是。
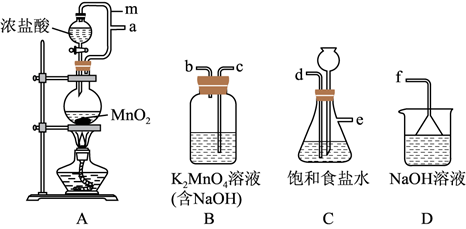
-
(2) 若没有使用装置C,造成的影响是。
-
(3) II.KMnO4性质探究
取适量制取的KMnO4溶液稀释至约0.01mol/L(用硫酸酸化至pH=1),取配制好的KMnO4溶液2mL于试管中,逐滴滴加0.1mol/LKI溶液,KMnO4紫色溶液迅速变为棕褐色悬浊液,然后沉淀逐渐消失,最终溶液变为棕黄色。
最终溶液呈现踪黄色推测生成了(写化学式)。
-
(4) 实验小组对初始阶段的产物成分进行探究:
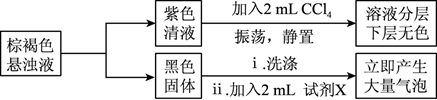
①黑色固体是MnO2 , 试剂X是(写化学式)。
②在“紫色清液"中存在
 ,写出生成
,写出生成  的离子方程式。
的离子方程式。③下列实验方案中,可用于检验“紫色清液"中是否存在
 的是(填序号)。
的是(填序号)。A.用洁净的玻璃棒随取紫色清液滴在淀粉-KI试纸上,观察试纸是否变蓝色。
B.取少量紫色清液于试管中,向其中加入几滴淀粉溶液,溶液不变蓝,再加入过量NaHSO3溶液,观察溶液是否变色。
C.取少量紫色清液于试管中,向其中加入稀硝酸酸化,再加入几滴硝酸银溶液,观察是否生成黄色沉淀。
-
(5) 探究实验II中棕褐色沉淀消失的原因:
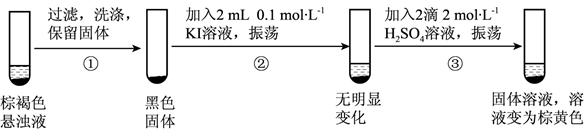
用离子方程式解释步骤③中固体消失的原因。
-
(6) 由上述实验可知,KMnO4的还原产物与有关。
实验操作及现象 | 结论或解释 | |
A | 向Na2SO3溶液中,加入BaCl2溶液,产生白色沉淀,过滤洗涤后,向所得沉淀中加入足量稀硝酸,沉淀不溶解 | Na2SO3溶液已变质 |
B | 向酸性KMnO4溶液中滴加H2O2溶液,紫红色褪去 | H2O2具有还原性 |
C | 向Al2(SO4)3溶液中逐滴加入NaOH溶液至过量,先生成白色沉淀,后沉淀消失 | Al(OH)3具有两性 |
D | 向饱和NaHCO3溶液中滴加饱和CaCl2溶液,既产生白色沉淀又生成无色气体 | Ca2++2HCO |
-
(1) I.确定该蛋白质中的某些组成元素
为确定该蛋白质中含氮元素,将样品中有机氮转化成铵盐,能证明铵盐存在的实验方法是。
-
(2) 为确定该蛋白质中含碳、氢、硫三种元素,采用如图装置进行探究,通入氧气使样品在装置A中 充分燃烧,并使其产物依次缓缓通过其余装置。
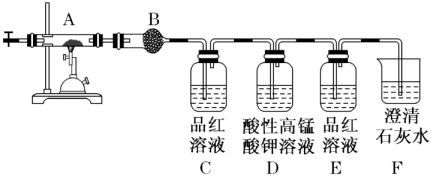
①装置B中的试剂是。
②装置D的作用是。
③当装置B、C、E、F依次出现下列现象:,品红溶液褪色,,出现白色浑浊;可证明燃烧产物中含有H2O,SO2>CO2 , 结论:该蛋白质中含碳、氢、硫、氮等元素。
-
(3) II.为测定该蛋白质中硫元素的质量分数,小组取蛋白质样品充分燃烧,先用足量碘水吸收二氧化硫, 再取吸收液,以淀粉为指示剂,用硫代硫酸钠溶液滴定过量的碘。已知:2
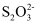 +I2=
+I2=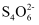 +2I-
+2I-写出二氧化硫与碘水反应的化学方程式:。
-
(4) 滴定终点的现象为。
-
(5) 取蛋白质样品m g进行测定,采用c1 mol·L-1的碘水V1 mL进行吸收,滴定过量的碘样时消耗c2 mol·L-1硫代硫酸钠溶液V2mL。该蛋白质中的硫元素的质量分数为。
-
(6) 若燃烧时过量氧气进入吸收液中,可能会导致该蛋白质中的硫元素的质量分数测定值(填“偏大*偏小”或“无影响”)。
选项 | 实验目的 | 实验操作 |
A | 证明加碘食盐中存在 | 向食盐水中加入 |
B | 证明 | 向 |
C | 证明 | 向 |
D | 制备 | 将饱和 |
- 解不等式x(x+1)2(3-x)(x2+2x+2)(2x2+5x+2)<0.
- 生态系统稳定性的原因是 ( ) A.阳光充足
- 读漫画《晕》,回答下列各题。风险性是居民投资理财考虑的一个重要因素。下列投资理财产品的风险性从低到高排序,正确的是(
- 在体积可变的容器中发生反应N2 + 3H2 NH3当增大压强使容器体积缩小时,化学反应速率加快,其主要原因是 A.分子
- 人体的下列免疫活动,由第二道防线完成的是 ( ) A.胃黏膜分
- 某学生参加某高校的自主招生考试,须依次参加A、B、C、D、E五项考试,如果前四项中有两项不合格或第五项不合格,则该考生就
- “波士顿市市长带领10万名儿童在广场上宣誓:我要做一个美国的好公民,保证为全国复兴运动尽自己的一份义务,买东西只在蓝鹰
- 弹簧测力计的钩上分别挂了几个物体,弹簧测力计的读数为10N时,这个物体可能是( )A、一袋方便面 B、一
- 把下面的句子组成前后衔接、意思完整的一段话。(写出句子序号即可)(4分)①像死水一般静止的趣味必定陈腐②我想不仅作者如此
- Researchersfound that people become happier and experience l
- 以下关于细胞核的叙述,正确的是() A.核内存在易被碱性染料染成深色的物质 B.在不同的细胞内,核仁的大小和数量相同 C
- 如图所示,理想变压器原、副线圈的匝数比n1:n2=1:3,次级回路中联入三个均标有“36V,40W”的灯泡, 且均正常发
- StudyingWendy’s menu, I found that many of the items are si
- _____in a well—known university is what everybody wishes for
- . _____ of you comes first will get the ticket.A. Which
- 阅读下面的文字,完成后面题目。 有容之大 回顾近30年中国美术发展历程,真有隔世之感。从那个人人自畏、噤若寒蝉、色调单一
- 下列加点字注音完全正确的一项是: (2分) A.妖娆(ruó) 伫立(chù) 法家拂士(fú)
- 当时,分式无意义,当时,分式的值为0,则( ) A.2 B. C.0
- 材料一:我国外汇储备情况表(单位:万亿美元)年份 2005 2006 2007 2008 2009 外汇储备 0.818
- 19世纪中期,列强侵略激化了中国的社会矛盾,一场轰轰烈烈的农民运动在中国南方兴起。这场运动是 A.太平天国运动B.洋务运

 CaCO3+H2CO3 , 随Ca2+浓度增加,平衡向右移动
CaCO3+H2CO3 , 随Ca2+浓度增加,平衡向右移动
 溶液,取该溶液滴在碘化钾淀粉试纸上
溶液,取该溶液滴在碘化钾淀粉试纸上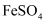 溶液部分被氧化
溶液部分被氧化 溶液
溶液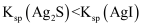
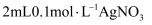 溶液中滴加 1 mL
溶液中滴加 1 mL 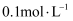 KI再滴加 1 mL
KI再滴加 1 mL 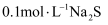 溶液
溶液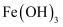 胶体
胶体 溶液滴入NaOH溶液
溶液滴入NaOH溶液


