常见化学电源的种类及其工作原理 知识点题库
伏打电堆(Voltaic pile)的照片和结构如图.它用圆形的锌板、铜板间隔堆积而成.所有的圆板之间夹放几层盐水泡过的布.下列说法正确的是( )
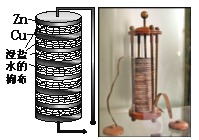
A . 伏打电堆能将电能转化成化学能
B . 锌是正极
C . 盐水是电解质溶液
D . 伏打电堆工作时铜被还原
大力发展电动汽车,可以有效控制空气污染.目前机动车常使用的电池有铅蓄电池、锂电池等.
-
(1) Ⅰ.铅蓄电池充放电的总反应为:PbO2+Pb+2H2SO4
 2PbSO4+2H2O,锂硫电池充放电的总反应为:2Li+S
2PbSO4+2H2O,锂硫电池充放电的总反应为:2Li+S  Li2S.
Li2S. a.放电时,铅蓄电池的负极反应式为.
b.锂硫电池工作时,电子经外电路流向(填“正极”或“负极”).
c.当消耗相同质量的负极活性物质时,锂硫电池的理论放电量是铅蓄电池的倍.
-
(2) Ⅱ.由方铅矿(PbS)制备铅蓄电池电极材料(PbO2)的方法如下:
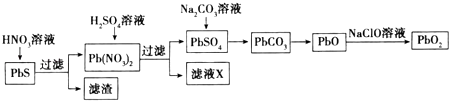
a.油画所用的白色颜料PbSO4置于空气中,遇H2S气体变成黑色PbS,从而使油画的色彩变暗,用H2O2清洗,可使油画“复原”.
①H2O2的作用是.
②已知硫化铅溶于水时存在溶解平衡:PbS(s)⇌Pb2+(aq)+S2﹣(aq),试分析PbS(s)能溶于稀HNO3的原因.
b.滤液X是一种可循环使用的物质,其溶质主要是(填化学式),若X中残留的SO42﹣过多,循环使用时可能出现的问题是.
c.①PbO与次氯酸钠溶液反应可制得PbO2 , 写出该反应的离子方程式.
②以石墨为电极,电解Pb(NO3)2溶液也可以制得PbO2 , 则阳极的电极反应式为;电解时为提高Pb元素的利用率,常在Pb(NO3)2溶液中加入适量Cu(NO3)2 , 理由是.
下列有关电池的说法不正确的是( )
A . 手机上用的锂离子最池属于二次电池
B . 铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
C . 甲醇燃料电池可把化学能转化为电能
D . 锌锰干电池中,锌电极是负极
已知空气﹣锌电池的电极反应为:锌片:Zn+20H﹣﹣2e﹣=ZnO+H20,石墨:02+2H20+4e﹣=40H﹣ . 根据此判断,锌片是( )
A . 负极,并被氧化
B . 负极,并被还原
C . 正极,并被氧化
D . 正极,并被还原
铅蓄电池的总反应式为:PbO2+Pb+2H2SO4  2PbSO4+2H2O据此判断下列叙述正确的是( )
2PbSO4+2H2O据此判断下列叙述正确的是( )
 2PbSO4+2H2O据此判断下列叙述正确的是( )
2PbSO4+2H2O据此判断下列叙述正确的是( )
A . 放电时,H2SO4浓度增加
B . 放电时,负极的电极反应式为:Pb+SO42﹣﹣2e﹣═PbSO4
C . 在充电时,电池中每转移1 mol电子,理论上生成2 mol硫酸
D . 在充电时,阴极发生的反应是PbSO4﹣2e﹣+2H2O═PbO2+SO42﹣+4H+
下列关于化学电源的说法不正确的是( )
A . 我们可以根据硫酸密度的大小来判断铅蓄电池是否需要充电
B . 燃料电池是利用燃料和氧化剂之间的氧化还原反应,将化学能转化为热能,然后再转化为电能的化学电源
C . 普通锌锰干电池中,发生氧化还原反应的物质大部分被消耗后,就不能再使用了
D . 由Ag2O和Zn形成的碱性银锌纽扣电池,发生电化学反应时,Zn作为负极
自2016年1月1日起,无线电动工具中使用的镍镉电池在欧盟全面退市.镍镉电池放电时的总反应为Cd+2NiO(OH)+2H2O═2Ni(OH)2+Cd(OH)2 , 下列说法正确的是( )
A . 电池的电解液为碱性溶液,正极为2NiO(OH)、负极为Cd
B . 放电时,每通过2 mol电子,负极质量减轻112 g
C . 放电时,电子从正极流向电源的负极
D . 充电时,Cd极板应与外电源的正极相接
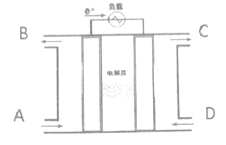
燃料电池利用原电池的工作原理将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能:能有效提高能源利用率,具有广泛的应用前景。某种燃料电池的总反应式是:CH4+2O2+2OH-=CO32-+ 3H2O,装置如下图所示,该电池用金属铂片作电极在两极上分别通甲烷和氧气。请思考回答以下问题:

-
(1) 电解质溶液可能是;阳离子的移动方向:。(“左→右”、“右→左”)
-
(2) D气体通入的电池的极,发生的电极反应式:;A通入的是,发生的电极反应式:。
-
(3) 当该电子流经导线的电子为4mol时,A入口至少需要通入L的气体(标准状态下)。
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。以下说法正确的是( )。
A . 电池工作时,MnO2失去电子
B . 电池工作时,电子由锌经外电路流向MnO2
C . 从反应方程式来看,不使用氢氧化钾,也不影响电流大小
D . 电池的正极反应式为2MnO2(s)+H2O(l)+2e-=Mn2O3(s)+2OH-(aq)
比亚迪纯电动汽车采用一种具有高效率输出、可快速充电、对环境无污染等优点新型电池,其工作原理如图。M电极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,聚合物交换膜只允许Li+通过,而e-不能通过。电池反应式为LixC6+Li1-xFePO4 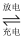 LiFePO4+6C。下列说法错误的是( )
LiFePO4+6C。下列说法错误的是( )
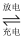 LiFePO4+6C。下列说法错误的是( )
LiFePO4+6C。下列说法错误的是( )
A . 放电时,N极是正极,电极反应式为Li(1-x)FePO4+xLi++xe-=LiFePO4
B . 充电时,Li+通过聚合物交换膜向M极迁移
C . 用该电池电解精炼铜,阴极质量增重19.2g时,通过聚合物交换膜的Li+数目为0.6NA
D . 充电时电路中通过0.5mol e- , 消耗36gC
下列电池不属于化学电池的是( )
A . 铅蓄电池
B . 太阳能电池
C . 锌锰电池
D . 镍镉电池
下列说法正确的是()
A . 通电一段时间后,搅拌均匀,溶液的pH增大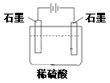 B . 此装置可实现铜的精炼
B . 此装置可实现铜的精炼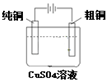 C . 盐桥中的K+移向FeCl3溶液
C . 盐桥中的K+移向FeCl3溶液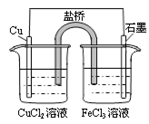 D . 若观察到甲烧杯中石墨电极附近先变红,则乙烧杯中铜电极为阳极
D . 若观察到甲烧杯中石墨电极附近先变红,则乙烧杯中铜电极为阳极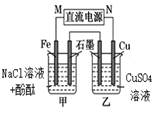
 B . 此装置可实现铜的精炼
B . 此装置可实现铜的精炼 C . 盐桥中的K+移向FeCl3溶液
C . 盐桥中的K+移向FeCl3溶液 D . 若观察到甲烧杯中石墨电极附近先变红,则乙烧杯中铜电极为阳极
D . 若观察到甲烧杯中石墨电极附近先变红,则乙烧杯中铜电极为阳极
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。下图是通过人工光合作用制备HCOOH的原理示意图,下列说法错误的是()
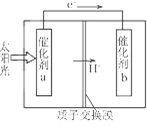
A . 该过程是将太阳能转化为化学能的过程
B . 催化剂a表面发生氧化反应,有O2产生
C . 催化剂a附近酸性减弱,催化剂b附近酸性增强
D . 催化剂b表面的反应是CO2+2H++2e一=HCOOH
锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。
回答下列问题:
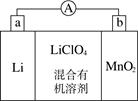
-
(1) 外电路的电流方向是由极流向极。(填字母)
-
(2) 电池正极反应式为。
-
(3) 是否可用水代替电池中的混合有机溶剂?(填“是”或“否”),原因是。
-
(4) MnO2可与KOH和KClO3在高温下反应,生成K2MnO4 , 反应的化学方程式为。
下列有关电池叙述正确的是( )
A . 化学电池的反应本质是复分解反应
B . 铅蓄电池放电时,是电能转化为化学能的过程
C . 锌锰干电池碳棒是负极,锌片是正极
D . 锌锰干电池工作一段时间后锌外壳逐渐变薄
电池是人类生产和生活中的重要能量来源,各式各样的电池的发明是化学对人类的一项重大贡献。下列有关电池的叙述正确的是( )
A . 太阳能电池的主要材料是高纯度的二氧化硅
B . 氢氧燃料电池可将热能直接转变为电能
C . 铅蓄电池充电时也发生了氧化还原反应
D . 氢氧燃料电池工作时,H2在负极上得到电子
燃料电池是一种将燃料所具有的化学能直接转换成电能的化学装置。
-
(1) 以多孔铂为电极,如图甲装置中A、B口分别通入CH3CH2OH和O2构成乙醇燃料电池,则b电极是(填“正极”或“负极”),该电池的负极电极反应式为。
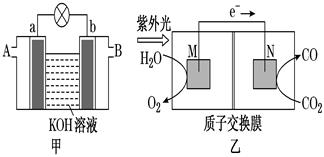
-
(2) 科学家研究了转化温室气体的方法,利用图乙所示装置可以将CO2转化为气体燃料CO,该电池负极反应式为,
-
(3) 铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2 , 电解液为硫酸。该电池总反应式为Pb+PbO2+2H2SO4
 2PbSO4+2H2O。(已知:硫酸铅为不溶于水的白色沉淀,生成时附着在电极上)
2PbSO4+2H2O。(已知:硫酸铅为不溶于水的白色沉淀,生成时附着在电极上) ①该蓄电池放电时,电解质溶液中阴离子移向(填“正极”或“负极”);正极附近溶液的酸性(填“增强”“减弱”或“不变”),当外电路通过1 mol电子时,理论上正极板的质量增加g。
如图为原电池装置示意图:
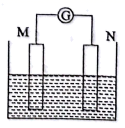
-
(1) 若M为铜片,N为碳棒,电解质溶液为FeCl3溶液,则铜片为极(填“正”或“负”),写出正极反应式。
-
(2) 若M为Pb,N为PbO2 , 电解质为H2SO4溶液,工作时的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出M电极反应式:;该电池工作时,M电极的质量将(填“增加”、“减小”或“不变”)。若该电池反应消耗了0.2 mol H2SO4 , 则转移电子的数目为。
-
(3) 若M、N均为铂片,电解质为KOH溶液,分别从M.、N两极通入CH4和O2 , 该电池为甲烷燃料电池,写出M电极反应式:。该电池工作一段时间后,溶液的碱性将(填“增强”、“减弱”或“不变”)。
下列关于化学电源的说法不正确的是( )
A . 判断一种电池的优劣或者是否适合某种用途,主要看它的比能量或比功率
B . 碱性锌锰电池中,锌作负极,溶解转化为 ,
, 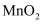 作正极,转化为
作正极,转化为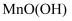 C . 铅酸蓄电池正极板上覆盖有
C . 铅酸蓄电池正极板上覆盖有 , 负极板上覆盖有
, 负极板上覆盖有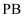 , 电解质溶液为稀硫酸
D . 燃料电池是一种连续地将燃料和氧化剂的化学能直接转化为电能的化学电源
, 电解质溶液为稀硫酸
D . 燃料电池是一种连续地将燃料和氧化剂的化学能直接转化为电能的化学电源
 ,
, 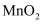 作正极,转化为
作正极,转化为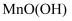 C . 铅酸蓄电池正极板上覆盖有
C . 铅酸蓄电池正极板上覆盖有 , 负极板上覆盖有
, 负极板上覆盖有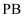 , 电解质溶液为稀硫酸
D . 燃料电池是一种连续地将燃料和氧化剂的化学能直接转化为电能的化学电源
, 电解质溶液为稀硫酸
D . 燃料电池是一种连续地将燃料和氧化剂的化学能直接转化为电能的化学电源
放热反应在生产、生活中用途广泛。
-
(1) 已知25℃、101kPa时,1g甲烷不完全燃烧生成CO和液态水时放出37.96kJ热量,则1mol甲烷不完全燃烧的热化学方程式为。
-
(2) 甲烷可以消除氮氧化物污染,发生的反应为
 , 在体积固定的密闭容器中,每次实验均加入
, 在体积固定的密闭容器中,每次实验均加入 和
和 , 使
, 使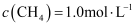 、
、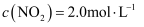 , 在不同条件下进行反应,测得
, 在不同条件下进行反应,测得 随时间的变化情况如下表:
随时间的变化情况如下表:实验
序号
时间/min
浓度
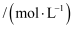
温度/℃
10
20
30
40
50
1
800
0.80
0.67
0.57
0.50
0.50
2
800
0.60
0.50
0.50
0.50
0.50
①实验1中,在10~20min内,
 ,40min时v(正)v(逆)(填:“大于”、“小于”、“等于”)。
,40min时v(正)v(逆)(填:“大于”、“小于”、“等于”)。②0~20min内,实验2比实验1反应速率快的原因可能是。
-
(3) 乙醇应用于燃料电池,该电池采用可传导
 的固体氧化物为电解质,其工作原理如图1所示。b极电极反应式为。
的固体氧化物为电解质,其工作原理如图1所示。b极电极反应式为。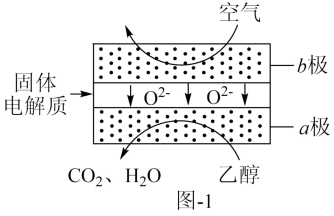
-
(4) 乙醇在Cu作催化剂时与氧气反应的关系如图2,反应②的化学方程式:。
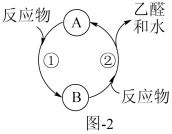
-
(5) 硝酸铵在高温或猛烈撞击时易爆炸,放出大量的热。
 高温分解不可能生成
高温分解不可能生成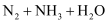 。理由是。
。理由是。
最近更新
- 根据下图,回答15~16题。15.A地区农业地域类型的优越区位条件是( ) A.农业机械化水平高
- 听音能辨认,主要是依据不同人的讲活声具有不同的( )A.音色B.音调C.响度D.振幅
- 李明为好友制作一个(如图)正方体礼品盒,六面上各有一字,连起来就是“预祝中考成功”,其中“预”的对面是“中”,“成”的对
- 静止在水平桌面上的书,受到的平衡力是( ) A.书的重力和书对桌子的压力 B.书对桌子的压力和桌子的重力 C.书的重力
- 从分子的角度分析,下列解释不正确的是 A.水结冰体积变大——分子大小发生改变B.氧气加压后贮存在钢瓶中——分子间有间隔
- 如热气球的探测器显示,从热气球A处看一栋高楼顶部的仰角为45°,看这栋高楼底部的俯角为60°,A处与高楼的水平距离为60
- 亚氯酸钠(NaClO2)是一种漂白剂。用过氧化钠与ClO2作用,可得到纯净的NaClO2: 2C1O2+
- He had to speak in a loud voice in order tomake himself____
- 如图11所示,一个变压器(可视为理想变压器)的原线圈接在220V的市电上,向额定电压为1.80×104V的霓虹灯供电,使
- 古诗文默写。 ⑴予独爱莲之 ,
- 关于函数.有下列三个结论:①的值域为;②是 上的增函数;③的图像是中心对称图形,其中所有正确命题的序号是_______;
- 哥伦布的话在15世纪的西欧非常具有代表性,他说:“黄金是一切商品中最宝贵的,黄金是财富,谁占有黄金,谁就获得他在世上所需
- 右图为实验室用等质量的高锰酸钾和氯酸钾(另加少量的二氧化锰),分别制取氧气的数据分析示意图。 下列依据图示信息所得出的分
- 氮化硅是一种新合成的结构材料,它是一种超硬、耐磨、耐高温的物质。下列各组物质熔化时,所克服的粒子间作用力与氮化硅熔化时所
- 阅读下面的文字,完成下面小题。张桂梅,筹建了全免费的公办女子高中——云南丽江华坪女子高级中学。该
- 汉译英 1. 九年级的学生都在盼望着上高中。(look forward to) 2. 生活总是充满意外。(full) 3
- 在日常生活中应注意合理摄取营养物质和人体必需的元素。 (1)食物的成分主要有蛋白质、糖类、油脂、 、无机
- 下列有关溶液的叙述错误的是()A. 溶液中的溶剂只能是水 B. 固体NaOH溶于水时,溶液温度升高 C. 一定条件下,饱
- 传说中“大禹治水”的水,你认为应该是 A、长江 B、黄河 C、淮河
- 创新是历史发展的动力,实事求是和理论创新是社会主义事业能持续发展的重要保证。阅读下列材料,回答问题:材料一: “……前面



