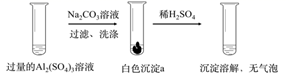
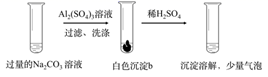
盐类水解的应用 知识点题库
 减少
B . 将NH4Cl溶液从20℃升温至30℃,溶液中
减少
B . 将NH4Cl溶液从20℃升温至30℃,溶液中  增大
C . 向氢氧化钠溶液中加入醋酸至中性,溶液中
增大
C . 向氢氧化钠溶液中加入醋酸至中性,溶液中  =1
D . 向含有BaSO4、BaCO3的饱和溶液中加入少量的Ba(NO3)2 , 溶液中的
=1
D . 向含有BaSO4、BaCO3的饱和溶液中加入少量的Ba(NO3)2 , 溶液中的  减小
减小
相关物质的溶度积常数见下表:
物质 | Cu(OH)2蓝色 | Fe(OH)3红褐 | CuCl白色 | CuI白色 |
Ksp | 2.2×10-20 | 2.6×10-39 | 1.02×10-6 | 1.3×10-12 |
-
(1) 某酸性CuCl2溶液中含有少量的FeCl3 , 为得到纯净的CuCl2·2H2O晶体,加入,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2·2H2O晶体。
-
(2) 在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2 , 原因是(用化学方程式表示)。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是。
-
(3) 某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
可选用作滴定指示剂,滴定终点的现象是。
CuCl2溶液与KI反应的离子方程式为。
-
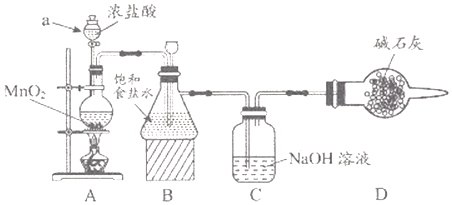
(1) 该学习小组按上图装置进行实验(部分夹持装置省去),反应一段时间后,分别取B、C瓶中的溶液进行实验,实验现象如下表。
已知:①饱和 NaClO溶液pH为11;
②25℃时,弱酸电离常数为:H2CO3:K1=4.4×10-7 , K2=4.7×10-11;HClO:K=3×10-8
实验步骤
实验现象
B瓶
C瓶
实验1:取样,滴加紫色石蕊试液
变红,不褪色
变蓝,不褪色
实验2:测定溶液的pH
3
12
回答下列问题:
①仪器a的名称,装置A中发生反应的离子方程式。
②C瓶溶液中的溶质是NaCl、(填化学式)。
③若将C瓶溶液换成 NaHCO3溶液,按上述操作步骤进行实验,C瓶现象为:实验1中紫色石蕊试液立即褪色;实验2中溶液的pH=7.结合平衡移动原理解释紫色石蕊试液立即褪色的原因
-
(2) 测定C瓶溶液中NaClO含量(单位:g/L)的实验步骤如下:
Ⅰ.取C瓶溶液20mL于锥形瓶中,加入硫酸酸化,加入过量KI溶液,盖紧瓶塞并在暗处充分反应。
Ⅱ.用0.1000mol/LNa2S2O3标准溶液滴定锥形瓶中的溶液,淀粉溶液显示终点后,重复操作2~3次,Na2S2O3溶液的平均用量为24.00mL。(已知:I2+2S2O32-=2I-+S4O62-)
①步骤I的C瓶中发生反应的离子方程式为。
②盖紧瓶塞并在暗处反应的原因滴定至终点的现象。
③C瓶溶液中NaClO含量为g/L(保留2位小数)
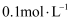 的溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是( )
的溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是( )
 混合溶液(pH=10.30):
混合溶液(pH=10.30): 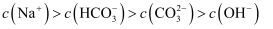 B . 氨水-NH4Cl混合溶液(pH=9.25):
B . 氨水-NH4Cl混合溶液(pH=9.25): 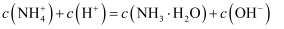 C .
C . 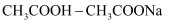 混合溶液(pH=4.76):
混合溶液(pH=4.76): 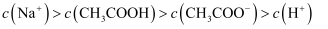 D .
D . 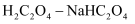 混合溶液(pH=1.68,H2C2O4为二元弱酸):
混合溶液(pH=1.68,H2C2O4为二元弱酸): 
-
(1) 溶液①呈性(填“酸”、“碱”或“中”),其原因是(用离子方程式表示)。
-
(2) 室温下,测得溶液②的pH=7,则CH3COO-与NH4+浓度的大小关系是c(CH3COO-) c(NH4+)(填“>”、“<”或“=”)。
-
(3) 上述溶液中c(NH4+)最小的是(填序号)。
-
(4) 常温下,0.1 mol/ L氨水溶液加水稀释过程中,下列表达式的数值变大的是____________(填字母)。A . c(OH-) B .
 C . c(H+)·c(OH-)
D .
C . c(H+)·c(OH-)
D . 
| 实验1 | |
| 实验2 | |
下列分析正确的是( )
-
(1) 海水会腐蚀铁质海轮外壳,制造海轮时会在船底四周镶嵌。(填“锌块”或“铜块”)
-
(2) 自来水厂常用含有 Fe3+的净水剂净水,其原理是。(用离子方程式表示)
-
(3) 自来水常用氯气杀菌消毒,
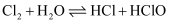 ,要增大 HClO 的浓度,可以加入下列物质中的____。
A . CH3COONa B . HCl C . CaCO3固体 D . H2O E . SO2
,要增大 HClO 的浓度,可以加入下列物质中的____。
A . CH3COONa B . HCl C . CaCO3固体 D . H2O E . SO2 -
(4) 常温下,0.01mol·L-1NaOH溶液,由水电离出的c(OH-)=mol·L-1。
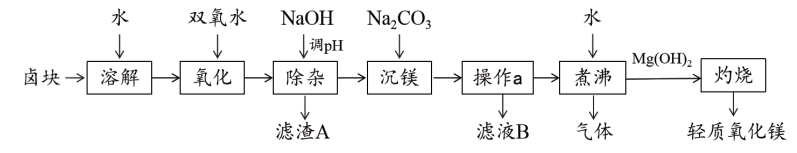
已知:I.氢氧化亚铁呈絮状。
II.右表是25℃时生成氢氧化物沉淀对应的pH。
离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe2+ | 7.6 | 9.6 |
Fe3+ | 2.7 | 3.7 |
Mn2+ | 8.3 | 9.8 |
Mg2+ | 9.6 | 11.1 |
回答下列问题:
-
(1) 溶解时要先将卤块粉碎,其目的是。
-
(2) 加入双氧水的目的是;不能用酸性KMnO4溶液代替双氧水的原因是。
-
(3) “除杂”时,溶液pH至少应调至;滤渣A的主要成分是。
-
(4) “沉镁”的主要反应的离子方程式为;“煮沸”时产生气体的化学方程式为。
-
(5) “操作a”包括过滤、洗涤沉淀等操作。若要检测“洗涤沉淀”是否完成,其方法是(包括操作、现象、结论)。
-
(6) 若该工艺中用285t卤块(含MgCl290%)为原料,制得102.6t轻质氧化镁,则MgO的产率为。
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满溶液;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00 mL待测液注入洁净的未干燥的锥形瓶中,加入2滴指示剂溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答下列问题:
-
(1) 以上操作步骤有不正确的是(填数字序号)。下列操作中,能造成中和滴定的测定结果偏高的有(填字母序号)。
a.配制标准溶液的固体NaOH中混有KOH杂质
b.中和滴定到达终点时俯视滴定管内液面读数
c.振荡时锥形瓶中溶液飞溅出来
d.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
-
(2) 某同学在滴定实验中,碱式滴定管中的液面如图所示。侧消耗的NaOH溶液的体积为mL。

-
(3) 常温下向0.2000 mol/L二元酸H2A溶液中滴加0.2000 mol/L NaOH溶液。溶液中H2A、HA-、A2-的物质的量分数(
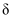 )随溶液pH的变化关系如图所示。
)随溶液pH的变化关系如图所示。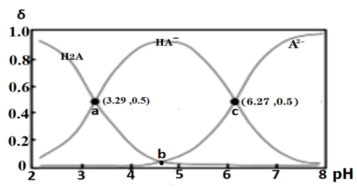
①列说法正确的是(填字母序号)。
A.该滴定过程若选择单一指示剂最好选择甲基橙
B.当V(NaOH)=V(H2A)时,溶液中存在:
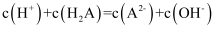
C.pH=6.27时,c(HA-)=c(A2-)>c(H+)>c(OH-)
D.V(NaOH):V(H2A)=3:2时,
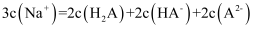
②常温下H2A的电离平衡常数Ka1=。
③当pH=6时
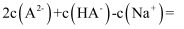 mol/L。
mol/L。④滴加至a、b、c三个交点处,溶液中水的电离程度由大到小依次为(用字母排序)。
 为二元弱酸,在25℃时,溶液中
为二元弱酸,在25℃时,溶液中 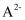 及HA-浓度的负对数pc随溶液pH变化的关系如图所示[已知:溶液中始终保持
及HA-浓度的负对数pc随溶液pH变化的关系如图所示[已知:溶液中始终保持 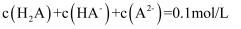 ]。下列有关叙述错误的是( )
]。下列有关叙述错误的是( ) 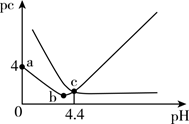
 C . 由a点到c点的过程中,水的电离程度一直增大
D . NaHA溶液呈碱性
C . 由a点到c点的过程中,水的电离程度一直增大
D . NaHA溶液呈碱性
- 在细胞免疫中,效应T细胞发挥免疫作用的机制是( ) A.激活靶细胞内的溶酶体酶 B.与抗原结合使其失去活性 C.
- 中学生小强最近感到很烦恼,他渴望自主地安排生活,可是父母却总是过多地干预他;他想与同学友好交往,但又不愿意主动接近他们。
- 人类是生活离不开水,某生活污水主要含有碎菜叶、碎塑料薄膜、泥沙、氯化钠和碳酸钠等物质.现欲将其经去渣处理后作为清洗厕所的
- 下表是组成地壳和组成细胞的一些元素的含量(%),试根据表格回答下列问题: 种类位置 O Si C N H 地壳 48.6
- 如图所示为冰在加热过程中,温度随时间变化的图像。以下说法中不正确的是 ( )A.冰是一种晶体B.冰的熔点为0℃C
- 一列简谐机械横波某时刻的波形图如图所示,波源的平衡位置坐标为x=0.当波源质点处于其平衡位置上方且向下运动时,介质中平衡
- 下列说 法中正确的一组有 ( ) ①商品和货币是一对孪生兄弟
- 穆罕默德·阿里的土地制度改革产生了重大的历史影响,但不包括( ) A.一定程度上减轻了农民的负担 B.推动了埃及新兴
- 文学名著阅读 《水浒传》 是中国古典文学中最优秀的一部英雄传奇。它成功地塑造了一批个性鲜明、令人经久不忘的人物形象。请你
- 学过单摆的周期公式以后,同学们对各种摆产生了兴趣,他们用厚度和质量分布均匀的方木块(如一把米尺)做成摆(这种摆被称为复摆
- 先化简,再求值:,其中=.
- a、b、c、d四个集气瓶中,分别盛有H2、Cl2、HCl、HBr中的任意一种,将a和b两瓶气体混合后见光发生爆炸,将b
- 若线性方程组 ( ) A、1 .B、-1 . C、1 . D
- I _________ Beijing tomorrow. A.will back B.am back
- 有“世界屋脊”之称的高原是( ) A.巴西高原 B.蒙古高原 C.青藏高
- 下列各句中,加点词语使用正确的一句是 A、互联网大肆“入侵”教育领域已是人所共知的事实,仅从近年来在线教育在创业热点中所
- 选出下列各项中注音有误的一项:( ) A.重创 chuāng 阐明 chǎn 颤动 chàn B.鞭笞 chī 场院
- Spring is here and sois the cycling season. Here are some ti
- 在做凸透镜成像实验时,当蜡烛距凸透镜15 cm,在光屏上成放大的像,则下列说法中不正确的是( )A.蜡烛距透镜40
- Na2FeO4是一种高效多功能水处理剂,应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下: 2FeS