弱电解质在水溶液中的电离平衡 知识点题库
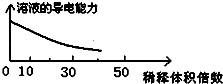 醋酸稀释
C .
醋酸稀释
C . 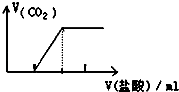 向Na2CO3溶液中逐滴滴入盐酸
D .
向Na2CO3溶液中逐滴滴入盐酸
D . 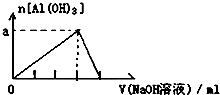 向AlCl3溶液中滴加过量的NaOH溶液
向AlCl3溶液中滴加过量的NaOH溶液
H2CO3 | HBO3(硼酸) |
K1=4.4×10-7 K2=4.7×10-11 | K=5.8×10-10 |
I.下表是几种弱酸常温下的电离平衡常数:
CH3COOH | H2CO3 | H2S | H3PO4 |
1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
-
(1) CH3COOH、H2CO3、H2S、H3PO4四种酸的酸性由强到弱的顺序为。
-
(2) 多元弱酸的二级电离程度远小于一级电离的原因是。
-
(3) 同浓度的CH3COONa、NaHCO3、Na2CO3、Na2S溶液的pH由大到小的顺序为。
-
(4) II.常温下,0.1 mol/LNaHCO3溶液的pH大于7,则溶液中c(H2CO3)c(CO32-) (填“>”、“=”或“<”);常温下,已知0.1 mol/LNaHCO3溶液的pH等于8,则溶液中c(H2CO3)-c(CO32-)=mol/L(写出计算数值结果)。
-
(5) c(NH4+)相等的①(NH4)2SO4 ②(NH4)HSO4③(NH4)2CO3④ NH4Cl四种溶液,其物质的量浓度由大到小的顺序为。
-
(6) 等体积等浓度的Ba(OH)2与NH4Cl的混合溶液中各种离子浓度大小关系为(由大到小排列)。
弱电解质 | HCOOH | HCN | H2CO3 |
电离常数(25 ℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
下列说法错误的是( )
 HCN+ HCOO-的化学平衡常数3.67×105
HCN+ HCOO-的化学平衡常数3.67×105
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向同pH、同体积的醋酸和盐酸溶液中加入足量镁粉,完全反应后收集H2的体积 | 比较两种酸的电离程度 |
| B | 将混有Ca(OH)2杂质的 Mg(OH)2样品放入水中,搅拌,成浆状后,再加入饱和MgCl2溶液,充分搅拌后过滤,用蒸馏水洗净沉淀。 | 除去Mg(OH)2样品中的Ca(OH)2杂质 |
| C | 向盛有1mL0.01mol/LAgNO3溶液的试管中滴加5滴0.01mol/L NaCl溶液,有白色沉淀生成,再滴加0.01mol/L NaI溶液,产生黄色沉淀。 | 常温下,Ksp(AgCl)>Ksp(AgI) |
| D | 室温下,用pH试纸测得:0.1mol/LNa2SO3溶液pH约为10,0.1mol/LNaHSO3溶液pH约为5 | HSO3-结合H+的能力比SO32-的弱 |
|
化学式 |
HA(A代表某种酸根) |
HNO2 |
H2CO3 |
|
Ka |
Ka=4.9´10-10 |
Ka=4.6´10-4 |
Ka1=4.1´10-7 Ka2=5.6´10-11 |
-
(1) 用离子方程式表示NaNO2溶液呈碱性的原因。
-
(2) NaHCO3的电离方程式是。
-
(3) A-、CO
 、HCO
、HCO  在水中结合H+的能力由大到小的顺序为。
在水中结合H+的能力由大到小的顺序为。
-
(4) 写出NaA溶液中通少量CO2的离子方程式。
-
(5) 某同学用Na2CO3和NaHCO3溶液进行如下图所示实验。
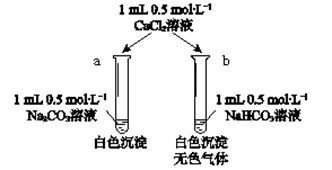
①充分反应后a试管中大量存在的离子是。
②用离子方程式表示b试管中发生的反应。
 的值增大
D . Kw的值减小
的值增大
D . Kw的值减小
| 化学式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
| Ksp或Ka | Ksp=1.8×10-10 | Ksp=2.0×10-12 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
 、NH3·H2O、HCO
、NH3·H2O、HCO  、CO
、CO  的分布如图(忽略溶液体积的变化)。已知常温下Kb(NH3·H2O)=1.8×10−5 , Ka1(H2CO3)=4.2×10−7 , Ka2(H2CO3)=5.6×10−11 , 则下列说法正确的是( )
的分布如图(忽略溶液体积的变化)。已知常温下Kb(NH3·H2O)=1.8×10−5 , Ka1(H2CO3)=4.2×10−7 , Ka2(H2CO3)=5.6×10−11 , 则下列说法正确的是( ) 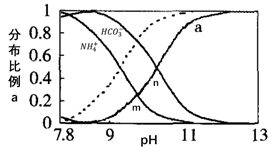
 )
C . n点时,溶液中3c(HCO
)
C . n点时,溶液中3c(HCO  )+c(OH⁻)=c(NH
)+c(OH⁻)=c(NH  )+c(H+)
D . 反应HCO
)+c(H+)
D . 反应HCO  +OH—
+OH—  CO
CO  +H2O的平衡常数K=
+H2O的平衡常数K= 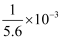
-
(1) 加适量醋酸钠晶体后,醋酸溶液中c(H+)(填“增大”、“减小”或“不变”,下同),盐酸中c(H+)。
-
(2) 加水稀释10倍后,溶液中的c(H+):醋酸 (填“>”、“=”或“<”,下同)盐酸。加等浓度的NaOH溶液至恰好中和,所需NaOH溶液的体积:醋酸盐酸。
-
(3) 使温度都升高20℃,溶液中c(H+):醋酸(填“>”、“=”或“<”)盐酸。
-
(4) 分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是(填字母)。(①表示盐酸,②表示醋酸)
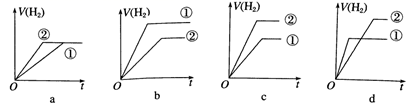
-
(5) 将0.1mol∙L-1的CH3COOH加水稀释,有关稀释后醋酸溶液的说法中,正确的是(填字母)。
a.电离程度增大
b.溶液中离子总数增多
c.溶液导电性增强
d.溶液中醋酸分子增多
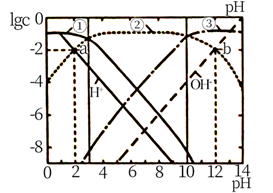
 的平衡常数
的平衡常数 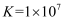 D . 25℃时,0.1mol/L的NaHA溶液中:
D . 25℃时,0.1mol/L的NaHA溶液中: 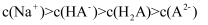
-
(1) 氨水显碱性的原因是(用电离方程式表示)。向氨水中加入 NH4Cl 固体,氨水的电离程度(填“增大”“减小”或“不变”),原因是 ,溶液的 pH(填“增大”“减小”或“不变”)。
-
(2) NH4Cl 溶液显性,原因是(用离子方程式表示)。室温下,若向 NH4Cl溶液中加入少量氨水,使溶液中c(
 )=c(Cl-),则溶液的 pH7(填“>”“<”或“=”)。
)=c(Cl-),则溶液的 pH7(填“>”“<”或“=”)。
-
(3) Mg(OH)2浊液中存在 Mg(OH)2 的沉淀溶解平衡。向此浊液中加入浓的 NH4Cl溶液,观察到的现象是,反应原理是(用离子方程式表示)。
 CH3COO-+H+ , 要使溶液中
CH3COO-+H+ , 要使溶液中  增大,可以采取的措施是( )
增大,可以采取的措施是( ) ①加少量烧碱固体 ②升高温度 ③加少量冰醋酸 ④加水 ⑤加少量醋酸钠固体
-
(1) 现有0.01mol/L的
 和0.01mol/L的
和0.01mol/L的 两种溶液。[已知:电离度
两种溶液。[已知:电离度 ,
, 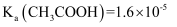 ,
, 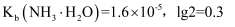 ]
]①
 的电离方程式为。
的电离方程式为。②0.01mol/L的
 的电离度约为%。
的电离度约为%。③0.01mol/L的
 的pH=。
的pH=。④若上述酸和碱等体积充分混合,混合后所得溶液的pH(填“>”、“<”或“=”)7,此时溶液中各离子浓度由大到小的顺序为。
-
(2) 甲酸钠(HCOONa)属于(填“强”或“弱”)电解质,HCOONa溶液呈碱性的原因是(用离子方程式表示)。0.01mol/L的HCOONa溶液中
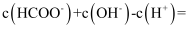 mol/L。
mol/L。
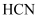 )有剧毒,易挥发。金矿提金时,用
)有剧毒,易挥发。金矿提金时,用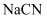 溶液浸取金生成
溶液浸取金生成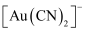 , 再用锌置换出金,产生的含氰废水需处理后排放。
, 再用锌置换出金,产生的含氰废水需处理后排放。
-
(1) ①
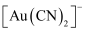 存在着两步电离平衡,其第一步电离方程式为。
存在着两步电离平衡,其第一步电离方程式为。
②
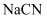 可用于制备
可用于制备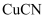 ,
, 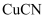 浊液中加入
浊液中加入 溶液可发生反应:
溶液可发生反应: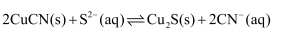 , 该反应的平衡常数
, 该反应的平衡常数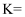 。
。[已知
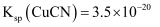 ,
, 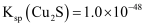 ]。
]。 -
(2)
 可催化
可催化 氧化废水中的
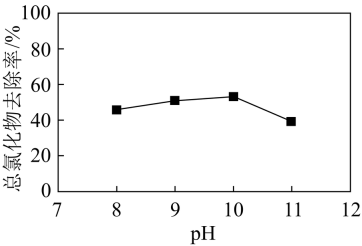
氧化废水中的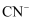 。其他条件相同时,总氯化物(
。其他条件相同时,总氯化物(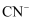 、
、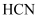 等)去除率随溶液初始
等)去除率随溶液初始 变化如图所示。
变化如图所示。
①在酸性条件下,
 也能氧化
也能氧化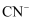 , 但实际处理废水时却不在酸性条件下进行的原因是。
, 但实际处理废水时却不在酸性条件下进行的原因是。②当溶液初始
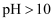 时,总氰化物去除率下降的原因可能是。
时,总氰化物去除率下降的原因可能是。 -
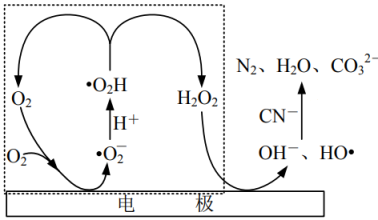
(3) 通过电激发产生
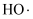 和
和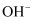 处理废水中的
处理废水中的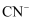 , 可能的反应机理如图所示。虚线方框内的过程可描述为。
, 可能的反应机理如图所示。虚线方框内的过程可描述为。
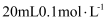 的HAuCl4溶液。溶液中,含氯微粒a、b的分布系数
的HAuCl4溶液。溶液中,含氯微粒a、b的分布系数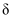 、NaOH溶液体积V(NaOH)与pH的关系如图所示。[比如HAuCl4的分布系数,
、NaOH溶液体积V(NaOH)与pH的关系如图所示。[比如HAuCl4的分布系数,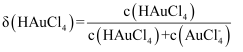 ]。下列叙述错误的是( )
]。下列叙述错误的是( )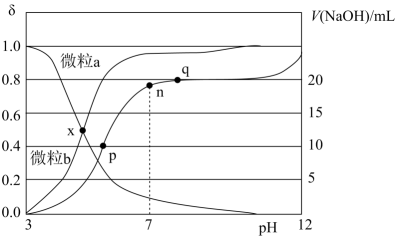
 )
C . 微粒b为AuCl
)
C . 微粒b为AuCl , 该滴定可选酚酞作指示剂
D . 滴定到q点时,溶液中c(HAuCl4)>c(AuCl
, 该滴定可选酚酞作指示剂
D . 滴定到q点时,溶液中c(HAuCl4)>c(AuCl )
)
- 老张有一家食品加工厂,在市场竞争日益激烈的情况下,他要给自己的产品提供降价空间,应采取的措施是
- The building around the corner caught fire last night.The po
- 在1和128之间插入6个数,使它们和这两数成等比数列,则这6个数的和为( )A.126
- 如图20所示,电源电压为6V。闭合开关S,电压表V1示数为4V,电流表A的示数为0.4A.求:(1)电压表V2的示数;(
- 有A、B、C、D、E五种元素.其相关信息如下:元素 相关信息 A A元素的一种原子没有中子,只有一个质子 B B是电负性
- 目前,我国有宗教活动场所8万余处,宗教团体3千多个。宗教界人士依法参与国家政治生活,宗教界与70多个国家和地区的宗教组织
- 不粘锅的内壁有一薄层为聚四氟乙烯的涂层,用不粘锅烹烧饭菜时不易粘锅、烧焦。下列关于聚四氟乙烯的说法正确的是( )
- 做简谐振动的物体,当振子的位移为负值时,下列说法中可能正确的是( ) A.速度一定为正值,加速度一定为负值 B
- ________, the bookseller gave him something else as a presen
- 第三部分:阅读理解(共20小题.每小题3分,满分60分) 阅读下列短文,从每题所给的四个选项( A, B,C,和D
- 对右图人物的统治给予充分肯定,主要是因为 ( ) A.她是我国历史上唯一的女皇帝 B.她帮助有病的唐高宗处理
- 面对美国加大重返亚太的“攻势”、日本在钓鱼岛以及菲律宾在南海的“无理”,我国要 ①坚定地维护我国的国家利益 ②
- 已知曲线y=-1上两点A(2,-)、B(2+Δx,-+Δy),当Δx=1时,割线AB的斜率为__________.
- 爱因斯坦认为:“想象力比知识更重要,因为知识是有限的,想象力概括着世界上的一切,推动着进步,并且是知识进化的源泉。”下列
- 下面加点的成语,使用恰当的一项是( ) A.他的毕业设计终于完成了,但是大家对此评价并不高,认为实在是差强人意,有
- 河流阶地是常见的河流地貌之一,是由河流作用形成的沿河分布的阶梯状地形。河流阶地主要由阶地面和阶地斜坡(坡坎)两个形态要
- 及时复习已学过的知识,对神经系统的活动来说这是( ) A.使神经中枢交替活动和休息
- 已知以下反应的热化学方程式: ①CH3COOH(l)+2O2(g)2CO2(g)+2H2O(l) ΔH(298 K)=
- (本题满分10分) 已知:(R,a为常数). (I)若,求f(x)的最小正周期及单调减区间; (II)若,时,f(x
- 已知方框内是食品香精菠萝酯的生产路线,A、B又能发生方框外所示的转化关系。A、B、C的分子式分别C2H3ClO2、C8H



