弱电解质在水溶液中的电离平衡 知识点题库
 B .
B .  C .
C .  D .
D . 
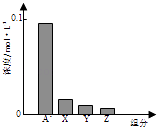
 比值增大,可以采用的措施是( )
比值增大,可以采用的措施是( )
酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
CH3COOH | 1.8×10-5 | HClO | 3×10-8 |
H2O2 | K1=2.4×10-12 K2=1×10-25 | H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
I.结合上表回答下列问题(均为常温下的数据):
-
(1) 在常温下,相同物质的量浓度的①CH3COONa②Na2CO3③NaClO三种溶液的pH由小到大的顺序为(用序号回答)
-
(2) 向Na2CO3溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的钠盐,同时还有另两种钠盐生成,该反应的化学方程式为
-
(3) II.过氧化氢(H2 O2)为淡蓝色粘稠液体,是中学常见试剂.
①H2O2含有的共价键类型为
②实验室可用稀硫酸与BaO2反应来制取H2 O2 , 该反应的化学方程式为
③经测定H2O2为二元弱酸,酸性比碳酸还弱,不稳定易分解.已知Na2O2中通入干燥的CO2不反应,但通入潮湿的CO2却可以产生O2 , 试用化学方程式表示这一过程
①NaHCO3 ②NaHSO4 ③Na2SO4 ④Na2CO3
-
(1) 水存在如下平衡:H2O+H2O
 H3O++OH-,向水中加入NaHSO4固体,水的电离平衡向(填 “左”或“右”)移动, 且所得溶液显
性。
H3O++OH-,向水中加入NaHSO4固体,水的电离平衡向(填 “左”或“右”)移动, 且所得溶液显
性。
-
(2) 向水中加NaHCO3固体,水的电离平衡向(填“左”或“右”)移动,且所得溶液显 性。
-
(3) 常温下,0.1 mol·L-1 CH3COONa溶液的pH为9,则由水电离出的c(H+)=。
-
(4) 若取pH、体积均相等的NaOH溶液和氨水分别加水稀释m倍、n倍后pH仍相等,则mn ( 填“>”“<”或“=”)。

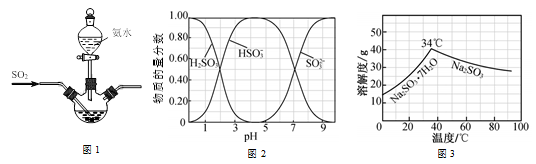
已知:①反应Ⅰ在三颈烧瓶中发生,装置如图所示(固定及加热类仪器省略);
②H2SO3、HSO3-、SO32-在水溶液中的物质的量分数随pH的分布如图;
③Na2SO3·7H2O 和Na2SO3的溶解度曲线如图。
-
(1) 为提高Na2SO3产率,反应Ⅰ应控制pH在左右。
-
(2) 反应Ⅱ所得滤液的主要成分是和Na2SO3。
-
(3) 将操作Ⅰ后所得的Na2SO3溶液(填操作),过滤出的固体用无水乙醇洗涤、在真空干燥箱中采用150℃干燥,得无水Na2SO3固体。
-
(4) 可以用KIO3测定产品中无水Na2SO3的纯度:称取0.1260 g样品于锥形瓶中,用蒸馏水溶解,并加入淀粉做指示剂,滴加酸性KIO3溶液(a mol·L-1)至Na2SO3恰好完全氧化成Na2SO4 , 发生反应3Na2SO3 + KIO3 = 3Na2SO4 + KI,消耗KIO3溶液体积为b mL。通过计算确定样品中Na2SO3的质量分数(写出计算过程)
-
(5) 滴加酸性KIO3溶液时,剧烈震荡锥形瓶或者滴加时间过长都会造成所测Na2SO3纯度偏低,原因是。
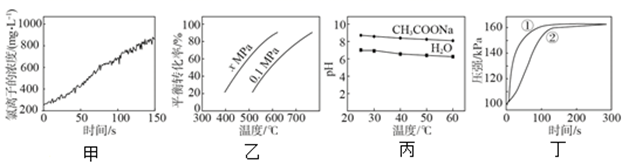
 C4H8(g) + H2(g)的平衡转化率与温度和压强的关系曲线,推断该反应的∆H>0、x>0.1
C . 丁是 0.03g 镁条分别与 2 mL 2 mol/L 盐酸和醋酸反应过程中密闭容器内气体压强随时间的变化曲线,推断①代表盐酸与镁条的反应
D . 丙是 0.5 mol/L CH3COONa 溶液及水的 pH 随温度的变化曲线,说明随温度升高,CH3COONa 溶液中 c(OH-)减小
C4H8(g) + H2(g)的平衡转化率与温度和压强的关系曲线,推断该反应的∆H>0、x>0.1
C . 丁是 0.03g 镁条分别与 2 mL 2 mol/L 盐酸和醋酸反应过程中密闭容器内气体压强随时间的变化曲线,推断①代表盐酸与镁条的反应
D . 丙是 0.5 mol/L CH3COONa 溶液及水的 pH 随温度的变化曲线,说明随温度升高,CH3COONa 溶液中 c(OH-)减小
 ]随pH变化的关系如图所示,下列表述正确的是( )
]随pH变化的关系如图所示,下列表述正确的是( ) 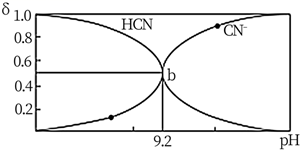
|
① |
② |
③ |
④ |
|
0.01mol/L的甲胺溶液 |
pH=12的甲胺溶液 |
0.01mol/L的氢溴酸 |
pH=2的氢溴酸 |
回答下列问题:
-
(1) ①稀释到原来体积的10倍后,溶液的pH(填“>”“=”或“<”,下同)11,①和③两溶液中由水电离出的c(H+):①③。
-
(2) ②③等体积混合后所得溶液的pH7。
-
(3) ①与③混合时发生反应的离子方程式为。
-
(4) ②与④混合,若所得溶液呈酸性,则溶液体积:②(填“>”“=”或“<”)④。
-
(1) 已知部分弱酸的电离常数如下表:
弱酸
HF
CH3COOH
H2CO3
H2S
电离平衡常数(25℃)
Ka=7.2×10-4
Ka=1.75×10-5
Ka1=4.30×10-7
Ka2=5.61×10-11
Ka1=9.1×10-8
Ka2=1.1×10-12
①写出H2S的Ka1的表达式:。
②常温下,浓度相同的三种溶液NaF、Na2CO3、CH3COONa,pH由大到小的顺序是。
③将过量H2S通入Na2CO3溶液,反应的离子方程式是。
-
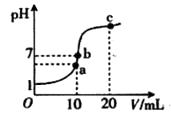
(2) 室温下,用0.100 mol·L-1盐酸溶液滴定20.00 mL 0.100 mol·L-1的氨水溶液,滴定曲线如图所示。
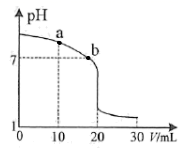
(忽略溶液体积的变化,①②填“>”“<”或“=”)
①a点所示的溶液中c (NH3·H2O)c (Cl-)。
②b点所示的溶液中c (Cl-)c (NH
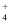 )。
)。③室温下pH=11的氨水与pH=5的NH4Cl溶液中,由水电离出的c (H+)之比为。
-
(3) 雌黄(As2S3)可转化为用于治疗白血病的亚砷酸(H3AsO3)可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分数与溶液的pH 关系如下图所示:
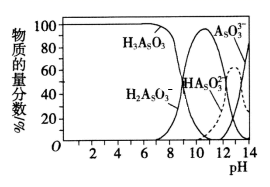
①人体血液的pH在7.35 -7.45之间,用药后人体中含砷元素的主要微粒是 。
②将KOH 溶液滴入亚砷酸溶液,当pH 调至11 时发生反应的离子方程式是。
③下列说法正确的是(填字母序号)
a.n(H3AsO3)∶n(H2AsO
 )=1∶1时,溶液显碱性
)=1∶1时,溶液显碱性b.pH=12时,溶液中c(H2AsO
 )+2c(HAsO
)+2c(HAsO  )+3c(AsO
)+3c(AsO 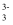 )+c(OH-)=c(H+)
)+c(OH-)=c(H+)c.在K3AsO3溶液中,c(AsO
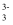 )>c(HAsO
)>c(HAsO  )>c(H2AsO
)>c(H2AsO  )
)
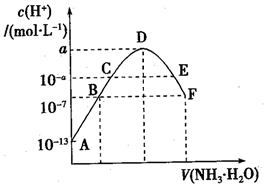
 )=2c(B2-)
)=2c(B2-)
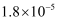 ,H2S的
,H2S的  、
、  依次为
依次为 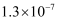 、
、 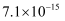 。下列说法正确的是( )
。下列说法正确的是( )
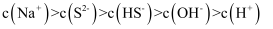 B . 室温时,
B . 室温时, 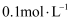 的(NH4)2S溶液中
的(NH4)2S溶液中  比相同浓度的Na2S溶液中
比相同浓度的Na2S溶液中  大
C . 室温时,反应
大
C . 室温时,反应  的平衡常数K=234
D .
的平衡常数K=234
D . 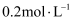 的氨水与
的氨水与 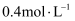 的NaHS等体积混合(体积变化可忽略):
的NaHS等体积混合(体积变化可忽略): 
 )
D . 相同温度下,pH相等的盐酸、醋酸溶液中,c(Cl-)=c(CH3COO-)
)
D . 相同温度下,pH相等的盐酸、醋酸溶液中,c(Cl-)=c(CH3COO-)
- 漫画《挑好“小官”干好“大事”》中,“小官”的选举( )①采取的是差额选举和间接选举的方式 ②是人民群众直接行使民主
- 某物理兴趣小组在探究平抛运动规律时用频闪相机记录了一个小球在做平抛运动过程中的连续的四个位置,已知背景方格纸的边长为a,
- 经济全球化是当今世界经济发展的总趋,它表现的区域特征是( ) A.整体性 B.开放性 C.差异性 D.阶段性
- Only when it rains in summer_______ such beautiful rainbows
- 函数y=+的定义域为__________
- 【小题1】The sign on the left tells us that _______ . A. this is
- 白头搔更短,
- 在此次高三模拟考试前,你们班就试题该易还是该难进行了一次调查。请结合下表内容,用英语写一篇短文,介绍有关调查情况并发表你
- 水蜜桃味甜,毛桃味酸,现将水蜜桃(接穗)接到毛桃(砧木)上,成活后,结出的成熟果实,其味是A.酸味的 B.甜味的
- ______deep down in the earth, the dead forests rotted away
- 已知命题:抛物线的准线方程为;命题:若函数为偶函数,则关于对称.则下列命题是真命题的是 A.
- 根据拼音写汉字或给加点字注音(4分) ①喧xiāo( ) ②sì无忌惮( ) ③如火如tú(
- I like to play _____ my cat . A.on B.at C.
- 关于花生的谚语:“麻屋子,红帐子,里面住着白胖子”中所说“麻屋子”“红帐子”“白胖子”分别是由何结构发育成的(
- 根据“三氟化硼→正三角形→非极性分子”的因果关系,则“三氯甲烷→( ① )→( ② )”的因果关系是 A、正
- 在紧张的高三备考阶段,你们英语老师陈老师为了提高复习效率,广泛征求学生意见。假如你叫王飞,请根据以下提示,给陈老师写封信
- . John ______ buy a sports car for a long time but he doesn’
- 如图,已知在Rt△ABC中,AB=AC=2,在△ABC内作第一个内接正方形DEFG;然后取GF的中点P,连接PD、PE,
- 常温下,某气体能溶于水,密度比空气大,收集该气体可采用的方法是() A.向上排空气法 B.排水法 C.排水法或向下排空气
- 下列几项表述不正确的是() A. 甲骨文已经相当成熟 B.金文比甲骨文规范 C.竹帛书出现于春秋



