盖斯定律及其应用 知识点题库
-
(1) 已知:C(s)+O2(g)=CO2(g)△H1=﹣393.5kJ•mol﹣1
C(s)+H2O(g)=CO(g)+H2(g)△H2=+131.3kJ•mol﹣1
则反应CO(g)+H2(g)+O2(g)=H2O(g)+CO2(g)△H=kJ•mol﹣1 .
-
(2) 利用反应CO(g)+H2(g)+O2(g)=CO2(g)+H2O(g)设计而成的MCFS燃料电池是用水煤气(CO和H2物质的量之比为1:1)作负极燃气,空气与CO2的混合气为正极助燃气,用一定比例的Li2CO3和Na2CO3低熔点混合物做电解质的一种新型电池.现以该燃料电池为电源,以石墨作电极电解饱和NaCl溶液,反应装置以及现象如图所示.则有:
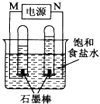
①燃料电池即电源的N极的电极反应式为;
②已知饱和食盐水的体积为1L,一段时间后,测得左侧试管中气体体积为11.2mL(标准状况),若电解前后溶液的体积变化忽略不计,而且电解后将溶液混合均匀,则此时溶液的pH为.
CO2(g)+C(s)=2CO(g) ΔH2
2CO(g)+O2(g)=2CO2(g) ΔH3
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH4
3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s) ΔH5
下列关于上述反应焓变的判断正确的是( )
Ⅰ.CH3CH2CH2CH3 (g)  CH3CH=CH2(g)+CH4(g) △H1=+ 61.31 kJ·mol-1
CH3CH=CH2(g)+CH4(g) △H1=+ 61.31 kJ·mol-1
Ⅱ.CH3CH2CH2CH3(g)  CH2=CH2(g)+CH3CH3(g) △H2=-56.00 kJ·mol-1
CH2=CH2(g)+CH3CH3(g) △H2=-56.00 kJ·mol-1
-
(1) 维持体系温度T不变,总压p恒定时,体积为V1 L的正丁烷发生裂解反应,一段时间平衡后气体体积变为V2 L,此时正丁烷的转化率a(正丁烷)=;维持体系温度不变,向体系中充入一定量的水蒸气(水蒸气在该条件下不参与反应),再次平衡后正丁烷的转化率将(填“增大”、“不变”或“减小”),原因为。
-
(2) 一定温度下向体积为2L的密闭容器中充入0.2molCH3CH=CH2和0.5 molCH4发生反应CH3CH=CH2(g) +CH4(g)
 CH2=CH2(g)+CH3CH3(g) △H3;5 min后达到平衡状态,容器内剩余CH3CH =CH2的物质的量为0.1mol。
CH2=CH2(g)+CH3CH3(g) △H3;5 min后达到平衡状态,容器内剩余CH3CH =CH2的物质的量为0.1mol。①△H3=。
②5min内该反应的反应速率v(CH4)=。
③保持温度不变,向某密闭容器中充入等物质的量的CH3CH =CH2和CH4 , 平衡后容器内CH4的体积分数为。
-
(3) 将0.1molCH2=CH2完全燃烧后的气体通入100mL一定浓度的NaOH溶液中,并将所得溶液稀释至1L。最终所得溶液中CO32-、HCO3-、H2CO3 三者所占物质的量分数随原NaOH溶液浓度变化的关系如图所示:
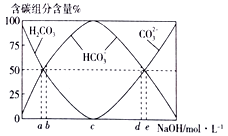
其中图中表示原氢氧化钠溶液浓度为3mol·L-1的是(选填“a”、“b”、“c”、“d”或“e” ),
-
(4) 以氢氧化钠溶液为电解质溶液,CH2=CH2 燃料电池的负极反应式为。
-
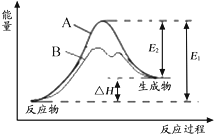
(1) 反应物和生成物均为气态的某可逆反应,在不同条件下的反应历程分别为A、B,如图所示。
①正反应的活化能为(用图中字母表示);
②当反应达平衡后,其他条件不变,升高温度,反应物的转化率将(填“增大”、“减小”、“不变”);
③B历程表明此反应采用的条件为(填标号)。
A.升高温度
B.降低温度
C.增大反应物浓度
D.使用催化剂
-
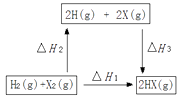
(2) 在如图的转化关系中(X代表卤素)。△H20(填“>”、“=”或“<”);△H1、△H2和△H3三者存在的关系为。
-
(3) 甲醇(
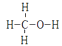 )是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
)是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:①CO(g)+2H2(g)
 CH3OH(g) △H1
CH3OH(g) △H1②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2③CO2(g)+H2(g)
 CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3已知反应①中的相关的化学键键能数据如下:
化学键
H-H
C-O
C
 O
OH-O
C-H
E/(kJ·mol-1)
436
343
1076
465
413
①计算△H1=kJ.mol-1;
②已知△H3=+41.1 kJ.mol-1 , 则△H2 =kJ.mol-1。
-
(1) 页岩气不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应 CH4(g)+H2O(g)=CO(g)+3H2(g)△H1
已知:①CH4、H2、CO 的燃烧热(△H)分别为-a kJ•mol-1、-b kJ•mol-1、-c kJ•mol-1;
②H2O (l) =H2O(g); △H=+dkJ•mol-1
则△H1= (用含字母a、
B、
C、d的代数式表示)kJ•mol-1。
-
(2) 用合成气生成甲醇的反应为:CO(g)+2H2(g)
 CH3OH(g) △H2 , 在10L恒容密闭容器中按物质的量之比1∶2充入CO和H2 , 测得CO的平衡转化率与温度和压强的关系如下图所示,200℃时n(H2)随时间的变化如下表所示:
CH3OH(g) △H2 , 在10L恒容密闭容器中按物质的量之比1∶2充入CO和H2 , 测得CO的平衡转化率与温度和压强的关系如下图所示,200℃时n(H2)随时间的变化如下表所示: 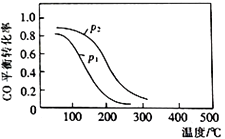
t/min
0
1
3
5
n(H2)/mol
8.0
5.4
4.0
4.0
①△H2 (填“>”“<”或“ = ”)0。
②下列说法正确的是 (填标号)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
③ 0〜3 min内用CH3OH表示的反应速率v(CH3OH)=mol • L-1·min-1。
④ 200℃时,该反应的平衡常数K =。向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则化学平衡(填“正向”、“逆向”或“不”)移动。
-
(3) 甲烷、氧气和KOH溶液可组成燃料电池。标准状况下通入5.6 L甲烷,测得电路中转移1.2 mol电子,则甲烷的利用率为。
 2NO(g),是导致汽车尾气中含有NO的原因之一。
2NO(g),是导致汽车尾气中含有NO的原因之一。
-
(1) 已知H2或CO可以催化还原NO以达到消除污染的目的。N2(g) + O2(g) = 2NO(g) △H= +180.5 kJ·mol-1 , 2H2(g) + O2(g) = 2H2O(l) △H=-571.6 kJ·mol-1 , 则H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是,判断该反应自发进行的条件:(填“高温自发”或“低温自发”)。
-
(2) 当质量一定时,增大固体催化剂的表面积可提高化学反应速率。下图表示在其他条件不变时,反应:2NO(g) + 2CO(g)
 2CO2(g) + N2(g)中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
2CO2(g) + N2(g)中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。 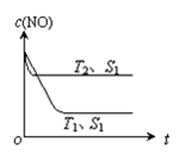
①则该反应的△H0(填“>”或“<”)。
②若催化剂的表面积S1>S2 ,在该图中画出c(NO)在T1、S2条件下达到平衡过程中的变化曲线。
-
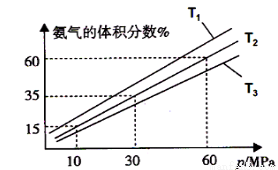
(3) 某小组往一恒温恒压容器充入9mol N2和23mol H2模拟合成氨反应,图C为不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系图.若体系在T2、60MPa下达到平衡.
①能判断N2(g)+3H2(g)⇌2NH3(g)达到平衡的是(填序号).
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(N2)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
②此时N2的平衡分压为MPa.(分压=总压×物质的量分数)。计算出此时的平衡常数Kp=(用平衡分压代替平衡浓度计算,结果保留2位有效数字)。
-
(1) SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式。
-
(2) SiHCl3在催化剂作用下发生反应:
2SiHCl3(g)=SiH2Cl2(g)+SiCl4(g) ΔH1=+48kJ·mol-1
3SiH2Cl2(g)=SiH4(g)+2SiHCl3(g) ΔH2=-30kJ·mol-1
则反应4SiHCl3(g)=SiH4(g)+3SiCl4(g)的ΔH为kJ·mol-1。
-
(3) 对于反应2SiHCl3(g)
 SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。 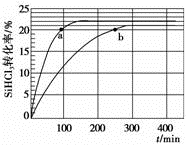
①343K时,反应的平衡转化率α=%。平衡常数K343 K=(保留2位小数)。
②在343K下:要提高SiHCl3转化率,可采取的措施是;要缩短反应达到平衡的时间,可采取的措施有。
-
(4) 甲醇水蒸气重整制氢(SRM)系统简单,产物中H2 含量高、CO含量低(CO会损坏燃料电池的交换膜),是电动汽车氢氧燃料电池理想的氢源。反应如下:
反应I(主):CH3OH(g)+H2O(g)
 CO2(g)+3H2(g) ΔH1=+49kJ/mol
CO2(g)+3H2(g) ΔH1=+49kJ/mol反应II(副):H2(g)+CO2(g)
 CO(g)+H2O(g) ΔH2=+41kJ/mol
CO(g)+H2O(g) ΔH2=+41kJ/mol温度高于300℃则会同时发生反应III:CH3OH(g)
 CO(g)+2H2(g) ΔH3
CO(g)+2H2(g) ΔH3反应1能够自发进行的原因是,升温有利于提高CH3OH转化率,但也存在一个明显的缺点是。写出一条能提高CH3OH转化率而降低CO生成率的措施。
-
(1) 已知下列热化学方程式:
①H2O(l)=H2(g)+
 O2(g) ΔH=+285.8 kJ/mol
O2(g) ΔH=+285.8 kJ/mol②H2(g)+
 O2(g)=H2O(g) ΔH=-241.8 kJ/mol
O2(g)=H2O(g) ΔH=-241.8 kJ/mol③NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3 kJ/mol
④C(s)+
 O2(g)=CO(g) ΔH=-110.5 kJ/mol
O2(g)=CO(g) ΔH=-110.5 kJ/mol⑤C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol
回答下列问题:如果反应物所具有的总能量大于生成物所具有的总能量,反应物转化为生成物时(填“吸收”或“放出”)热量,△H0(填“>”或“<”),上述反应中属于吸热反应的是,C(s)的燃烧热为。
-
(2)
总书记提出:绿水青山就是金山银山。我们在发展经济的同时要坚持节约资源和保护环境。
①用NH3催化还原NOx还可以消除氮氧化物的污染。已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-a kJ·mol-1 ①
N2(g)+O2(g)=2NO(g) ΔH2=-b kJ·mol-1 ②
若1molNH3还原NO至N2 , 则该反应过程中的反应热ΔH3=kJ·mol-1(用含a、b的式子表示)。
②捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)
 (NH4)2CO3(aq) ΔH1
(NH4)2CO3(aq) ΔH1反应Ⅱ:NH3(l)+H2O(l)+CO2(g)
 NH4HCO3(aq) ΔH2
NH4HCO3(aq) ΔH2反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)
 2NH4HCO3(aq) ΔH3
2NH4HCO3(aq) ΔH3请回答下列问题: ΔH3与ΔH1、ΔH2之间的关系是ΔH3=。
①2Li(s)+ H2(g)=2LiH(s) △H=-182 kJ/mol
②2H2(g)+O(g)=2H2O1) △H=- 572 kJ/mol
③4Li(s)+O2(g) = 2Li2O(s) △H=-1196 kJ/mol
则反应2LiH(s)+O2(g)=Li2O(s)+H2O(l)的焓变为( )
已知:CO(g)的燃烧热为283.0
kJ·mol-1;N2(g)+O2(g)  2NO(g) △H1=+180.0 kJ·mol-1。
2NO(g) △H1=+180.0 kJ·mol-1。
请回答下列问题:
-
(1) 反应2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H=。
N2(g)+2CO2(g) △H=。
-
(2) 用活性炭还原法可处理氮氧化物。向2 L恒容恒温密闭容器中加入足量的活性炭和2.0 mol NO,发生反应C(s)+2NO(g)
 N2(g)+CO2(g) △H<0。300℃时,测得反应进行到不同时间各物质的物质的量浓度如图所示。
N2(g)+CO2(g) △H<0。300℃时,测得反应进行到不同时间各物质的物质的量浓度如图所示。 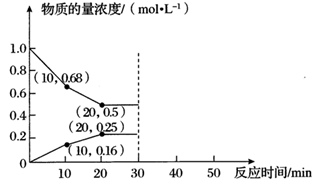
①300℃时,10min内,该反应的平均速率v(N2)=,平衡常数K=。
②保持反应条件与前30min的条件相同,若第30min时向该容器中再加入1 mol NO,则到达新平衡时,c(NO)=。
③若保持其他条件不变,将起始容器改为绝热密闭容器,则到达平衡所需的时间将(填“>”“<”或“=”)20 min。
-
(3) 以石墨为电极,稀NH4NO3为电解质溶液,电解废气中的NO生成NH4NO3的工作原理如图所示:
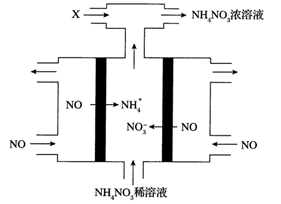
物质X的化学式为,电解时阴极的电极反应式为。
 )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
-
(1) 已知:
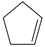 (g) =
(g) = 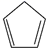 (g)+H2(g) ΔH1=100.3 kJ·mol −1①H2(g)+ I2(g) =2HI(g) ΔH2=−11.0 kJ·mol −1②,对于反应:
(g)+H2(g) ΔH1=100.3 kJ·mol −1①H2(g)+ I2(g) =2HI(g) ΔH2=−11.0 kJ·mol −1②,对于反应: 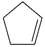 (g)+ I2(g) =
(g)+ I2(g) =  (g)+2HI(g) ③ ΔH3=kJ·mol −1。
(g)+2HI(g) ③ ΔH3=kJ·mol −1。
-
(2) 某温度下,等物质的量的碘和环戊烯(
 )在刚性容器内发生反应③,起始总压为105Pa,平衡时总压增加了20%,环戊烯的转化率为,该反应的平衡常数Kp=Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有(填标号)。
)在刚性容器内发生反应③,起始总压为105Pa,平衡时总压增加了20%,环戊烯的转化率为,该反应的平衡常数Kp=Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有(填标号)。 A.通入惰性气体 B.提高温度 C.增加环戊烯浓度 D.增加碘浓度
-
(3) 环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是__________(填标号)。
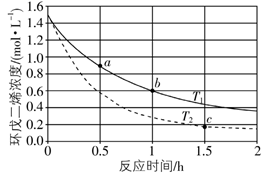 A . T1>T2 B . a点的反应速率小于c点的反应速率 C . a点的正反应速率大于b点的逆反应速率 D . b点时二聚体的浓度为0.45 mol·L−1
A . T1>T2 B . a点的反应速率小于c点的反应速率 C . a点的正反应速率大于b点的逆反应速率 D . b点时二聚体的浓度为0.45 mol·L−1
 重整技术是实现“碳中和”的一种理想的
重整技术是实现“碳中和”的一种理想的 利用技术,具有广阔的市场前景、经济效应和社会意义。该过程中涉及的反应如下。
利用技术,具有广阔的市场前景、经济效应和社会意义。该过程中涉及的反应如下。主反应: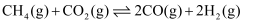
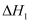
副反应: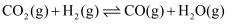
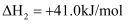
回答下列问题:
-
(1) 已知
 、
、 和
和 的燃烧热
的燃烧热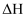 分别为
分别为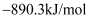 、
、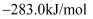 和
和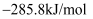 , 该催化重整主反应的
, 该催化重整主反应的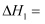
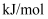 。有利于提高
。有利于提高 平衡转化率的条件是(填标号)。
平衡转化率的条件是(填标号)。A. 高温高压 B. 高温低压 C. 低温高压 D. 低温低压
-
(2) 在刚性密闭容器中,进料比
 分别等于1.0、1.5、2.0,且反应达到平衡状态。
分别等于1.0、1.5、2.0,且反应达到平衡状态。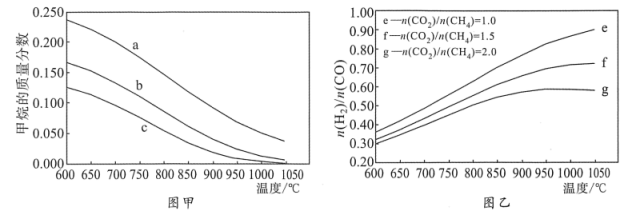
①甲烷的质量分数随温度变化的关系如图甲所示,曲线
 对应的
对应的 ;
;②反应体系中,
 随温度变化的关系如图乙所示,随着进料比
随温度变化的关系如图乙所示,随着进料比 的增加,
的增加, 的值(填“增大”、“不变”或“减小”),其原因是。
的值(填“增大”、“不变”或“减小”),其原因是。 -
(3) 在
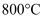 、
、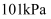 时,按投料比
时,按投料比 加入刚性密闭容器中,达平衡时甲烷的转化率为
加入刚性密闭容器中,达平衡时甲烷的转化率为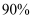 , 二氧化碳的转化率为
, 二氧化碳的转化率为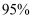 , 则副反应的压强平衡常数
, 则副反应的压强平衡常数 (计算结果保留3位有效数字)。
(计算结果保留3位有效数字)。
-
(4) 我国科学家设计了一种电解装置如图丙所示,能将二氧化碳转化成合成气
 和
和 , 同时获得甘油醛。则催化电极
, 同时获得甘油醛。则催化电极 为极,催化电极
为极,催化电极 产生
产生 的电极反应式为。
的电极反应式为。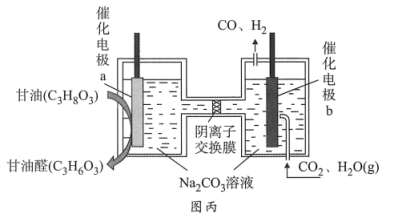
-
(1) 已知①NO2(g)+CO(g)⇌CO2(g)+NO(g)△H1=-234kJ·mol-1
②N2(g)+O2(g)⇌2NO(g)△H2=+179.5kJ·mol-1
③2NO(g)+O2(g)⇌2NO2(g)△H3=-112.3kJ·mol-1
NO2与CO反应生成无污染气体的热化学方程式为。
-
(2) 氨气可将氮氧化物转化为无毒气体。450℃时,在2L恒容密闭容器中充入1molNO、1molNO2和2molNH3 , 起始时体系压强为pMPa,发生反应:NO(g)+NO2(g)+2NH3(g)⇌2N2(g)+3H2O(g),5min时反应达到平衡,此时测得N2的物质的量分数为
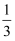 。
。①0~5min内,v(NH3)=mol·L-1·min-1 , NO的平衡转化率=%。
②450℃时,该反应的压强平衡常数Kp=(填含p的代数式,Kp为以分压表示的平衡常数,分压=总压×气体组分物质的量分数)MPa。
-
(3) 工业上,常温下将含NOx的尾气与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中进行无害化处理,原理如图所示。
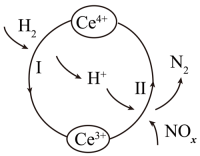
该吸收过程中,Ce3+/Ce4+的作用是,其中反应II的离子方程式为。
-
(1) H2S可以分解制取硫黄和氢气。已知下列热化学方程式:
SO2(g)+I2(s)+2H2O(l)=2HI(aq)+H2SO4(aq) ΔH=-151 kJ·mol-1
2HI(aq)=H2(g)+I2(s) ΔH=+110 kJ·mol-1
H2S(g)+H2SO4(aq)=S(s)+SO2(g)+2H2O(l) ΔH=+61 kJ·mol-1
则H2S分解的热化学H2S(g)=H2(g)+S(s)ΔH=kJ·mol-1。
-
(2) H2S与CO2在高温下发生反应:H2S(g)+CO2(g)
 COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的密闭容器中,保持体积不变,反应平衡后H2O(g)的物质的量分数为0.02。在620 K重复实验,平衡后H2O(g)的物质的量分数为0.03。
COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的密闭容器中,保持体积不变,反应平衡后H2O(g)的物质的量分数为0.02。在620 K重复实验,平衡后H2O(g)的物质的量分数为0.03。 ①下列情况能说明该反应已到达平衡的是(填字母)。
A.容器的压强保持不变
B.容器内气体密度保持不变
C.v正(H2S)=v逆(COS)
D.H2S和CO2的物质的量之比保持不变
②平衡时只改变下列条件,既可以提高反应速率又可以提高H2S(g)转化率的是(填字母)。
A.升高容器的温度
B.保持容器体积一定,充入He,使体系总压强增大
C.缩小容器的体积,使体系总压强增大
D.分离出部分COS(g)
-
(3) 已知Ka1(H2S)=1.3×10-7 , Ka2(H2S)=7×10-15。pH=11时,含H2S、HS-和S2-的溶液中,
 =。
=。
-
(4) 一种CO2、H2S的协同转化装置可实现对天然气中CO2和H2S的高效去除。工作原理如图所示,其中电极分别为石墨烯包裹的ZnO和石墨烯,石墨烯电极发生的反应为:EDTA—Fe2+-e-=EDTA—Fe3+。
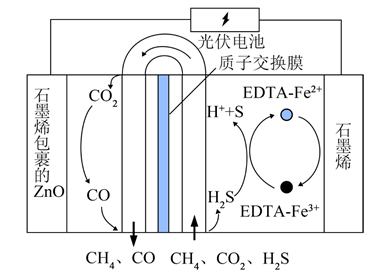
①H2S所发生反应的离子方程式为。
②阴极的电极反应式为。
-
(5) 在恒容密闭容器中,用H2还原SO2生成S的反应分两步完成(如图所示),该过程中部分物质的物质的量浓度随时间的变化关系如图所示:
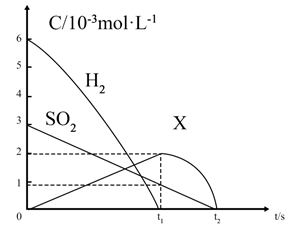
依据如图描述H2还原SO2生成S的过程:。
-
(1) 火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂。
已知:N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=−534 kJ∙mol−1
H2O2(l)=H2O(l)+
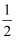 O2(g) ΔH=−98 kJ∙mol−1
O2(g) ΔH=−98 kJ∙mol−1H2O(l)=H2O(g) ΔH=44 kJ∙mol−1
试写出N2H4和液态H2O2反应生成气态水的热化学方程式:。
-
(2) 反应的自发性由焓变和熵变两个因素决定。N2(g)+O2(g)=2NO(g),已知N≡N的键能为946 kJ∙mol−1 , O=O键的键能为498 kJ∙mol−1 , N≡O的键能为630 kJ∙mol−1;该反应的ΔH=,其反应自发的原因是。
-
(3) 电动汽车的电源常以乙醇(CH3CH2OH)为燃料的固体燃料电池,以熔融的氧化物为电解质,其高温下能传导O2− , 写出负极的电极反应式。
-
(4) 以纯铜作阴极,以石墨作阳极,电解某浓度的硫酸铜溶液,阴极产物均附在电极上,通电一段时间后,关闭电源,迅速撤去电极(设阴极产物没有损耗),若在电解后的溶液中加入16.0gCuO固体,则恰好能使溶液恢复到原浓度,则整个电解过程中,所产生的气体体积为(标准状况)L。
 和
和 转化为CO和
转化为CO和 , 其主要反应如下为
, 其主要反应如下为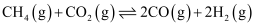 , 该反应历程及能量变化如图1,在发生上述反应的同时,还存在以下反应:
, 该反应历程及能量变化如图1,在发生上述反应的同时,还存在以下反应:积碳反应: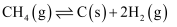
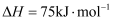
消碳反应: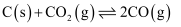
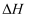
积碳会影响催化剂的的活性。反应相同时间,测得积碳量与反应温度的关系如图2。
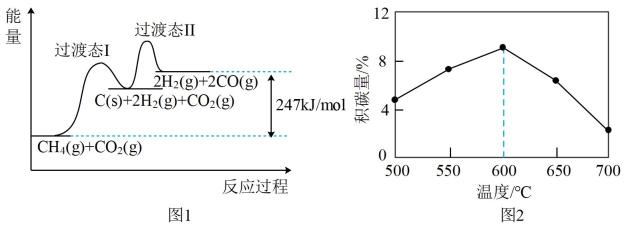
下列说法正确的是( )
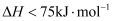 B . 增大
B . 增大 与
与 的物质的量之比有助于减少积碳
C . 温度高于600℃,积碳反应的速率减慢,积碳量减少
D .
的物质的量之比有助于减少积碳
C . 温度高于600℃,积碳反应的速率减慢,积碳量减少
D .  和
和 反应的快慢由反应物→过渡态Ⅰ的速率决定
反应的快慢由反应物→过渡态Ⅰ的速率决定
-
(1) 在催化剂
 作用下,
作用下, 和
和 重整生成
重整生成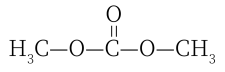 可能的部分反应机理如图所示,其中
可能的部分反应机理如图所示,其中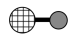 表示
表示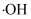 )。
)。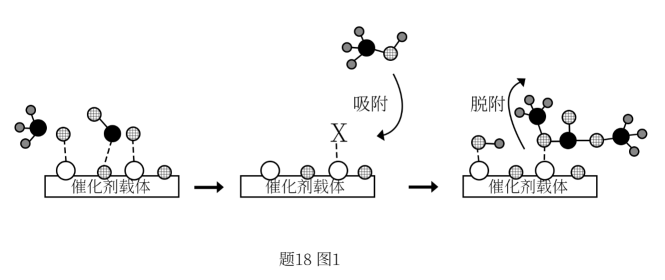
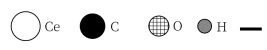 表示原子间存在化学键,表示原子间有吸附作用
表示原子间存在化学键,表示原子间有吸附作用①反应开始时
 在催化剂表面解离为
在催化剂表面解离为 和
和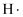 , 该过程首先是
, 该过程首先是 中的氢原子与催化剂载体上的
中的氢原子与催化剂载体上的 形成较为强烈的相互作用。请具体描述
形成较为强烈的相互作用。请具体描述 中的哪一种氢原子与
中的哪一种氢原子与 形成较为强烈的相互作用,并说明判断的理由。
形成较为强烈的相互作用,并说明判断的理由。②X的结构简式为。
-
(2)
 与
与 催化重整制氢气的主反应为
催化重整制氢气的主反应为反应Ⅰ
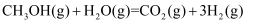
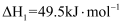
同时还发生副反应:
反应Ⅱ
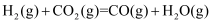
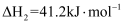
温度在300℃以上,
 也可以直接分解
也可以直接分解反应Ⅲ
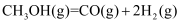
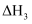
①
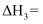
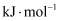
②向该体系中加入适量多孔
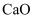 , 会提高
, 会提高 的产率,其原因是。
的产率,其原因是。 -
(3)
 与
与 催化重整制氢气的体系中,平衡时甲醇的转化率、
催化重整制氢气的体系中,平衡时甲醇的转化率、 物质的量分数与反应温度(T)以及初始加入的水醇比(S/M)的关系如图所示。例如:曲线M表示甲醇的平衡转化率均为80%时,所对应的反应温度以及初始加入的水醇比(S/M)。①其他条件相同,当温度低于300℃时,随着温度升高,平衡体系中
物质的量分数与反应温度(T)以及初始加入的水醇比(S/M)的关系如图所示。例如:曲线M表示甲醇的平衡转化率均为80%时,所对应的反应温度以及初始加入的水醇比(S/M)。①其他条件相同,当温度低于300℃时,随着温度升高,平衡体系中 的物质的量分数增大,其可能原因是。
的物质的量分数增大,其可能原因是。②氢能源汽车对氢气中的
 有严格的要求,
有严格的要求, 物质的量分数必须小于0.5%。根据如图所示,催化重整制氢气用于汽车时,适宜控制的水醇比和温度为。
物质的量分数必须小于0.5%。根据如图所示,催化重整制氢气用于汽车时,适宜控制的水醇比和温度为。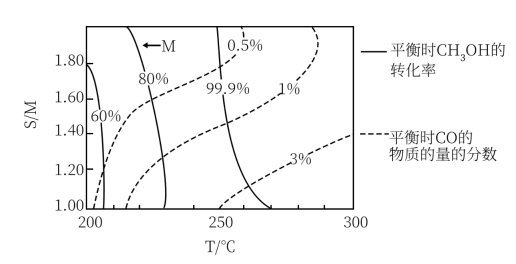
-
(1) 甲烷水蒸气重整制氢:
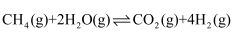
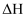
已知:a.

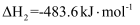 ;
;b.
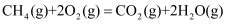
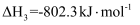 。
。①
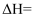
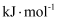 , 为了得到更多的
, 为了得到更多的 , 一般采用的反应条件是(填“高温”、“低温”或“常温”)。
, 一般采用的反应条件是(填“高温”、“低温”或“常温”)。②工业上甲烷水蒸气重整制氢的过程中,经常加入
 吸附剂
吸附剂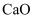 强化[
强化[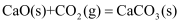
 ],相比于甲烷水蒸气重整,吸附强化甲烷水蒸气重整的优点有、。
],相比于甲烷水蒸气重整,吸附强化甲烷水蒸气重整的优点有、。 -
(2) 甲醇水蒸气重整制氢:甲醇和水蒸气重整时,未使用催化剂和使用催化剂两种反应进程中能量的变化曲线a和b如图所示。
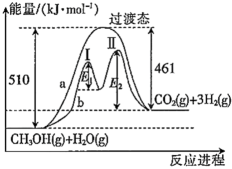
①b过程第Ⅰ步反应和第Ⅱ步反应分别为(填“放热反应”或“吸热反应”,下同)、,第Ⅰ步反应与第Ⅱ步反应的
 (填“>”、“<”或“=”)
(填“>”、“<”或“=”) 。
。②甲醇和水蒸气重整时发生反应的热化学方程式为。
-
(1) 25℃、
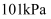 时,
时,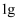 氨气完全燃烧放出
氨气完全燃烧放出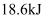 的热量,则
的热量,则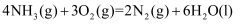
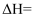
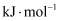 。
。
-
(2)
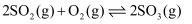 反应过程的能量变化如图所示。
反应过程的能量变化如图所示。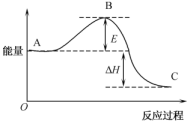
已知:
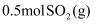 被氧化为
被氧化为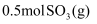 的
的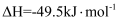 。则:
。则:①E的大小对该反应的反应热(填“有”或“无”)影响;该反应通常用
 作催化剂,加
作催化剂,加 会使图中B点(填“升高”或“降低”)。
会使图中B点(填“升高”或“降低”)。②
 氧化为
氧化为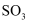 的热化学方程式为。
的热化学方程式为。 -
(3) 已知拆开
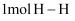 键、
键、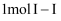 、
、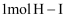 键分别需要吸收的能量为
键分别需要吸收的能量为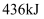 、
、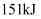 、
、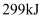 。则由氢气和碘反应生成
。则由氢气和碘反应生成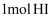 需要(填“放出”或“吸收”)
需要(填“放出”或“吸收”)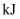 的热量。
的热量。
-
(4) 发射卫星时可用肼(
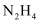 )为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。已知:①

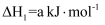
②

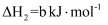
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:。
- 1.设集合,则等于 ( ) A.{1,2} B.{3,4} C.{1} D.{
- You needn’t have taken a taxi. Why didn’t you catchthe last
- 据报道,欧盟最近对奥地利、德国和比利时三国的国家铁路公司开出4800多万欧元罚单。调查发现,这三家铁路公司在跨境铁路整车
- 如图,平面平面ABC,是等腰直角三角形,AC =BC= 4,四边形ABDE是直角梯形,BD∥AE,BDBA,,, 求直线
- (1)已知函数f(x)=x2+lnx-ax 在(0,1)上是增函数,求a的取值范围;(2)在(1)的结论下,设g(x)
- 某同学用石灰石、稀盐酸、浓氢氧化钠溶液等化学试剂和试管,单孔橡皮塞、玻璃导管、可乐瓶、注射器等实验仪器,做了如下实验。
- 用含有少量镁的铝片制取纯净的Al(OH)3,可能有的步骤为:①加盐酸溶解;② 加过量苛性钠溶液;③ 过滤;④ 通入过量C
- 6.依次填入下列各句横线处的成语,最恰当的一组是 ( ) ①阿里巴巴与苏宁联手,显然直指京东。不过,短期内两者的协同
- 完形填空(共20小题,每小题1.5分,满分30分) 阅读下面短文,掌握其大意,然后从16-35各题所给的k^s5*uA.
- 青藏地区自然环境的主要特征是( ) A.高寒 B.干旱 C.冷热变化剧烈
- 阅读杜甫《春夜喜雨》一诗好雨知时节,当春乃发生。 随风潜入夜,润物细无声。 野径云俱黑,江船火独明。 晓看红湿处,花重锦
- 阿里巴巴集团的成功离不开以互联为载体的信息传播渠道的发展。近年来,互联技术的发展,极大促进了信息消费的增长。经测算,到2
- (1)是她那对世界无私的爱丰富了我, 。 (
- 印度地形自北向南依次是A.平原—高原—山地B.平原—山地—高原C.山地—平原—高原D.高原—山地—平原
- 据昌平交通局网上公布,地铁昌平线(一期)2011年1月4日出现上班运营高峰,各站进出站约47600人次. 将47600用
- 深圳气象台发布:强台风“天兔”中心21日21时位于深圳东南方约600千米的洋面上,风雨区半径约300千米左右。预计“
- 2014年7月3日至20日,北京市发展改革委和北京市交通委就北京市公共交通票价改革问题面向社会公开征集意见建议。这是发展
- 国务院总理李克强说,“要把法律放在神圣的位置,无论任何人、办任何事,都不能超越法律的权限,我们要用法治精神来建设现代经济
- (Ⅰ)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合制备甲醇,该反应的热化学方程式为:CO(g)+2H2(g)
- 元素R的气态氢化物的化学式为H2R,下列叙述错误的是( ) A.该元素的原子最外电子层上有6个电子



