物质的结构与性质之间的关系 知识点题库
下图是已经合成的最著名硫-氮化合物分子结构。下列说法正确是( )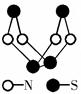
(1)写出元素符号:W为 ,X为 ,Y为 ,Z为 .
(2)W2Z是由 键组成的分子,其电子式为 .
(3)由Y、X、W组成的物质是 键和 键组成的 化合物.
-
(1) 镓元素位于元素周期表的周期族,砷原子核外的电子有种运动状态。
-
(2) Si、P、S 的第一电离能由大到小的顺序是 , 二氧化硅和干冰晶体的熔点差别很大,其原因是。
-
(3) 与AsF3互为等电子体的分子为(只写一中),其空间构型为。
-
(4) 硼酸(H3BO3)本身不能电离出H+ , 在水溶液中易结合一个OH-生成[B(OH)4]- , 而体现弱酸性。
①[B(OH)4]-中B原子的杂化类型为。
②[B(OH)4]-的结构式为。
-
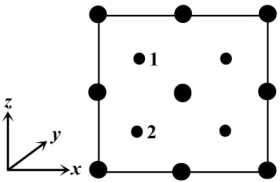
(5) 金刚石的晶胞如图所示,
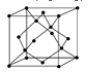
若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅;若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是(用化学式表示);
②金刚石的晶胞参数为a pm(1 pm=10-12 m)。 金刚石晶胞的密度为g/cm3(只要求列算式,阿伏加德罗常数为NA)。
-
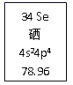
(1) Se元素在周期表中的位置为。表中78.96的意义为。Se原子最外层电子排布的轨道表示式为。
-
(2) 从原子结构角度解释硫的非金属性大于硒。
-
(3) 硒化氢(H2Se)是一种有恶臭味的有毒气体,是一种(选填“极性、或非极性”)分子,其空间结构为型。
-
(4) 工业上常用浓H2SO4焙烧CuSe的方法提取硒,反应产生SO2、SeO2的混合气体,写出反应的化学方程式。理论上该反应每转移1mol电子,可得到SeO2的质量为g,得到SO2在标准状况下的体积为 L。
| 选项 | 规律 | 结论 |
| A | 较强酸可以制取较弱酸 | 次氯酸溶液无法制取盐酸 |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | CH4沸点低于C2H6 |
| D | 活泼金属做原电池的负极 | Mg-Al—NaOH构成原电池,Mg做负极 |
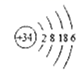
① 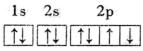 该原子的电子排布图,最外层违背了洪特规则
该原子的电子排布图,最外层违背了洪特规则
②处于最低能量状态原子叫基态原子,1s22s22px1→1s22s22py1过程中形成的是发射光谱
③运用价层电子对互斥理论,CO32-离子的空间构型为三角锥型
④具有相同核外电子排布的粒子,化学性质相同
⑤NCl3中N-Cl键的键长比CCl4中C-Cl键的键长短
-
(1) Sn为ⅣA族元素,单质Sn与干燥Cl2反应生成SnCl4。常温常压下SnCl4为无色液体,SnCl4空间构型为,其固体的晶体类型为。
-
(2) NH3、PH3、AsH3的沸点由高到低的顺序为(填化学式,下同),还原性由强到弱的顺序为,键角由大到小的顺序为。
-
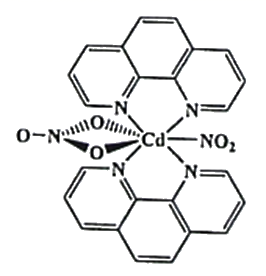
(3) 含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Cd2+配合物的结构如图所示,1mol该配合物中通过螯合作用形成的配位键有mol,该螯合物中N的杂化方式有种。
-
(4) 以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系CdSnAs2的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
坐标
原子
x
y
z
Cd
0
0
0
Sn
0
0
0.5
As
0.25
0.25
0.125
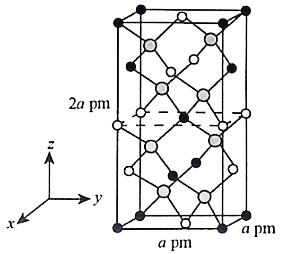
一个晶胞中有个Sn,找出距离Cd(0,0,0)最近的Sn(用分数坐标表示)。CdSnAs2
晶体中与单个Sn键合的As有个。
-
(1) 基态P原子中,电子占据的最高能级符号为,基态N原子核外有种运动状态不同的电子。
-
(2) C、N、O三种元素电负性从大到小的顺序为;第一电离能χ(P)χ(Cl)(填“>”或“<”)。
-
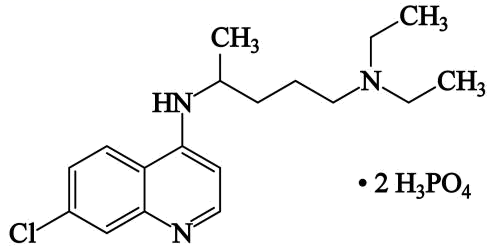
(3) 磷酸氯喹中N原子的杂化方式为,NH3是一种极易溶于水的气体,其沸点比AsH3的沸点高,其原因是。
-
(4) GaN、GaP、GaAs都是很好的半导体材料,晶体类型与晶体碳化硅类似,熔点如表所示,
GaN
GaP
GaAs
熔点/℃
1700
1480
1238
①GaN、GaP、GaAs的熔点变化原因是。
②砷化镓晶体中含有的化学键类型为(填选项字母)。
A.离子键 B.配位键 C.σ键 D.π键 E.极性键 F.非极性键
③以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置。称作原子分数坐标。如图为沿y轴投影的磷化镓晶胞中所有原子的分布图。若原子1的原子分数坐标为(0.25,0.25,0.75),则原子2的原子分数坐标为;若磷化镓的晶体密度为ρg·cm-3 , 阿伏加德罗常数的值为NA , 则晶胞中Ga和P原子的最近距离为pm(用代数式表示)。
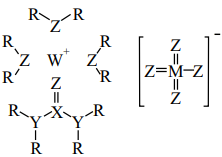
 呈四面体
D . 最高价氧化物对应水化物的酸性:Y<X
呈四面体
D . 最高价氧化物对应水化物的酸性:Y<X
- 下列各句中,没有语病的一句是A.铁道部春运办预计春节后第二个客流高峰将在2月16 日至2月26日出现,高峰日发送旅客将不
- 下列方法中不可用于区别蒸馏水和硬水的是 A.水蒸干后有固体剩
- 1.下列有关哺乳动物成熟红细胞的叙述中,不正确的是 ( ) A.制备细胞膜可用清水处理红细胞
- — Shall we go and ________ hello to the foreignteachers?
- 紫外线指数是度量到达地球表面的太阳紫外线对人类皮肤损伤的程度。世界气象组织及世界卫生组织的一般划分等级为:0~2为低,3
- 某市面积为2000平方千米,人口为50万人,其人口密度为( ) A.25人/平方千米 B.2.5人/平方千
- 下面有关昆虫采集的方法中正确的是( ) A.采集昆虫作标本一定要用采集工具 B.毒杀昆虫一定要先放昆虫在三角纸包中
- 可用酒精灯直接加热的玻璃仪器是( )A.试管 B.烧杯 C.蒸发皿 D.量筒
- 作文 任选其一 (1)家乡的景物是迷人且绚丽多彩的,如名胜古迹、海上日出、月下村景、田野雾岚、苍山奇石、林海晨曦等等。请
- 对渐开线和摆线的理解是本节学习的关键,要理解其形成过程和图象的特点及在实际中的应用,还应该从多方面收集信息.那么,我们可
- 下列词语中加点字的读音完全正确的一项是( ) A.淤滩(yū) 恣睢(suī) 诘难(ji
- The update of the machines should the most advanced
- 下列各项中,对作品故事情节的叙述不正确的两项是 A.陆逊火烧七百里连营,大获全胜。赵云救出刘备,逃往白帝城。陆逊引兵追击
- 某课外小组的同学为了探究不同条件对植物光合作用速率的呼吸作用速率的影响,做了如下实验:用8株各有20片叶片、大小和长势相
- 已知一个半圆形工件,未搬动前如图所示,直径平行于地面放置,搬动时为了保护圆弧部分不受损伤,先将半圆作如图所示的无滑动翻转
- 某种鼠中,黄鼠基因Y对灰鼠基因y为显性,短尾基因T对长尾基因t为显性。且基因Y或t纯合时都能使胚胎致死,这两对基因是独立
- 在下列长度的各组线段中,能组成直角三角形的是( ) A. 5,6,7 B. 5,12,
- 对实验用小白鼠饲喂某种单一食物后,其排泄物中尿素、尿酸含量明显减少,这种食物的主要成分肯定不是( ) A.蛋白质
- 已知抛物线的焦点为,直线与抛物线交于、(在轴上方)两点,若,则实数的值为( ) A.
- 若一束光线从点P(1,0)射出后,经直线x﹣y+1=0反射后恰好过点Q(2,1),在这一过程中,光线从P到Q所经过的最短



