原子结构与元素的性质 知识点题库
核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学论断等高科技领域.已知只有质子数或中子数为奇数的原子核才有NMR现象.试判断下列哪组原子均可产生NMR现象( )
A . 18O、31P、119Sn
B . 27Al、19F、12C
C . 元素周期表中VA族所有元素的原子
D . 元素周期表中第一周期所有元素的原子
已知一般情况下原子核外最外层电子数相等的元素具有相似的化学性质.氟元素原子的核外电子排布示意图为.下列原子中,与氟元素原子的化学性质相似的是( )
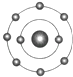
A . 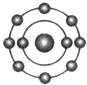 B .
B . 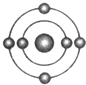 C .
C . 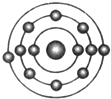 D .
D . 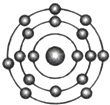
 B .
B .  C .
C .  D .
D . 
下列叙述正确的是( )
A . 40K和40Ca原子中的质子数和中子数都相等
B . 某元素最外层只有一个电子,则它一定是金属元素
C . 任何原子或离子的组成中都含有质子
D . 同位素的不同核素物理、化学性质完全相同
某元素X的气态氢化物的分子式为H2X,则X的最高价含氧酸的分子式为( )
A . H2XO3
B . H2XO4
C . HXO3
D . HXO4
根据部分短周期元素的原子半径及主要化合价信息,判断以下叙述正确的是( )
元素代号 | L | M | Q | R | T |
原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
主要化合价 | +2 | +3 | +2 | +6、﹣2 | ﹣2 |
A . 氢化物的沸点为H2T<H2R
B . 金属性强弱:L<Q
C . M与T形成的化合物的化学式是Al2O3
D . L2+与R2﹣的核外电子数相等
下列关于元素的原子结构与元素性质的叙述正确的是( )
A . 同一元素不可能既表现金属性,又表现非金属性
B . 短周期元素形成离子后,最外层都达到8电子稳定结构
C . 第三周期元素的最高正化合价等于它所处的主族序数
D . 同一主族的元素的原子,最外层电子数相同,化学性质完全相同
某元素B的核电荷数为Z,已知Bn﹣和Am+的核外具有相同的电子层结构,则A元素的原子序数用Z、n、m来表示,应为( )
A . Z+n﹣m
B . Z+m+n
C . Z﹣n﹣m
D . Z﹣n+m
短周期主族元素A、B、C、D、E的原子序数依次递增,A、B两元素相邻,B、C、E原子的最外层电子数之和为13,E原子最外层电子数是B原子内层电子数的3倍,也是C原子最外层电子数的3倍,B、D原子最外层电子数之和等于C、E原子最外层电子数之和.下列说法正确的是( )
A . 原子半径C>D>E,三者形成的简单离子中D离子的半径最小
B . 元素A所形成的氢化物常温下一定为气态
C . 元素C、
D . E在自然界中均不能以游离态存在D.元素B的氧化物对应的水化物一定为强酸
下列说法正确的是( )
A . 元素的种类由最外层电子数决定
B . 化学键是存在于分子、原子和离子间的作用力
C . 原子的种类由原子核内质子数与中子数共同决定
D . 化学反应速率可以决定反应的限度
下列关于物质结构的说法中正确的是( )
A . BF3、HClO分子中所有原子都满足最外层8电子结构
B . 某元素原子最外层电子数是次外层电子数的a(a为整数)倍,则该原子核内质子数为2a+2
C . D2O分子与H2O分子是所含电子总数不相等的分子
D . 在任何物质分子中都含有化学键
X、Y是短周期元素,二者能形成化合物X2Y3 . 若已知X的原子序数为n,则Y的原子叙述不可能是( )
A . n+11
B . n﹣5
C . n+3
D . n+4
下列说法中正确的是( )
A . 核外电子排布完全相同的两种微粒,其化学性质一定相同
B . 具有固定熔点或沸点的物质一定是纯净物
C . 一种离子和一种分子的质子数和电子数不可能同时相等
D . 由分子构成的物质中一定含有共价键
A,B,C,D,E,F代表6种元素.请填空:
-
(1) A元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素符号为;
-
(2) B元素的负二价离子和C元素的正一价离子的电子层结构都与氩相同,C的元素符号为,B和C形成化合物的电子式;
-
(3) D元素的正三价离子的3d能级为半充满,D的元素符号为,其基态原子的电子排布式为;
-
(4) E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素号为,其正二价的电子排布式为.
-
(5) F元素的原子最外层电子排布式为nsnnpn+1 , 则n=;原子中能量最高的是电子.
回答下列相关问题:
-
(1) 用“>”或“<”填写下表:
电负性
第一电离能
熔点
沸点(同压)
在水中溶解性
CH
SP
NaFKCl
PH3NH3
CH3OHCH3SH
-
(2) 某半导体材料由X、Y两种元素组成,已知X的基态原子4p轨道上只有1个电子,Y的基态原子L层上有3个未成对电子。X位于周期表第周期族;该半导体材料的化学式为。
-
(3) 由极性共价键构成的非极性分子是(填序号)。
a.P4
b.COS
c.CH3OCH3
d.BCl3
-
(4) 雷氏盐(Reinecke's salt)结构式如下图所示:
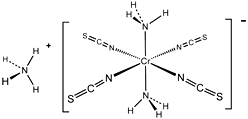
配离子中Cr3+的配体为(填化学式),Cr3+与配体间形成的共价键又称为。
下列各组原子中,彼此化学性质一定相似的是( )
A . 原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子
B . 2p轨道上只有2个电子的X原子与3p轨道上只有2个电子的Y原子
C . 原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子
D . 最外层都只有一个电子的X、Y原子
已知钠的结构示意图为Na 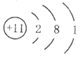 ,下列说法错误的是( )
,下列说法错误的是( )
 ,下列说法错误的是( )
,下列说法错误的是( )
A . 该元素的化合价为2
B . 该元素位于第三周期
C . 该元素位于第1A族
D . 该元素易失最外层1个电子
短周期的三种元素X、Y、Z,已知X元素的原子核外只有一个电子,Y元素的原子M层上的电子数是它的内层电子总数的一半,Z元素原子的L层上的电子数比Y元素原子的L层上的电子数少2个,则这三种元素所组成的化合物的化学式不可能是( )
A . X2YZ4
B . XYZ3
C . X3YZ4
D . X4Y2Z7
元素的化学性质主要取决于原子的( )
A . 原子序数
B . 核外电子数
C . 核内中子数
D . 最外层电子数
若aAm+与bBn-的核外电子排布相同,则下列关系错误的是( )
A . 离子半径aAm+<bBn-
B . 原子半径A<B
C . A的原子序数比B的原子序数大(m+n)
D . b=a-n-m
科学家最近发现两种粒子:第一种是由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”;第二种是由四个氧原子构成的分子。下列有关这两种粒子的说法错误的是( )
A . “四中子”的粒子不显电性
B . “四中子”的质量数为4
C . 第二种粒子是氧元素的另一种同位素
D . 第二种粒子的化学式为O4
最近更新
- 某同学用天平测量物体质量时,通过加减砝码总发现指针在分度盘偏左一点,这时他应该
- 有关坐物体内ATP的叙述,错误的是 A线粒体合成的ATP可在细胞核中发挥作用 B.在代谢旺盛的细胞中AT
- 各组词语中有两个错别字的一组是( ) A.冒然 奖掖 纯厚朴实 行若狗彘 B.呕气 福祉 头昏脑胀以
- “入乡随俗”表明了 A.对传统文化的继承 B.优秀文化取代落后文化 C.尊重文化的多样性
- 已知等比数列首项为3,公比,对给定的,设是首项为,公差为的等差数列,(Ⅰ)求的前10项之和; (Ⅱ)设为数列的第项,,求
- 一路风雪一路歌 ①他的一生再平凡不过,可是他从未
- --What does your mother do to keep healthy,Tim? --S
- 下列反应中前者属于取代反应,后者属于加成反应的是() A.甲烷与氯气混和后光照反应 ;乙烯使酸性高锰酸钾溶液的褪色 B.
- 近年来,一些地方名贵特产在商家疯狂炒作下,价格一路飙升,频频刷新“天价”。江苏名产阳澄湖大闸蟹运至北京超市,卖到每斤32
- 下列叙述中正确的是 A.某ⅡA族元素的原子序数为a,则原子序数为a+1的元素一定是ⅢA族元素 B.除短周期外,其他周期均
- 一个物体从H高处自由落下,当其速度达到着地速度的一半时,下落的高度为( )A. B.
- 血液由 和 组成。
- People can do shopping in different ways.For several years,p
- 若不等式x2+ax+1³0对于一切xÎ(0,)成立,则a的取值范围是 ( ) A. B.
- 中国首架大飞机有望于2017年升空,在大飞机全球市场份额上,将排在波音、空客之后,位列第三。大飞机处于产业链的顶端,是拉
- It has been my lifelong dream to play on the middle school b
- 许多既有趣味性又富含哲理的歇后语与动物有关。如:“地里的蚯蚓—能屈能伸”,“长颈鹿的脖子丹顶鹤的腿—各有所长”,“春蚕结
- (1)求实数k的取值范围; (2)若△AOB的面积 s=24,求k.
- 在下面这段文字的横线上填上恰当的句子,要求符合上下文特定的语意。(4分) 白春礼院士把“青年”的英文大写YOUTH进行了
- 已知二次函数y=x2+bx+c的图像与x轴的两个交点的横坐标分别为x1、x2,一元二次方程x2+b2x+20=0的两实根



