原子结构与元素的性质 知识点题库
X元素最高价氧化物对应的水化物为H3XO4 , 则它对应的气态氢化物为( )
A . HX
B . H2X
C . XH4
D . XH3
下表是部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是( )
元素代号 | L | M | Q | R | T |
原子半径/nmm | 0.160 | 0.134 | 0.089 | 0.102 | 0.074 |
主要化合价 | +2 | +3 | +2 | +6、﹣2 | ﹣2 |
A . L2+与R2﹣的核外电子数相等
B . L与T形成的化合物具有两性
C . L和Q金属性:Q<L
D . 氢化物的稳定性为H2T<H2R
几种短周期元素的原子半径及主要化合物如表所示:
元素代号 | X | Y | Z | W |
原子半径/pm | 160 | 143 | 70 | 66 |
主要化合价 | +2 | +3 | +3、+5、﹣3 | ﹣2 |
下列叙述正确的是( )
A . Z的最高价氧化物对应水化物与其氢化物能发生化合反应生成离子化合物
B . 一定条件下,Z单质与W的常见单质直接生成ZW2
C . Y的最高价氧化物对应的水化物能溶于稀氨水
D . 相同条件下,X,Y的单质分别与盐酸反应时,后者反应剧烈些
在元素周期表短周期中的X和Y两种元素可组成化合物XY3 , 下列说法正确的是( )
A . XY3一定是离子化合物
B . 若Y的原子序数为m,X的原子序数一定是m±4
C . X和Y可属同一周期,也可属于两个不同周期
D . XY3一定不属于同一主族
X,Y均为元素周期表ⅦA族中的两种元素.下列叙述中,能够说明X的原子得电子能力比Y强的是( )
A . 原子的电子层数:X>Y
B . 对应的简单离子的还原性:X>Y
C . 气态氢化物的稳定性:X>Y
D . 氧化物对应水化物的酸性:X>Y
已知五种短周期元素的原子半径及主要化合价如表,判断以下叙述不正确的是( )
元素代号 | L | M | Q | R | T |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
主要化合价 | +2 | +3 | +6、﹣2 | +2 | ﹣2 |
A . T,Q的氢化物常温常压下均为无色气体
B . L,M的氢氧化物碱性:L>M
C . L与Q形成的化合物属于离子化合物
D . M与T形成的化合物具有两性
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
A . 元素A,B组成的化合物常温下一定呈气态
B . 元素C,D的最高价氧化物对应的水化物之间不能发生反应
C . 工业上常用电解法制备元素C,D,E的单质
D . 化合物AE与CE有相同类型的化学键
短周期元素A、B、C、D的原子序数依次递增,它们的核电荷数之和为32,各原子最外层电子数之和为10.A与C同主族,B与D同主族,A、C原子的最外层电子数之和等于B原子的次外层电子数.则下列叙述不正确的是( )
A . D元素处于元素周期表中第三周期ⅣA族
B . 四种元素的原子半径:A<B<D<C
C . B,D的氧化物均为酸性氧化物
D . 一定条件下,B单质能置换出D单质,C单质能置换出A单质
某元素最高价含氧酸的化学式是HRO3 , 该元素的气态氢化物化学式可表示为( )
A . HR
B . H2R
C . RH3
D . 不能确定
氮化硅是一种新型陶瓷材料的主要成分,能承受高温,可用于制造业、航天业等领域.图是氮、硅的原子结构示意图,请推测氮化硅的化学式(分子式)为( )
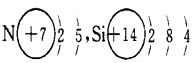
A . Si4N3
B . Si3N4
C . Si3N7
D . Si7N3
X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是( )
A . 若原子半径X>Y,则气态氢化物稳定性:HmX<HnY
B . X、Y一定不是同周期元素
C . 由mXa﹣与nYb﹣得m+a=n﹣b
D . Xa﹣的还原性一定强于Yb﹣
下列A、B两种元素的原子序数,其中可以组成A2B型离子化合物的是( )
A . 6和8
B . 19和16
C . 17和12
D . 1和8
周期表中16号元素和4号元素的原子相比较,前者的下列数据是后者的4倍的是( )
A . 电子数
B . 最外层电子数
C . 电子层数
D . K层电子数
根据如图的原子结构示意图回答下列问题.
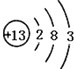
-
(1) 该原子的核内质子数为.
-
(2) 该原子在化学反应中表现为较易(填“得”或“失”)电子.
-
(3) 写出该元素组成的单质与稀盐酸反应的化学方程式.
W粒子的结构如图所示,下列关于它的说法不正确的是( )
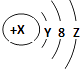
A . Y=2
B . 若X=18,则Z=8
C . 若X=17,它的最高价氧化物化学式为W2O7
D . 若X=14,它的氢化物的化学式为H2W
已知A、B、C均为短周期元素,A的P能级上只有一对成对电子,A和B是同周期相邻的两种元素,B、C两种元素组成的五原子一价阳离子含10个电子,请回答:
-
(1) A元素的电子排布式为.
-
(2) A、B、C可组成化学式C4B2A3的物质是(填“离子”或“共价”)化合物.
-
(3) B、C两种元素组成的五原子离子的中心原子杂化方式为,该离子的空间构型为.
-
(4) 化合物BC3是(“极性”或“非极性”)分子.
原子序数为x的元素R.在周期表中位于A,B,C,D 4种元素的中间.A,B,C,D 4种元素的原子序数之和不可能为( )
| C |
|
A | xR | B |
| D |
|
A . 4x
B . 4x+10
C . 4x+5
D . 4x+14
有A,B,C,D,E,F 六种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6 L H2 , E的阳离子与A的阴离子核外电子层结构完全相同,F原子半径在短周期元素中最大,回答下列问题:
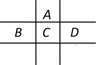
-
(1) 元素的名称:B;
-
(2) 画出C离子的结构示意图:;
-
(3) 写出D元素在周期表中的位置:;D元素的单质可用于制漂白液和漂白粉,写出制漂白液的离子方程式:,漂白粉的有效成分是;
-
(4) B的同族上一周期元素的氢化物为(化学式) ,实验室制取该物质的方程式为,制取该气体时用做干燥剂。
根据下列四种粒子的结构示意图,所获取的信息正确的是( )
![]()
A . 它们表示四种元素
B . ①④表示的是阳离子
C . ④表示的元素是非金属元素
D . ②表示的元素在化合物中通常显+2价
下列各分子中所有原子都满足最外层8电子稳定结构且共用电子对发生偏移的是( )
A . BeCl2
B . PCl3
C . PCl5
D . N2
最近更新
- 若{a,b,c}为空间的一组基底,则下列各项中,能构成基底的一组向量是()A.a,a+b,a-bB.b,a+b,a-bC
- 阅读下面文字,回答问题。(4分)路边开满了带刺的蔷薇花,三个步行者打这里路过。第一个脚步匆匆。他什么也没看见。第二个感慨
- (12分)在△ABC中,A、B、C的对边分别为a、b、c,且 成等差数列.(Ⅰ)求B的值;(Ⅱ)求的范围.
- 下列除杂方法不正确的是()实验目的 方案设计 A 除去CO混有的少量CO2 将混合气体通入氢氧化钠溶液 B 除去生石灰C
- 相同质量的下列烃,完全燃烧时,需要氧气最多的是( ) A CH4 B C2H4
- 鱼,我所欲也;熊掌,亦我所欲也。二者不可得兼,__________________。
- 四棱锥P-ABCD中,底面ABCD为菱形,且, 侧面PAD是正三角形,其所在的平面垂直于底面ABCD, 点G为AD的中点
- 已知25 ℃、101 kPa条件下: (1)4Al(s)+3O2(g)===2Al2O3(s) ΔH=-2 834.9
- 用“/”给下面句子断句 子曰好勇疾贫乱也人而不仁疾之已甚乱也
- 公元1050年,范仲淹在杭州知州任上遇到大饥荒。范仲淹没有延用发粟救济之常规,而是实施了“荒政三策”。一是利用饥岁工价至
- 电视机的遥控器是利用 线实现遥控的;医院里用 线杀死微生物,达到灭菌的目的。
- 若变量x,y满足约束条件则的最小值为 A. B.6 C.
- 下列不符合现代化学研究方向的是 ( ) A.发现新物质 B.合成新材料 C.研究化
- 3.货币是商品交换长期发展的产物,货币的本质是一般等价物。金、银充当货币后,可以与一切商品相交换,这表明( ) A
- (15分) “宁夏红”枸杞果酒是利用我国宁夏回族自治区新鲜枸杞为原料,采用传统酿造技术与现代生物技术结合酿制而成。下面是
- 下列情况会对人体健康造成较大危害的是( )A.自来水中通入少量Cl2进行消毒杀菌B.用明矾净水C.用食醋清洗热水瓶
- 如图所示,一导体圆环位于纸面内,O为圆心。环内两个圆心角为90°的扇形区域内分别有匀强磁场,两磁场磁感应强度的大小相等,
- ---How do you like the film? ---There was nothing special
- 用分子的相关知识解释下列生活中的现象,其中错误的是( ) A. “酒香不怕巷子深”,说明分子在
- 2015年,国家进一步落实了支持小型和微型企业发展的金融、财税政策措施。对国家支持小、微型企业发展的理解正确的有 ①支持



